よむ、つかう、まなぶ。
【参考資料6】抗微生物薬適正使用の手引き 第三版 補遺 (27 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_45318.html |
| 出典情報 | 厚生科学審議会 感染症部会 薬剤耐性(AMR)に関する小委員会 抗微生物薬適正使用(AMS)等に関する作業部会(第6回 11/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
「1 回 3g-4.5g を 6 時間毎、静脈内に投与」した場合、当該使用事例を審査上認める。
』と記載が
ある。
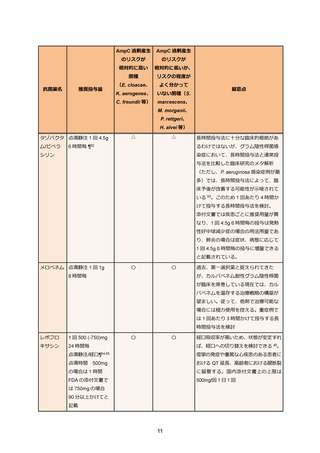
ミノサイクリンは、IDSA による治療ガイドラインでは 200mg 12 時間毎を推奨しているが 40、
添付文書上の最大投与量 200mg/日を超える。
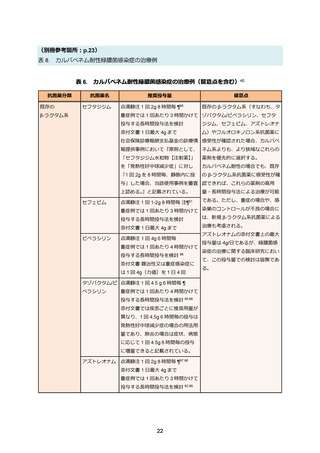
チゲサイクリンの添付文書での用法用量は、「通常、成人には、チゲサイクリンとして初回用
量 100mg を 30-60 分かけて点滴静脈内投与、以後 12 時間毎に 50mg を 30-60 分かけて点滴静脈
内投与する。
」である 86。
(別冊参考箇所:p.28-29)
1. 入院患者の感染症で問題となる微生物>(5) その他のグラム陰性桿菌(緑膿菌以外のブドウ糖
非発酵菌)>(ii) ステノトロフォモナス・マルトフィリア(Stenotrophomonas maltophilia)
<微生物検査に関する留意事項>
レボフロキサシン・セフタジジムにおいては、ディスク法や E-test、及び頻用されている微生
物感受性分析装置において再現性に懸念があることが報告されており 144,145、解釈に注意を要す。
また、ST 合剤以外の薬剤に関しては薬剤感受性結果と治療アウトカムの関連を支持するデータ
が乏しいことにも留意する必要がある 40,146。
さらに、S. maltophilia は近年保険適用となった、多項目遺伝子関連検査、特にマルチプレック
ス PCR 法やマイクロアレイ法による血液培養陽性培養液に対する細菌核酸・薬剤耐性遺伝子同
時検出システムにおいて、検出対象となっていない製品もあるため、注意を要する(「Verigene®
血液培養グラム陰性菌・薬剤耐性核酸テスト(BC-GN)」、「FilmArray®血液培養パネル」では検
出対象外、
「BioFire®血液培養パネル 2」では検出対象に含まれる)。
<薬剤耐性の機序>
S. maltophilia は内因性に L1・L2 と呼ばれる 2 種類の β-ラクタマーゼを保有する 139。L1 はメ
タロ-β-ラクタマーゼでカルバペネム系を含む幅広い β-ラクタム系抗菌薬(アズトレオナムを除
く)を分解することが可能で、一方、L2 は Class A に分類される β-ラクタマーゼで広域スペクト
ラムのセファロスポリン系抗菌薬及びアズトレオナムを分解可能である。また、アミノグリコシ
ド系抗菌薬についても内因性に保有する薬剤排泄ポンプ等複数の耐性機構を備えている 139。フ
ルオロキノロン系抗菌薬に対しても、薬剤排泄ポンプの過剰発現や変異、薬剤の作用点である
DNA gyrase・トポイソメラーぜ IV を保護する Smqnr の過剰発現等複数の耐性機構をもつ 140,141
治療の第一選択とされるスルファメトキサゾール/トリメトプリム(ST 合剤)に対しても、薬剤
排泄ポンプの過剰発現やプラスミドを介した class I integron による sul・dfrA の獲得により耐性
化することが知られている 142,143。
27
』と記載が
ある。
ミノサイクリンは、IDSA による治療ガイドラインでは 200mg 12 時間毎を推奨しているが 40、
添付文書上の最大投与量 200mg/日を超える。
チゲサイクリンの添付文書での用法用量は、「通常、成人には、チゲサイクリンとして初回用
量 100mg を 30-60 分かけて点滴静脈内投与、以後 12 時間毎に 50mg を 30-60 分かけて点滴静脈
内投与する。
」である 86。
(別冊参考箇所:p.28-29)
1. 入院患者の感染症で問題となる微生物>(5) その他のグラム陰性桿菌(緑膿菌以外のブドウ糖
非発酵菌)>(ii) ステノトロフォモナス・マルトフィリア(Stenotrophomonas maltophilia)
<微生物検査に関する留意事項>
レボフロキサシン・セフタジジムにおいては、ディスク法や E-test、及び頻用されている微生
物感受性分析装置において再現性に懸念があることが報告されており 144,145、解釈に注意を要す。
また、ST 合剤以外の薬剤に関しては薬剤感受性結果と治療アウトカムの関連を支持するデータ
が乏しいことにも留意する必要がある 40,146。
さらに、S. maltophilia は近年保険適用となった、多項目遺伝子関連検査、特にマルチプレック
ス PCR 法やマイクロアレイ法による血液培養陽性培養液に対する細菌核酸・薬剤耐性遺伝子同
時検出システムにおいて、検出対象となっていない製品もあるため、注意を要する(「Verigene®
血液培養グラム陰性菌・薬剤耐性核酸テスト(BC-GN)」、「FilmArray®血液培養パネル」では検
出対象外、
「BioFire®血液培養パネル 2」では検出対象に含まれる)。
<薬剤耐性の機序>
S. maltophilia は内因性に L1・L2 と呼ばれる 2 種類の β-ラクタマーゼを保有する 139。L1 はメ
タロ-β-ラクタマーゼでカルバペネム系を含む幅広い β-ラクタム系抗菌薬(アズトレオナムを除
く)を分解することが可能で、一方、L2 は Class A に分類される β-ラクタマーゼで広域スペクト
ラムのセファロスポリン系抗菌薬及びアズトレオナムを分解可能である。また、アミノグリコシ
ド系抗菌薬についても内因性に保有する薬剤排泄ポンプ等複数の耐性機構を備えている 139。フ
ルオロキノロン系抗菌薬に対しても、薬剤排泄ポンプの過剰発現や変異、薬剤の作用点である
DNA gyrase・トポイソメラーぜ IV を保護する Smqnr の過剰発現等複数の耐性機構をもつ 140,141
治療の第一選択とされるスルファメトキサゾール/トリメトプリム(ST 合剤)に対しても、薬剤
排泄ポンプの過剰発現やプラスミドを介した class I integron による sul・dfrA の獲得により耐性
化することが知られている 142,143。
27