よむ、つかう、まなぶ。
【医薬品・医療機器等安全性情報No.416】 (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000185468_00019.html |
| 出典情報 | 医薬品・医療機器等安全性情報 416号(1/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
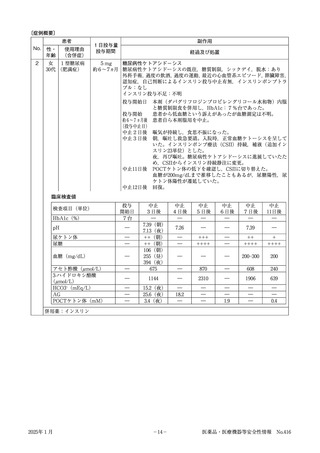
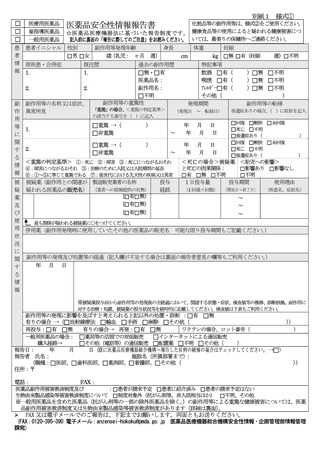
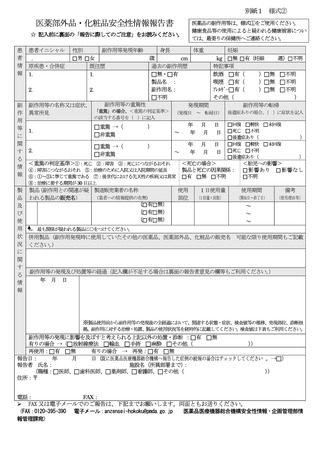
〔症例概要〕
患者
No.
性・
年齢
1
男 肝細胞癌
80代 (高血圧,
うっ
血性心不全,
認知症)
使用理由
(合併症)
副作用
1日投与量
投与期間
400mg
3日間
経過及び処置
腫瘍崩壊症候群
投与開始日 肝細胞癌に対して本剤投与開始。
投与3日目 腫瘍崩壊症候群が発現。
(投与中止日) カリウム:6.3mEq/L,尿素窒素:58mg/dL,無機リン:5.4mg/
dL,尿酸:11.2mg/dLに上昇。本剤投与中止し,アロプリノー
ル100mg,補液負荷2000mL/日,フロセミド40mg/日投与開
始。
中止1日後 急性膵炎が発現。
ナファモスタットメシル酸塩30mg/日投与開始。
CT検査(胸部~骨盤[単純]):肝右葉の肝細胞癌に大きな変
化認めず。
中止2日後 ナファモスタットメシル酸塩を60mg/日に増量。炭酸水素ナ
トリウム40mL追加投与。
中止7日後 腹部超音波検査(肝臓)
:辺縁鈍化,表面平滑であり,内部
に粗雑な印象は乏しい。肝右翼に直径70mm大の高低輝度混
在の腫瘤を認める。CTと比較し,大きさの著変はないが,
低輝度の領域は壊死が疑われる。
中止8日後 腫瘍崩壊症候群は回復。補液投与終了。
中止15日後 急性膵炎は軽快。
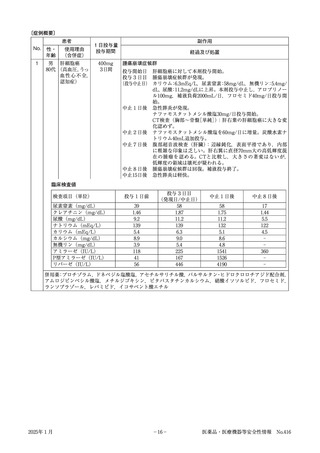
臨床検査値
検査項目(単位)
尿素窒素(mg/dL)
クレアチニン(mg/dL)
尿酸(mg/dL)
ナトリウム(mEq/L)
カリウム(mEq/L)
カルシウム(mg/dL)
無機リン(mg/dL)
アミラーゼ(IU/L)
P型アミラーゼ(IU/L)
リパーゼ(IU/L)
投与1日前
39
1.46
9.2
139
5.4
8.9
3.9
118
41
56
投与3日目
(発現日/中止日)
58
1.87
11.2
139
6.3
9.0
5.4
225
167
446
中止1日後
中止8日後
58
1.75
11.2
132
5.1
8.6
4.8
1541
1526
4190
17
1.44
5.5
122
4.5
360
-
併用薬:ブロチゾラム,ドネペジル塩酸塩,アセチルサリチル酸,バルサルタン・ヒドロクロロチアジド配合剤,
アムロジピンベシル酸塩,メチルジゴキシン,ピタバスタチンカルシウム,硝酸イソソルビド,フロセミド,
ランソプラゾール,レバミピド,イコサペント酸エチル
2025年1月
-16-
医薬品・医療機器等安全性情報
No.416
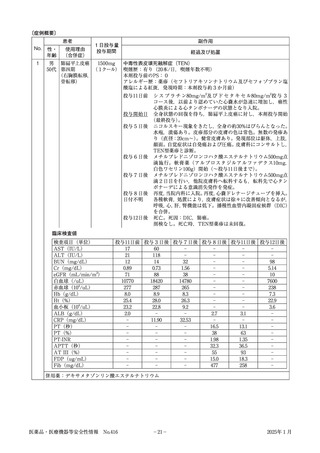
患者
No.
性・
年齢
1
男 肝細胞癌
80代 (高血圧,
うっ
血性心不全,
認知症)
使用理由
(合併症)
副作用
1日投与量
投与期間
400mg
3日間
経過及び処置
腫瘍崩壊症候群
投与開始日 肝細胞癌に対して本剤投与開始。
投与3日目 腫瘍崩壊症候群が発現。
(投与中止日) カリウム:6.3mEq/L,尿素窒素:58mg/dL,無機リン:5.4mg/
dL,尿酸:11.2mg/dLに上昇。本剤投与中止し,アロプリノー
ル100mg,補液負荷2000mL/日,フロセミド40mg/日投与開
始。
中止1日後 急性膵炎が発現。
ナファモスタットメシル酸塩30mg/日投与開始。
CT検査(胸部~骨盤[単純]):肝右葉の肝細胞癌に大きな変
化認めず。
中止2日後 ナファモスタットメシル酸塩を60mg/日に増量。炭酸水素ナ
トリウム40mL追加投与。
中止7日後 腹部超音波検査(肝臓)
:辺縁鈍化,表面平滑であり,内部
に粗雑な印象は乏しい。肝右翼に直径70mm大の高低輝度混
在の腫瘤を認める。CTと比較し,大きさの著変はないが,
低輝度の領域は壊死が疑われる。
中止8日後 腫瘍崩壊症候群は回復。補液投与終了。
中止15日後 急性膵炎は軽快。
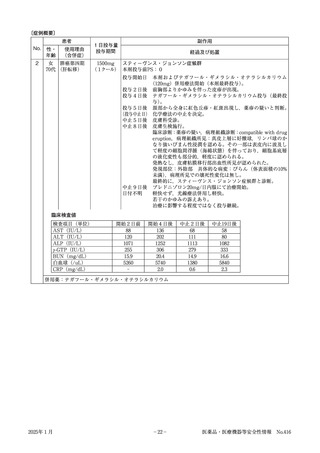
臨床検査値
検査項目(単位)
尿素窒素(mg/dL)
クレアチニン(mg/dL)
尿酸(mg/dL)
ナトリウム(mEq/L)
カリウム(mEq/L)
カルシウム(mg/dL)
無機リン(mg/dL)
アミラーゼ(IU/L)
P型アミラーゼ(IU/L)
リパーゼ(IU/L)
投与1日前
39
1.46
9.2
139
5.4
8.9
3.9
118
41
56
投与3日目
(発現日/中止日)
58
1.87
11.2
139
6.3
9.0
5.4
225
167
446
中止1日後
中止8日後
58
1.75
11.2
132
5.1
8.6
4.8
1541
1526
4190
17
1.44
5.5
122
4.5
360
-
併用薬:ブロチゾラム,ドネペジル塩酸塩,アセチルサリチル酸,バルサルタン・ヒドロクロロチアジド配合剤,
アムロジピンベシル酸塩,メチルジゴキシン,ピタバスタチンカルシウム,硝酸イソソルビド,フロセミド,
ランソプラゾール,レバミピド,イコサペント酸エチル
2025年1月
-16-
医薬品・医療機器等安全性情報
No.416