よむ、つかう、まなぶ。
【参考資料1】テーマ②(新技術による医薬品等にも対応したリスクに基づく市販後安全性対策の強化、法違反事例を踏まえた更なる法令遵守や品質確保の取組の実施)について(参考資料).pdf (26 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_41209.html |
| 出典情報 | 厚生科学審議会 医薬品医療機器制度部会(令和6年度第4回 7/5)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
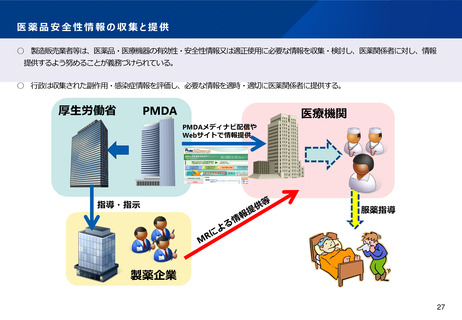
医薬品安全性情報の収集と提供
○ 製造販売業者等は、医薬品・医療機器の有効性・安全性情報又は適正使用に必要な情報を収集・検討し、医薬関係者に対し、情報
提供するよう努めることが義務づけられている。
○ 行政は収集された副作用・感染症情報を評価し、必要な情報を適時・適切に医薬関係者に提供する。
厚生労働省
PMDA
医療機関
副作用報告
副作用報告
製薬企業
26
○ 製造販売業者等は、医薬品・医療機器の有効性・安全性情報又は適正使用に必要な情報を収集・検討し、医薬関係者に対し、情報
提供するよう努めることが義務づけられている。
○ 行政は収集された副作用・感染症情報を評価し、必要な情報を適時・適切に医薬関係者に提供する。
厚生労働省
PMDA
医療機関
副作用報告
副作用報告
製薬企業
26