よむ、つかう、まなぶ。
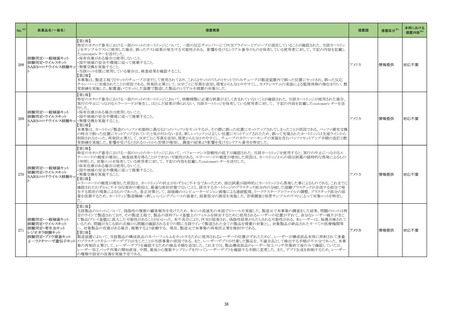
【資料5】医薬局からの定期報告 (40 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_37109.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第14回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
No.※2
医薬品名(一般名)
措置概要
措置国
クラスⅡ生化学・免疫・内分泌
検査用シリーズ
【第1報】
トロポニンキット
当該製品において技能試験用検体中のトロポニンの回収率が低いという苦情から、トロポニンの結果が低値に偏る可能性があることが確認され、海外製造元は、直ちに使
ミオグロビンキット
275
用を中止し代替手段で対応することが通知した。海外製造元において原因が原材料にあると特定され、再発防止のため工程試験が追加された。
アメリカ
クレアチンキナーゼアイソザイ
【第2報】
ムキット
特定ロットのTnI抗体が使用されたデバイスロットを回収対象とした。
ヒト脳性ナトリウム利尿ペプチ
ド前駆体N端フラグメントキット
措置区分※3
本邦における
措置内容※4
回収
対応不要
核酸同定・ブドウ球菌キット
核酸同定・一般細菌キット
【第1報】
製造元は、一部の顧客が、当該製品について既に技術的な切り替えを完了し、新しいキットの使用を開始したにもかかわらず、古いキットを受け取ったことを確認した。旧
キットと新キットの試薬カートリッジは同じだが、新キットは、変異SCC株によるメチシリン耐性結果の偽陰性の発生を減らすことを目的にアルゴリズム更新を含む新しい試験
定義ファイルを使用している。 メチシリン耐性黄色ブドウ球菌陽性検体から変異SCC株を検出した場合、メチシリン耐性結果が偽陰性になる可能性がある。このような偽陰
性は、抗生物質の変更により疾患が進行する可能性があり、一般集団に対する永続的な危害、および予後を脅かす危害の可能性は低いが、高リスクの集団に対しては、
生命を脅かす危害の恐れがある。 本件の対処として、製造元は使用者に対し在庫確認を依頼し、旧キットの未使用試薬カートリッジの在庫があり、新キットに切り替えた場 フランス
合には、旧キットの試薬カートリッジを交換、あるいは旧キットの使用を中止し、廃棄するよう注意喚起した。製造元は、新バージョンに切り替わった国での旧バージョンの
取り扱いを終了する。
【第2報】
新バージョンのキットを受注したにもかかわらず、誤って旧バージョンのキットを受注入力し、出荷してしまったことが根本原因である。製造元による再発防止策として、新
バージョンの流通を開始した地域には、誤って旧バージョンが出荷できないよう対策した。
情報提供
対応不要
クロストリジウム・ディフィシル
核酸キット
277
核酸同定・一般細菌キット
核酸同定・ウイルスキット
製造元における調査の結果、特定ロットのスワブの疎水性の問題により、まれに偽陰性の結果を示す可能性があることが確認された。特定ロットのスワブを含む製品の全
てのロットを自主回収することになった。 製造元は、スワブの全てのロットを評価した上で、当該ロットのみに問題があることを確認した。 現在、製造元にて原因を調査中で アメリカ
ある。 なお、本件は2022年に実施した措置の再発である。
回収
対応不要
278 トロポニンキット
製造元において、特定ロットで患者検体および精度管理試料を測定した場合に不正確な結果が出力される可能性があることが確認された。そのため、当該製品を使用す
る顧客に当該ロットの使用を中止するよう通知するための顧客案内を実施した。製造元において、特定のアッセイ試薬の製造のために使用されたリガンドウェルが、別の
アッセイ試薬の製造に使用されたことが確認された。別のアッセイ試薬のリガンドウェルが測定に使用された場合、正しいシグナル(発光強度)が得られず、キャリブレーショ
ンが失敗する、精度管理が規格範囲から外れる、あるいは患者検体を測定したときに不正確な結果が出力される可能性がある。製造元では使用期限内の全ての製品の
製造記録を確認し、対象ロットを特定した。他のアッセイ試薬は適切なリガンドウェルを使用して製造されたことを確認している。本事象の原因は、担当者が手順書に記載 アメリカ、
されたラインクリアランスの作業を適切に実施せず、直前に製造したアッセイ試薬のリガンドウェルがセットされたプレートを除去せずに、次の製造を開始してしまったことで カナダ
あることが確認された。また、前製造バッチで使用されたプレートが、次の製造バッチで再架設されたことを検出するシステム管理上の機能が無く、本事象が見逃されたこ
とが確認された。製造元では再発防止策として、製造バッチ毎にプレートIDをシステム上で管理し、チェックできる機能を追加した。これにより誤ったプレートIDが製造に使
用されないようにシステム上で製造開始前にチェックできる。また、製造元ではラインクリアランスに関連する手順書のレビューおよび担当者への教育訓練の実施を予定し
ている。
情報提供
対応不要
血液検査用グルコースキット 海外製造元は当該製品の一部ロットを血液ガス分析装置の特定のソフトウェアバージョンとの組み合わせで使用した場合、報告可能な範囲の下限濃度の検体でグルコー
乳酸キット
ス値が乖離し、高値になることを確認した。海外製造元における予備調査の結果、根本原因はソフトウェアに起因しないが、次のバージョンでは本事象の発生が軽減され
279
欧州連合
血液検査用クレアチニンキット ることが確認されており、ソフトウェアバージョンのアップデート後は、該当ロットを通常通り使用することが可能である。海外製造元では、血液ガス分析装置のソフトウェア
血液検査用尿素窒素キット
アップデートを顧客に依頼する。
情報提供
対応不要
製造元は、対象ロットの製品について、特定のアナライザーと併用した場合のみ、当該製品の試薬パックのエラストマーコーティングに試薬ピペッターが完全に穿刺されな
い可能性があると判断した。当該事象により、装置で検出されない閉塞が発生し、正しい試薬量が分注されない可能性や、検査結果が誤って低値になる可能性がある。
当該事象の原因は、対象ロットの試薬パックの製造に使用されたエラストマーについて、試薬ピペッター穿刺部位にあるスリットに完全に切れ込みが入っていなかったこと 欧州連合、
である。製造元は、使用施設に対して、当該アナライザーにおける対象ロットの試薬の使用を中止すること、過去の測定結果のレビューの必要性について検討すること、 イギリス
代替品への交換について企業担当者に連絡することを通知する。さらに、製造元は当該アナライザを使用している顧客に、対象ロットの出荷を停止するとともに、影響を受
けるエラストマーコーティングを使用した当該試薬の製造を中止した。
情報提供
対応不要
海外製造元は、生化学自動分析装置において試薬キャリーオーバーが発生し、当該製品がその測定直後に行われる特定の別製品の測定に干渉し、品質管理、患者検
血液検査用総ビリルビンキット
体、キャリブレーターの結果に正の影響を及ぼす可能性があることを確認した。本事象は近日中にリリース予定の分析装置のソフトウェアバージョンで改善する。顧客に
281 血液検査用ガンマ-グルタミル
欧州連合
は、ソフトウェアバージョンが更新されるまでの間、当該製品と特定の別製品を別のシステムで測定するか、当該製品の測定後に特定の試薬プローブクリーナーで洗浄を
トランスぺプチダーゼキット
実施するよう依頼する。
情報提供
対応不要
276
280
葉酸キット
甲状腺刺激ホルモンキット
40
医薬品名(一般名)
措置概要
措置国
クラスⅡ生化学・免疫・内分泌
検査用シリーズ
【第1報】
トロポニンキット
当該製品において技能試験用検体中のトロポニンの回収率が低いという苦情から、トロポニンの結果が低値に偏る可能性があることが確認され、海外製造元は、直ちに使
ミオグロビンキット
275
用を中止し代替手段で対応することが通知した。海外製造元において原因が原材料にあると特定され、再発防止のため工程試験が追加された。
アメリカ
クレアチンキナーゼアイソザイ
【第2報】
ムキット
特定ロットのTnI抗体が使用されたデバイスロットを回収対象とした。
ヒト脳性ナトリウム利尿ペプチ
ド前駆体N端フラグメントキット
措置区分※3
本邦における
措置内容※4
回収
対応不要
核酸同定・ブドウ球菌キット
核酸同定・一般細菌キット
【第1報】
製造元は、一部の顧客が、当該製品について既に技術的な切り替えを完了し、新しいキットの使用を開始したにもかかわらず、古いキットを受け取ったことを確認した。旧
キットと新キットの試薬カートリッジは同じだが、新キットは、変異SCC株によるメチシリン耐性結果の偽陰性の発生を減らすことを目的にアルゴリズム更新を含む新しい試験
定義ファイルを使用している。 メチシリン耐性黄色ブドウ球菌陽性検体から変異SCC株を検出した場合、メチシリン耐性結果が偽陰性になる可能性がある。このような偽陰
性は、抗生物質の変更により疾患が進行する可能性があり、一般集団に対する永続的な危害、および予後を脅かす危害の可能性は低いが、高リスクの集団に対しては、
生命を脅かす危害の恐れがある。 本件の対処として、製造元は使用者に対し在庫確認を依頼し、旧キットの未使用試薬カートリッジの在庫があり、新キットに切り替えた場 フランス
合には、旧キットの試薬カートリッジを交換、あるいは旧キットの使用を中止し、廃棄するよう注意喚起した。製造元は、新バージョンに切り替わった国での旧バージョンの
取り扱いを終了する。
【第2報】
新バージョンのキットを受注したにもかかわらず、誤って旧バージョンのキットを受注入力し、出荷してしまったことが根本原因である。製造元による再発防止策として、新
バージョンの流通を開始した地域には、誤って旧バージョンが出荷できないよう対策した。
情報提供
対応不要
クロストリジウム・ディフィシル
核酸キット
277
核酸同定・一般細菌キット
核酸同定・ウイルスキット
製造元における調査の結果、特定ロットのスワブの疎水性の問題により、まれに偽陰性の結果を示す可能性があることが確認された。特定ロットのスワブを含む製品の全
てのロットを自主回収することになった。 製造元は、スワブの全てのロットを評価した上で、当該ロットのみに問題があることを確認した。 現在、製造元にて原因を調査中で アメリカ
ある。 なお、本件は2022年に実施した措置の再発である。
回収
対応不要
278 トロポニンキット
製造元において、特定ロットで患者検体および精度管理試料を測定した場合に不正確な結果が出力される可能性があることが確認された。そのため、当該製品を使用す
る顧客に当該ロットの使用を中止するよう通知するための顧客案内を実施した。製造元において、特定のアッセイ試薬の製造のために使用されたリガンドウェルが、別の
アッセイ試薬の製造に使用されたことが確認された。別のアッセイ試薬のリガンドウェルが測定に使用された場合、正しいシグナル(発光強度)が得られず、キャリブレーショ
ンが失敗する、精度管理が規格範囲から外れる、あるいは患者検体を測定したときに不正確な結果が出力される可能性がある。製造元では使用期限内の全ての製品の
製造記録を確認し、対象ロットを特定した。他のアッセイ試薬は適切なリガンドウェルを使用して製造されたことを確認している。本事象の原因は、担当者が手順書に記載 アメリカ、
されたラインクリアランスの作業を適切に実施せず、直前に製造したアッセイ試薬のリガンドウェルがセットされたプレートを除去せずに、次の製造を開始してしまったことで カナダ
あることが確認された。また、前製造バッチで使用されたプレートが、次の製造バッチで再架設されたことを検出するシステム管理上の機能が無く、本事象が見逃されたこ
とが確認された。製造元では再発防止策として、製造バッチ毎にプレートIDをシステム上で管理し、チェックできる機能を追加した。これにより誤ったプレートIDが製造に使
用されないようにシステム上で製造開始前にチェックできる。また、製造元ではラインクリアランスに関連する手順書のレビューおよび担当者への教育訓練の実施を予定し
ている。
情報提供
対応不要
血液検査用グルコースキット 海外製造元は当該製品の一部ロットを血液ガス分析装置の特定のソフトウェアバージョンとの組み合わせで使用した場合、報告可能な範囲の下限濃度の検体でグルコー
乳酸キット
ス値が乖離し、高値になることを確認した。海外製造元における予備調査の結果、根本原因はソフトウェアに起因しないが、次のバージョンでは本事象の発生が軽減され
279
欧州連合
血液検査用クレアチニンキット ることが確認されており、ソフトウェアバージョンのアップデート後は、該当ロットを通常通り使用することが可能である。海外製造元では、血液ガス分析装置のソフトウェア
血液検査用尿素窒素キット
アップデートを顧客に依頼する。
情報提供
対応不要
製造元は、対象ロットの製品について、特定のアナライザーと併用した場合のみ、当該製品の試薬パックのエラストマーコーティングに試薬ピペッターが完全に穿刺されな
い可能性があると判断した。当該事象により、装置で検出されない閉塞が発生し、正しい試薬量が分注されない可能性や、検査結果が誤って低値になる可能性がある。
当該事象の原因は、対象ロットの試薬パックの製造に使用されたエラストマーについて、試薬ピペッター穿刺部位にあるスリットに完全に切れ込みが入っていなかったこと 欧州連合、
である。製造元は、使用施設に対して、当該アナライザーにおける対象ロットの試薬の使用を中止すること、過去の測定結果のレビューの必要性について検討すること、 イギリス
代替品への交換について企業担当者に連絡することを通知する。さらに、製造元は当該アナライザを使用している顧客に、対象ロットの出荷を停止するとともに、影響を受
けるエラストマーコーティングを使用した当該試薬の製造を中止した。
情報提供
対応不要
海外製造元は、生化学自動分析装置において試薬キャリーオーバーが発生し、当該製品がその測定直後に行われる特定の別製品の測定に干渉し、品質管理、患者検
血液検査用総ビリルビンキット
体、キャリブレーターの結果に正の影響を及ぼす可能性があることを確認した。本事象は近日中にリリース予定の分析装置のソフトウェアバージョンで改善する。顧客に
281 血液検査用ガンマ-グルタミル
欧州連合
は、ソフトウェアバージョンが更新されるまでの間、当該製品と特定の別製品を別のシステムで測定するか、当該製品の測定後に特定の試薬プローブクリーナーで洗浄を
トランスぺプチダーゼキット
実施するよう依頼する。
情報提供
対応不要
276
280
葉酸キット
甲状腺刺激ホルモンキット
40