よむ、つかう、まなぶ。
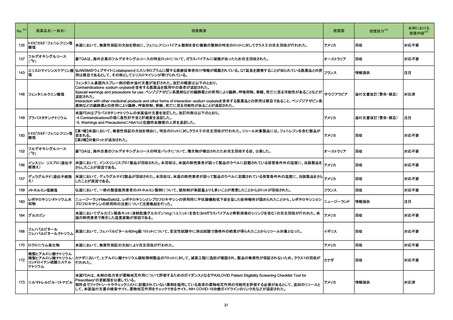
【資料4-1】医薬・生活衛生局からの定期報告 (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_30030.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第10回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
No.
4
5
6
カテゴリー
※2
承認日
③海外承認なし R4.9.26
③海外承認なし R4.9.26
③海外承認なし R4.11.22
販
売
名
(製造販売業者名)
有効成分名
ソーティクツ錠6mg
(ブリストル・マイヤーズスク デュークラバシチニブ
イブ㈱)
エザルミア錠50mg
同
錠100mg
(第一三共㈱)
ゾコーバ錠125mg
(塩野義製薬㈱)
フマ
SARS-CoV-2による感染症を効能・効果とす
る新有効成分含有医薬品
【緊急承認に係る品目】
※1 本表は「「医薬・生活衛生局からの定期報告」の報告対象等について」(令和3年7月19日
新有効成分を含有する医薬品のうち、
①先駆け審査指定制度の対象品目
②条件付き早期承認制度の対象品目
③海外で承認されていない医薬品
④特例承認の対象品目
(海外での承認の有無及び使用実績は、審査報告書の記載により判断しています。)
※2
承認条件
医薬品リスク管理計画(主なもの)
○重要な特定されたリスク
重篤な感染症
○重要な潜在的リスク
悪性腫瘍、心血管系事象、静脈血栓塞栓症、横紋
筋融解症、ミオパチー、B 型肝炎ウイルスの再活
性化
○重要な不足情報
本剤の臨床開発は2015年10月より開始
該当なし
既存治療で効果不十分な尋常性乾癬、膿疱性 され、今般、日本を含む国際共同試験の
医薬品リスク管理計画を策定の上、適切に実施す ○追加の医薬品安全性監視活動
乾癬、乾癬性紅皮症を効能・効果とする新有 成績等に基づき、製造販売承認申請が行
ること。
・市販直後調査
効成分含有医薬品
われた。2022年6月現在、米国及び欧州
・特定使用成績調査
において、審査中である。
・製造販売後データベース調査(重篤な感染症、
悪性腫瘍)
・製造販売後臨床試験(IM011-075 試験)
○追加のリスク最小化活動
・市販直後調査による情報提供
・医療従事者向け資材(適正使用ガイド)の作成
と提供
再発又は難治性の成人T細胞白血病リンパ腫
バレメトスタットトシル
を効能・効果とする新有効成分含有医薬品
酸塩
【希少疾病用医薬品】
エンシトレルビル
ル酸
海外での使用実績
※審査報告書から抜粋
効能・効果等
1. 医薬品リスク管理計画を策定の上、適切に実施
すること。
2. 国内での治験症例が極めて限られていることか
2022年5月時点において、再発又は難治 ら、製造販売後、一定数の症例に係るデータが集
性のATLLに係る効能・効果にて本薬が 積されるまでの間は、全症例を対象に使用成績調
承認されている国又は地域はない。
査を実施することにより、本剤使用患者の背景情
報を把握するとともに、本剤の安全性及び有効性
に関するデータを早期に収集し、本剤の適正使用
に必要な措置を講じること。
○重要な特定されたリスク
骨髄抑制、感染症、CYP3A阻害剤及びP-gp阻害剤
との薬物相互作用
○重要な潜在的リスク
二次性悪性腫瘍、生殖発生毒性
○重要な不足情報
該当なし
○追加の医薬品安全性監視活動
・市販直後調査
・一般使用成績調査
○追加のリスク最小化活動
・市販直後調査による情報提供
・医療従事者向け資材(エザルミア適正使用ガイ
ド)の作成・提供
1. 医薬品リスク管理計画を策定の上、適切に実施
すること。
2. 本剤の投与が適切と判断される症例のみを対象
に、あらかじめ患者又は代諾者に有効性及び安全
2022年5月時点で、本剤はいずれの国又 性に関する情報が文書をもって説明され、文書に
は地域においても承認されていない。 よる同意を得てから初めて投与されるよう、医師
に対して要請すること。
3. 国際共同第Ⅱ/Ⅲ相試験(T1221試験)の第Ⅲ
相パートから適切に有効性が確認された試験成績
を取りまとめ速やかに提出すること。
○重要な特定されたリスク
該当なし
○重要な潜在的リスク
催奇形性
○重要な不足情報
中等度以上の肝機能障害患者での安全性
○有効性に関する検討事項
国際共同第Ⅱ/Ⅲ相試験(T1221試験)の第Ⅲ相
パートでの有効性
○追加の医薬品安全性監視活動
・市販直後調査
・一般使用成績調査
・肝機能障害を有する被験者を対象とした臨床薬
理試験
○追加のリスク最小化活動
・市販直後調査による情報提供
・投与に際しての患者への説明と理解の実施(同
意説明文書・患者ハンドブック)
・医療従事者向け資材(ゾコーバ錠125mg「「妊
娠している女性、妊娠している可能性のある女
性、又は妊娠する可能性のある女性」への投与に
関するお願い」)の作成と提供
医薬品等行政評価・監視委員会決定)に基づき、以下のいずれかに該当するものを抜粋したもの。
「カテゴリー」の語句は以下を指す。
①先駆け:先駆け審査指定制度の対象品目
②条件付き:条件付き早期承認制度の対象品目
③海外承認なし:海外で承認されていない医薬品
④特例承認:特例承認に対象品目
3
4
5
6
カテゴリー
※2
承認日
③海外承認なし R4.9.26
③海外承認なし R4.9.26
③海外承認なし R4.11.22
販
売
名
(製造販売業者名)
有効成分名
ソーティクツ錠6mg
(ブリストル・マイヤーズスク デュークラバシチニブ
イブ㈱)
エザルミア錠50mg
同
錠100mg
(第一三共㈱)
ゾコーバ錠125mg
(塩野義製薬㈱)
フマ
SARS-CoV-2による感染症を効能・効果とす
る新有効成分含有医薬品
【緊急承認に係る品目】
※1 本表は「「医薬・生活衛生局からの定期報告」の報告対象等について」(令和3年7月19日
新有効成分を含有する医薬品のうち、
①先駆け審査指定制度の対象品目
②条件付き早期承認制度の対象品目
③海外で承認されていない医薬品
④特例承認の対象品目
(海外での承認の有無及び使用実績は、審査報告書の記載により判断しています。)
※2
承認条件
医薬品リスク管理計画(主なもの)
○重要な特定されたリスク
重篤な感染症
○重要な潜在的リスク
悪性腫瘍、心血管系事象、静脈血栓塞栓症、横紋
筋融解症、ミオパチー、B 型肝炎ウイルスの再活
性化
○重要な不足情報
本剤の臨床開発は2015年10月より開始
該当なし
既存治療で効果不十分な尋常性乾癬、膿疱性 され、今般、日本を含む国際共同試験の
医薬品リスク管理計画を策定の上、適切に実施す ○追加の医薬品安全性監視活動
乾癬、乾癬性紅皮症を効能・効果とする新有 成績等に基づき、製造販売承認申請が行
ること。
・市販直後調査
効成分含有医薬品
われた。2022年6月現在、米国及び欧州
・特定使用成績調査
において、審査中である。
・製造販売後データベース調査(重篤な感染症、
悪性腫瘍)
・製造販売後臨床試験(IM011-075 試験)
○追加のリスク最小化活動
・市販直後調査による情報提供
・医療従事者向け資材(適正使用ガイド)の作成
と提供
再発又は難治性の成人T細胞白血病リンパ腫
バレメトスタットトシル
を効能・効果とする新有効成分含有医薬品
酸塩
【希少疾病用医薬品】
エンシトレルビル
ル酸
海外での使用実績
※審査報告書から抜粋
効能・効果等
1. 医薬品リスク管理計画を策定の上、適切に実施
すること。
2. 国内での治験症例が極めて限られていることか
2022年5月時点において、再発又は難治 ら、製造販売後、一定数の症例に係るデータが集
性のATLLに係る効能・効果にて本薬が 積されるまでの間は、全症例を対象に使用成績調
承認されている国又は地域はない。
査を実施することにより、本剤使用患者の背景情
報を把握するとともに、本剤の安全性及び有効性
に関するデータを早期に収集し、本剤の適正使用
に必要な措置を講じること。
○重要な特定されたリスク
骨髄抑制、感染症、CYP3A阻害剤及びP-gp阻害剤
との薬物相互作用
○重要な潜在的リスク
二次性悪性腫瘍、生殖発生毒性
○重要な不足情報
該当なし
○追加の医薬品安全性監視活動
・市販直後調査
・一般使用成績調査
○追加のリスク最小化活動
・市販直後調査による情報提供
・医療従事者向け資材(エザルミア適正使用ガイ
ド)の作成・提供
1. 医薬品リスク管理計画を策定の上、適切に実施
すること。
2. 本剤の投与が適切と判断される症例のみを対象
に、あらかじめ患者又は代諾者に有効性及び安全
2022年5月時点で、本剤はいずれの国又 性に関する情報が文書をもって説明され、文書に
は地域においても承認されていない。 よる同意を得てから初めて投与されるよう、医師
に対して要請すること。
3. 国際共同第Ⅱ/Ⅲ相試験(T1221試験)の第Ⅲ
相パートから適切に有効性が確認された試験成績
を取りまとめ速やかに提出すること。
○重要な特定されたリスク
該当なし
○重要な潜在的リスク
催奇形性
○重要な不足情報
中等度以上の肝機能障害患者での安全性
○有効性に関する検討事項
国際共同第Ⅱ/Ⅲ相試験(T1221試験)の第Ⅲ相
パートでの有効性
○追加の医薬品安全性監視活動
・市販直後調査
・一般使用成績調査
・肝機能障害を有する被験者を対象とした臨床薬
理試験
○追加のリスク最小化活動
・市販直後調査による情報提供
・投与に際しての患者への説明と理解の実施(同
意説明文書・患者ハンドブック)
・医療従事者向け資材(ゾコーバ錠125mg「「妊
娠している女性、妊娠している可能性のある女
性、又は妊娠する可能性のある女性」への投与に
関するお願い」)の作成と提供
医薬品等行政評価・監視委員会決定)に基づき、以下のいずれかに該当するものを抜粋したもの。
「カテゴリー」の語句は以下を指す。
①先駆け:先駆け審査指定制度の対象品目
②条件付き:条件付き早期承認制度の対象品目
③海外承認なし:海外で承認されていない医薬品
④特例承認:特例承認に対象品目
3