よむ、つかう、まなぶ。
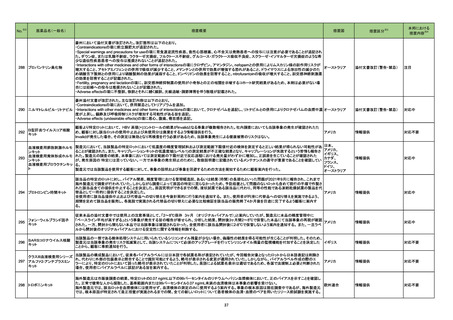
【資料4-1】医薬・生活衛生局からの定期報告 (32 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_30030.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第10回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
※2
No.
医薬品名(一般名)
措置概要
※3
措置国
米国FDAのEnforcementReportにおいて、GMPから逸脱した温度異常がみられた製造管理状態で製造されたSandoz Pharma社製のニトログリセリン製剤、
アメリカ
2ロットの回収を実施していることを公表したもの。
174
ニトログリセリン
アプレピタント
183
精製ヒアルロン酸ナトリウム
精製ヒアルロン酸ナトリウム・ ドイツにおいて、ヒアルロン酸ナトリウム眼粘弾剤製品全ロットに対して、滅菌工程に逸脱が確認され、製品の無菌性が保証されないため、期限切れでない製
コンドロイチン硫酸エステル 品を対象として回収が行われた。
ナトリウム
187
措置区分
本邦における
措置内容※4
回収
対応不要
ドイツ
回収
対応不要
精製ヒアルロン酸ナトリウム
精製ヒアルロン酸ナトリウム・ ドイツにおいて、ヒアルロン酸ナトリウム眼粘弾剤製品が滅菌工程に逸脱が確認され、製品の無菌性が保証されないため、期限切れでない製品全ロットを対象
ドイツ
コンドロイチン硫酸エステル として回収が行われた。
ナトリウム
回収
対応不要
情報提供
対応済
サルブタモール硫酸塩
アモキシシリン水和物・クラブ
米国FDAは、アルブテロール硫酸塩製剤、アモキシシリン製剤、ムピロシン製剤、スマトリプタン製剤についてcGMPから逸脱する温度不正を理由とする回収が
ラン酸カリウム
198
アメリカ
ムピロシンカルシウム水和物 進行中であるとの内容をEnforcement Reportに掲載した。
スマトリプタンコハク酸塩
スマトリプタン
回収
対応不要
ブルネイ・ダルサラーム国で登録、販売されているすべてのカンフル含有製品に、小児への使用に関する警告及び使用上の注意を記載することを義務付ける
指示を発表した。これは、医師の管理や助言なしに市販されているこれらの製品を使用することで、公共の安全性が懸念されるためである。
以下の情報を含める必要がある。
dl-カンフル含有一般用医薬
205
①本製品は2歳以下の小児には禁忌である。
ブルネイ
品
②年長の小児には注意して使用してください。
③本製品は痙攣を引き起こす可能性があります。
④カンフルを含む製品を小児の鼻の穴に入れるのは危険です。少量の使用でもすぐに虚脱する可能性があります。
添付文書改訂(警告・禁忌)
注目
情報提供
対応中
情報提供
対応不要
193 メトホルミン塩酸塩
英国MHRAはメトホルミンによるビタミンB12欠乏症に関して、以下の内容を公表した。
・ビタミンB12欠乏症はメトホルミンを服用する10人に1人に影響を与える可能性がある一般的な副作用であること。
・ビタミンB12欠乏症の発現はメトホルミンの投与量、治療期間の長さに応じて増加すること。
・リスク因子保有患者(貧血、神経障害を合併する患者)に対して投与する際には定期的な血液検査の検討が必要であること。
イギリス
206 デクスメデトミジン塩酸塩
【第1報】
独BfArMのHPにDirect healthcare professional communication(DHPC)が掲載された。概要は以下のとおり。
・SPICE III試験は、集中治療室の重症成人患者3,904名を対象に全死因死亡率に対してデクスメデトミジンによる鎮静の影響を標準治療の影響と比較した無
作為化臨床試験であり、65歳以下の年齢層で他の鎮静剤より死亡リスクが高かった(オッズ比1.26; 95 %信頼区間1.02~1.56)が、機序は不明である。
・65歳以下の患者の死亡率に対する影響の不均一性が最も顕著に現れたのは、術後ケア以外の理由で入院した患者の深鎮静でデクスメデトミジンを早期に
高用量で投与したケースであった。この不均一性は、APACHE II スコアの上昇に伴い増加した。
・若年患者において、他の鎮静剤とデクスメデトミジンに期待される臨床的有用性とを比較検討すべきである。
・警告が追加され、65歳以下の集中治療患者の死亡リスクの増加が追記された。
【第2報】
英MHRAのHPにもDHPCが掲載された。
207 セトロレリクス酢酸塩
欧州でセトロタイドの一時的供給不足に関するDHPCが発出された。主な内容は以下のとおり。
・主要な医薬品製造拠点における技術的な問題により、2021年12月~2022年3月末までの間、工場が閉鎖され、セトロタイドの供給が遅延したが、技術的な
問題を解決し2022年4月上旬に生産を再開した。
・出荷された医薬品の品質には影響がない。
ドイツ
・代替品はセトロタイドの代替パックサイズがある場合や、GnRH拮抗薬、GnRHアンタゴニスト等
・GnRH アゴニストなどの代替療法はOHSS のリスクを伴う。また卵巣周期がコントロールされている状態で代替療法を行わない場合卵巣刺激サイクルが失敗
するリスクがある。 リスク最小化対策として、治療を完了するのに十分な在庫が確認できない限りセトロタイドの投与を開始しないこと、又は市販されている代
替治療薬の使用を推奨する。
32
ドイツ、
フランス、
オランダ、
イギリス
No.
医薬品名(一般名)
措置概要
※3
措置国
米国FDAのEnforcementReportにおいて、GMPから逸脱した温度異常がみられた製造管理状態で製造されたSandoz Pharma社製のニトログリセリン製剤、
アメリカ
2ロットの回収を実施していることを公表したもの。
174
ニトログリセリン
アプレピタント
183
精製ヒアルロン酸ナトリウム
精製ヒアルロン酸ナトリウム・ ドイツにおいて、ヒアルロン酸ナトリウム眼粘弾剤製品全ロットに対して、滅菌工程に逸脱が確認され、製品の無菌性が保証されないため、期限切れでない製
コンドロイチン硫酸エステル 品を対象として回収が行われた。
ナトリウム
187
措置区分
本邦における
措置内容※4
回収
対応不要
ドイツ
回収
対応不要
精製ヒアルロン酸ナトリウム
精製ヒアルロン酸ナトリウム・ ドイツにおいて、ヒアルロン酸ナトリウム眼粘弾剤製品が滅菌工程に逸脱が確認され、製品の無菌性が保証されないため、期限切れでない製品全ロットを対象
ドイツ
コンドロイチン硫酸エステル として回収が行われた。
ナトリウム
回収
対応不要
情報提供
対応済
サルブタモール硫酸塩
アモキシシリン水和物・クラブ
米国FDAは、アルブテロール硫酸塩製剤、アモキシシリン製剤、ムピロシン製剤、スマトリプタン製剤についてcGMPから逸脱する温度不正を理由とする回収が
ラン酸カリウム
198
アメリカ
ムピロシンカルシウム水和物 進行中であるとの内容をEnforcement Reportに掲載した。
スマトリプタンコハク酸塩
スマトリプタン
回収
対応不要
ブルネイ・ダルサラーム国で登録、販売されているすべてのカンフル含有製品に、小児への使用に関する警告及び使用上の注意を記載することを義務付ける
指示を発表した。これは、医師の管理や助言なしに市販されているこれらの製品を使用することで、公共の安全性が懸念されるためである。
以下の情報を含める必要がある。
dl-カンフル含有一般用医薬
205
①本製品は2歳以下の小児には禁忌である。
ブルネイ
品
②年長の小児には注意して使用してください。
③本製品は痙攣を引き起こす可能性があります。
④カンフルを含む製品を小児の鼻の穴に入れるのは危険です。少量の使用でもすぐに虚脱する可能性があります。
添付文書改訂(警告・禁忌)
注目
情報提供
対応中
情報提供
対応不要
193 メトホルミン塩酸塩
英国MHRAはメトホルミンによるビタミンB12欠乏症に関して、以下の内容を公表した。
・ビタミンB12欠乏症はメトホルミンを服用する10人に1人に影響を与える可能性がある一般的な副作用であること。
・ビタミンB12欠乏症の発現はメトホルミンの投与量、治療期間の長さに応じて増加すること。
・リスク因子保有患者(貧血、神経障害を合併する患者)に対して投与する際には定期的な血液検査の検討が必要であること。
イギリス
206 デクスメデトミジン塩酸塩
【第1報】
独BfArMのHPにDirect healthcare professional communication(DHPC)が掲載された。概要は以下のとおり。
・SPICE III試験は、集中治療室の重症成人患者3,904名を対象に全死因死亡率に対してデクスメデトミジンによる鎮静の影響を標準治療の影響と比較した無
作為化臨床試験であり、65歳以下の年齢層で他の鎮静剤より死亡リスクが高かった(オッズ比1.26; 95 %信頼区間1.02~1.56)が、機序は不明である。
・65歳以下の患者の死亡率に対する影響の不均一性が最も顕著に現れたのは、術後ケア以外の理由で入院した患者の深鎮静でデクスメデトミジンを早期に
高用量で投与したケースであった。この不均一性は、APACHE II スコアの上昇に伴い増加した。
・若年患者において、他の鎮静剤とデクスメデトミジンに期待される臨床的有用性とを比較検討すべきである。
・警告が追加され、65歳以下の集中治療患者の死亡リスクの増加が追記された。
【第2報】
英MHRAのHPにもDHPCが掲載された。
207 セトロレリクス酢酸塩
欧州でセトロタイドの一時的供給不足に関するDHPCが発出された。主な内容は以下のとおり。
・主要な医薬品製造拠点における技術的な問題により、2021年12月~2022年3月末までの間、工場が閉鎖され、セトロタイドの供給が遅延したが、技術的な
問題を解決し2022年4月上旬に生産を再開した。
・出荷された医薬品の品質には影響がない。
ドイツ
・代替品はセトロタイドの代替パックサイズがある場合や、GnRH拮抗薬、GnRHアンタゴニスト等
・GnRH アゴニストなどの代替療法はOHSS のリスクを伴う。また卵巣周期がコントロールされている状態で代替療法を行わない場合卵巣刺激サイクルが失敗
するリスクがある。 リスク最小化対策として、治療を完了するのに十分な在庫が確認できない限りセトロタイドの投与を開始しないこと、又は市販されている代
替治療薬の使用を推奨する。
32
ドイツ、
フランス、
オランダ、
イギリス