【資料2】新型コロナウイルス感染症治療薬(ゾコーバ錠125mg)について(医薬・生活衛生局からの説明資料) (21 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32109.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第11回 3/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
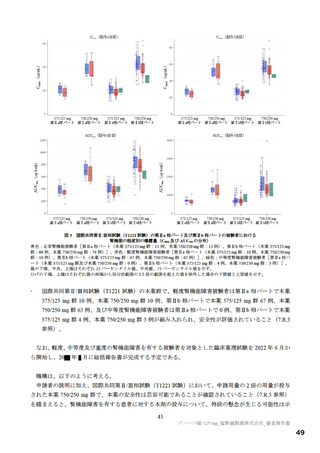
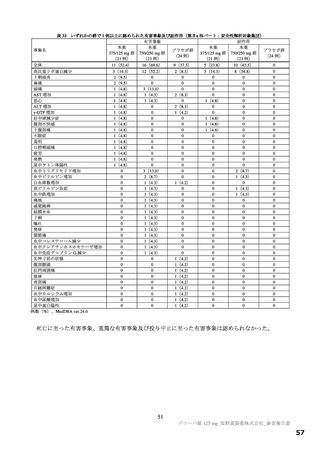
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)第Ⅱa 相パートにおける本薬群の被験者(34 例)19)の検体(本
薬投与前後)を用いて SARS-CoV-2 3CL プロテアーゼのアミノ酸配列を解析20)したところ、10 例で本
薬投与後にアミノ酸変異が認められた(表 11)。アミノ酸変異が認められた時点以降において、いずれ
の症例もウイルス力価及びウイルス RNA 量の再上昇は認められず、その後に塩基配列の解析が可能な
RNA 量が得られた 2 症例(症例 7 及び 9)で、当該アミノ酸変異は認められなかった。なお、当該アミ
ノ酸変異は、SARS-CoV-2 3CL プロテアーゼの活性中心部位及び本薬の結合部位(3.R.1、表 10)の変異
ではなく、in vitro 耐性発現試験で認められたアミノ酸変異とは異なる変異であった(3.1.3.1 参照)。第
Ⅱb 相パートにおいても、同様の解析を行う計画としているが、現時点で解析は未着手であり、結果が
得られる時期は未定である。
表 11
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)第Ⅱa 相パートで本薬投与後に認められた
SARS-CoV-2 3CL プロテアーゼのアミノ酸変異
症例
投与群
アミノ酸変異 a)
1
750/250 mg
A234S
2
375/125 mg
L87F
3
375/125 mg
H246Y
4
750/250 mg
T198I
5
375/125 mg
A94A/V
6
750/250 mg
L272L/P
7
750/250 mg
T45T/S
8
750/250 mg
M130M/V
K100K/Stop
9
750/250 mg
M130M/I
10
375/125 mg
D263D/E
Stop:終止コドン
a)症例 5~10 は未変異株及びアミノ酸変異株が混在
機構は、以下のように考える。
in vitro での検討において、本薬存在下で、SARS-CoV-2 3CL プロテアーゼにアミノ酸変異(D48G、
M49L、P52S、S144A 及び M49L/S144A)が認められ、これらのアミノ酸変異を有する場合、本薬に対す
る感受性が低下することを確認した。国際共同第Ⅱ/Ⅲ相試験(T1221 試験)第Ⅱa 相パートにおいてア
ミノ酸変異が認められた症例で、ウイルス力価及びウイルス RNA 量の再上昇は認められていないが、
アミノ酸変異と本薬の有効性との関連も含め、臨床試験における本薬に対する耐性変異に関する情報は
極めて限られており、in vitro において本薬に対する感受性が低下した変異株が認められていることを踏
まえると、本薬を臨床使用した場合に、耐性変異株が出現し、本薬の有効性に影響を及ぼす可能性は否
定できない。したがって、国際共同第Ⅱ/Ⅲ相試験(T1221 試験)第Ⅱb 相パートの解析結果が得られ次
第、速やかに評価し、新たな知見が得られた場合には適切に対応する必要がある。加えて、耐性変異の
発現の有無は本薬の有効性に関する重要な情報であることから、公表文献等も含めて引き続き収集し、
新たな知見が得られた場合には、適切に対応する必要がある。
3.R.3
アデノシン取込み阻害活性について
申請者は、副次的薬理試験で認められたアデノシンの取込み阻害活性について、以下のように説明し
ている。
無作為化され、治験薬初回投与開始前に得られた鼻咽頭ぬぐい検体で RT-PCR が陽性の被験者(ITT 集団)の 30 例及び RT-PCR 陽性
とは判断されなかったが塩基配列の解析に必要な RNA 量が存在した一部の被験者 4 例
20)
ベースライン、Day 6 及び Day 9 はすべての検体、Day 14 及び Day 21 は定性 PCR にて陽性であった検体が用いられた。
19)
15
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書
21