【資料2】新型コロナウイルス感染症治療薬(ゾコーバ錠125mg)について(医薬・生活衛生局からの説明資料) (98 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32109.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第11回 3/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
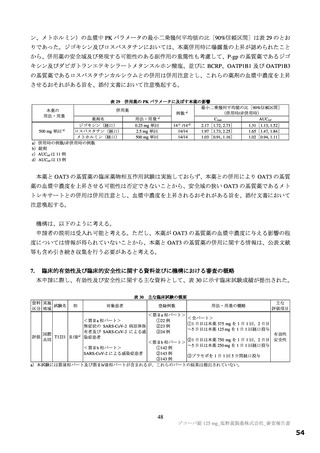
重篤な有害事象は、本薬 375/125 mg 群で 1 例(重度月経出血)に認められ、治験薬との因果関係は否
定され、転帰は回復であった。
投与中止に至った有害事象は、本薬 375/125 mg 群で 3 例(湿疹、嘔吐及び発疹各 1 例)、本薬 750/250 mg
群で 5 例[発疹、悪心、頭痛、腹痛、失神寸前の状態及び嘔吐各 1 例(重複あり)]及びプラセボ群 1 例
(頭痛)に認められ、本薬 375/125 mg 群 2 例(湿疹及び嘔吐各 1 例)及び本薬 750/250 mg 群 1 例(発疹)
は治験薬との因果関係はありとされ、転帰は回復であった。
4.R 機構における審査の概略
4.R.1 国際共同第Ⅱ/Ⅲ相試験(T1221 試験)の試験計画について
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)の第Ⅲ相パートにおいて、開鍵直前に盲検下で主要評価項目及び
有効性の主要な解析対象集団等の変更(4.1.1、表 5 参照)が行われており、申請者はその理由を以下のよ
うに説明している。
第Ⅲ相パートの症例集積時期に流行していたウイルス株の特性を踏まえ、医学専門家等との協議を行
い、以下の検討を行った上で、有効性の主要評価項目及び主要な解析対象集団を変更した上で有効性を検
討することが適切との結論に至った。
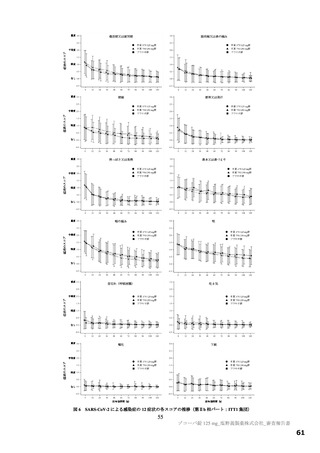
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)の第Ⅱb 相パート及び第Ⅲ相パートは、SARS-CoV-2 の omicron
株流行時期に実施しており、ベースライン時における症状スコアが「なし又は通常どおり」の被験者
の割合が少ない上位 5 つの症状(図 2、赤枠内)は、同時期の国内の入院患者での情報7)において、
身体所見で比較的多く認められた症状(呼吸器症状、発熱、全身倦怠感)と重複していたため、これ
ら 5 つの症状の快復までの時間を評価することには臨床的意義があると考えた。
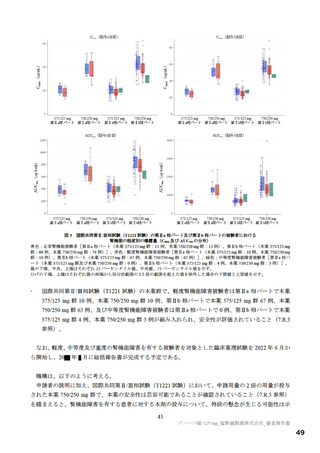
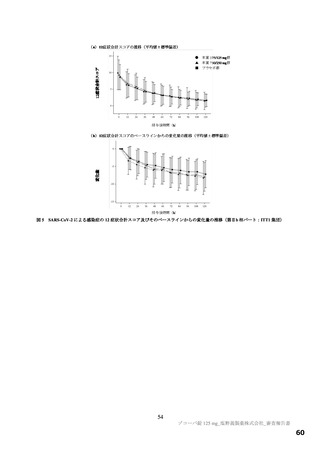
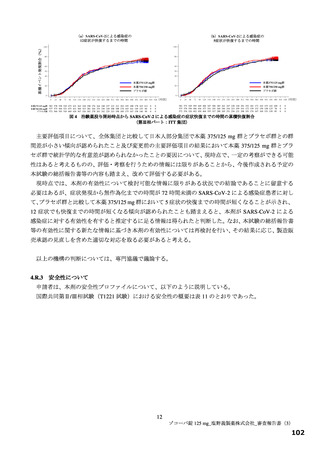
図 2 国際共同第Ⅱ/Ⅲ相試験(T1221 試験)の第Ⅱb パート a)及び第Ⅲ相パート b)のベースライン時における症状スコア
a)ITT1 集団(無作為化され、ベースラインの鼻咽頭ぬぐい検体において SARS-CoV-2 のウイルス力価が検出された被験者)
のうち、ベースライン時の症状スコアが記録された被験者 333 例(本薬 375/125 mg 群 110 例、本薬 750/250 mg 群 113 例
及びプラセボ群 110 例)
b)無作為化され、ベースライン時の症状スコアが記録された被験者 1768 例(2022 年 8 月 15 日時点のカットオフデータ、
開鍵前であったため投与群別の内訳不明)
第 94 回新型コロナウイルス感染症対策アドバイザリーボード(令和 4 年 8 月 10 日)広島県提出資料 広島県新型コロナウイルス感染
症版 J-SPEED データ等からの知見:https://www.mhlw.go.jp/content/10900000/000975398.pdf(最終確認日:2022 年 10 月 25 日)
7)
8
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書(3)
98