【資料2】新型コロナウイルス感染症治療薬(ゾコーバ錠125mg)について(医薬・生活衛生局からの説明資料) (73 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32109.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第11回 3/23)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
審査報告 () に対する、申請者の意見を以下に示す。
「7.R.2 有効性について」 関係
申請者は、本剤の有効性について、 「7.R.2 有効性について」の記載に加え、以下のとおり考える。
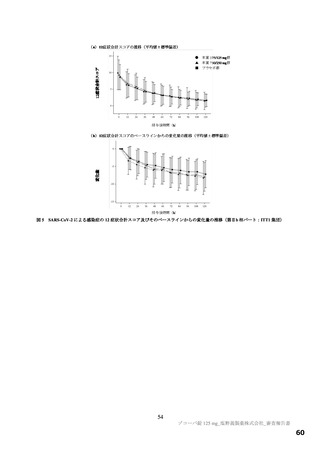
まず、SARS-CoV-2 による感染症の 12 症状合計スコアの変化量について有意差が認められなかった原
因として、 実施時期の流行株の影響を受けたことが考えられる。delta 株による感染が主流であった時期
に実施した第Ta 相パートの結果を基に本評価項目を設定したものの、第Tb 相パートを実施した期間
は omicron 株による感染が主流であった。
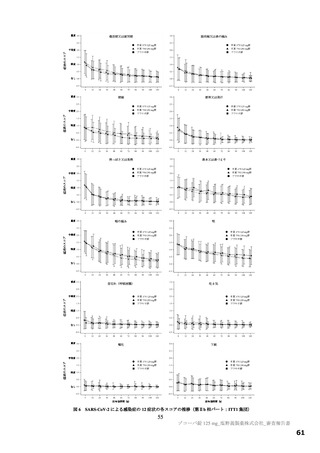
また、SARS-CoV-2 による感染症の 12 症状のうち、ベースラインのスコアの平均値が 1 (軽度) 以上
であったのは、 鼻水又は鼻づまり、 只の痛み、咳、 封っぽさ又は発熱であり、これらの症状は omicran 株
に特徴的な症状と一致していた%) 。
一方で、その他の全身症状及び消化器症状においては、ベースラインの各症状のスコアの平均値が 1
(軽度) 未満であり、症状がほとんど認められない又はその程度は軽かったため、了攻床症状の変化を感
度良く適切に捉えることは難しいと考えられた。 したがって、事前に規定 していた SARS-CoV-2 による
感染症の 12 症状では、 これらの症状も含めた評価であったことから、本剤による了臨床症状の改善効果を
捉えることが難しく、統計学的な有意差を確認することができなかったと考える。
また、SARS-CoV-2 による感染症に対する治療楽の開発においては、顔繁なウイルス変異による流行
株の遷移、及びワクチン接種による集団免疫の獲得状況など、了臨床試験の評価対象となる集団や医療提
供体制・公衆衛生体制が変わりゆく中で、抗ウイルス薬としての有効性を確認・検証していくことが求
められている。 そのため、事前に規定した項目で評価して、プラセボに対する優越性を示すこと以上に、
ウイルス学的に意義のある抗ウイルス効果を臨床試験実施中の流行株で確認することに加え、臨床症状
改善効果を流行株の特徴にあわせて評価することが重要であると考えた。 特に、 omicron 株の特徴は従来
株と大きく異なり、徒来株と同様の評価項目を使用することは困難である。
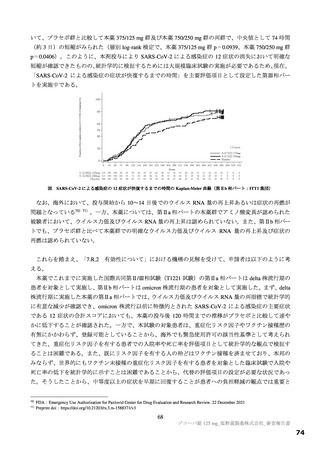
海外規制当局のガイダンスでは、 症状消失までの時間を評価することが推奨されておぉおり 、半証言較
還還間間昌間昌た-。 そこで、評価す
る 12 症状WW の全てのスコアが発症前の状態に戻る又は消失するまでの時間@ を表す「SARS-CoV-2 に
よる感染症の症状が快復するまでの時間」を定義し、第Hb 相パートの結果でさらなる事後解析を実施
した。 第Tb 相パートの ITT1 集団における SARS-CoV-2 による感染症の症状が快復するまでの時間につ
%⑳ 国立感症研究所 : SARS-CoV-2 B.1.1.529 系続 (オミタロン株) 感染による新型コロナウイルス感染症の積極的疫学調査 (第$報) :
疫学的・臨床的特徴 (令和 4 年 2 月 18 日) : https-//www.mitd_go.jp/ntdTa/2019-nmcov/2484_idsc/10969-covid19-72.html
7 下DA : COVTD-19- Developings Drugs and Biological Prodncts for Treatment or Prevention. Guidance for Industry. February 2021
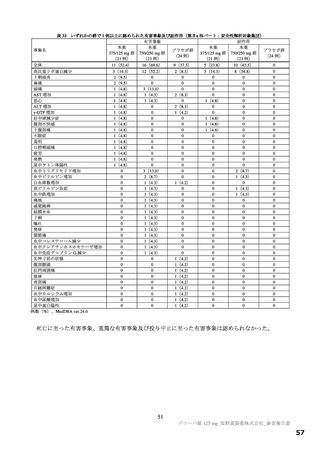
%⑳ SARS_CoV-2 による感染症の 12 症状 (①供意感又は疲労感、 ②筋肉痛又は体の痛み、 ③頭痛、 ①悪寒又は発汗、 ⑤熱っぽさ又は発熱、
⑥鼻水又は鼻づまり、⑦喉の痛み、⑧咳、⑨息切れ (呼吸困難) 、⑩吐き気、⑪嘱吐、⑫下痢) の各症状を4 段階 (0 : なし、1: 軽
度、2 : 中等度、3 : 重度) で被験者が評価
⑳⑲) COVID-19 症状の快復は、治験薬投与開始時点から COVTD_19 の 12 症状全てが下記の通 り に消失、改善又は維持した時点を指し、そ
の状態が少なく とも 224時間持続しているとき、当該被験者は本評価項目を達成したとする。
COVTD_19 発症前から存在 した既存症状で、 ベースライン (投与前検査) 時点で悪化していると披験者が判断した症状について
は、ベベースライン時点の重症度を改善又は維持する必要ががある。
COVID-19 発症前から存在 した既存症状で、ベースライン (投与前検査) 時点で悪化していないと被験者が判断した症状につい
ては、ベベースライン時点の重症度を維持又は改善する必要がある。
上記以外の症状、すなわち COVTD-19 発症前には存在しておらず, ベースライン (投与前検査) 時点あるいはそれ以降に発現し
た症状については、症状が無しになる必要がある。
67
ゾコーバ錠 125 mg 塩野義製薬株式会社 審査報告書
73