会議資料 (110 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00034.html |
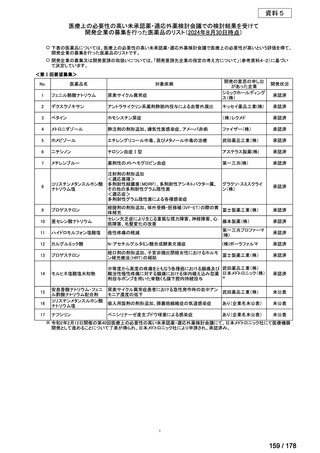
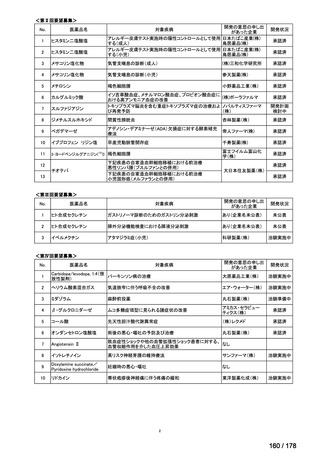
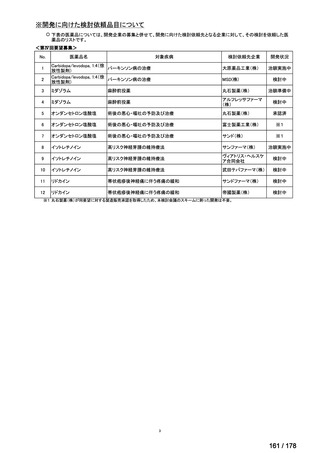
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第60回 9/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
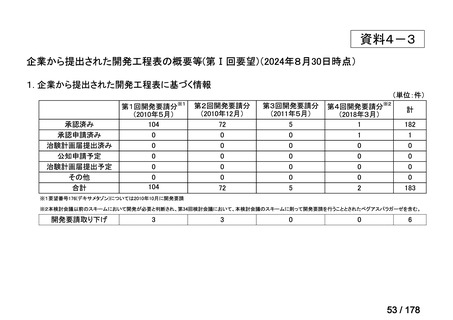
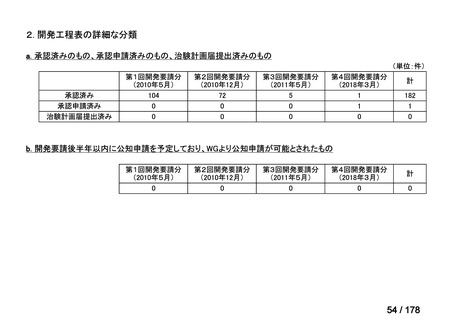
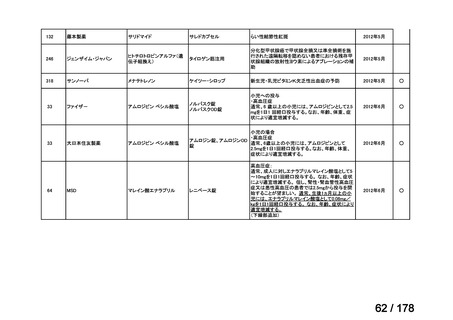
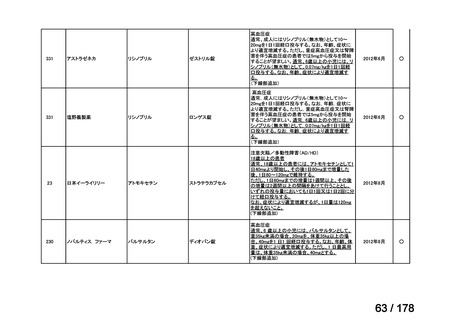
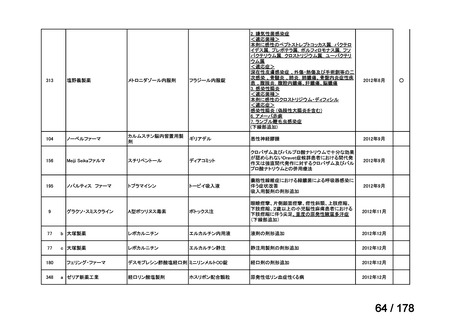
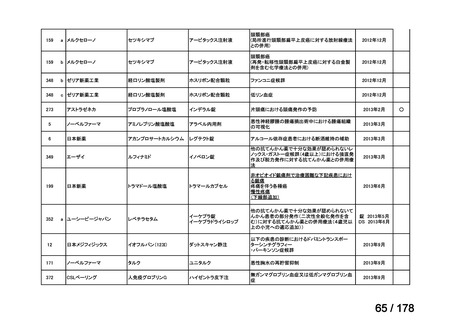
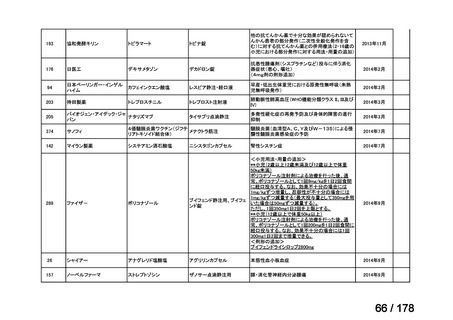
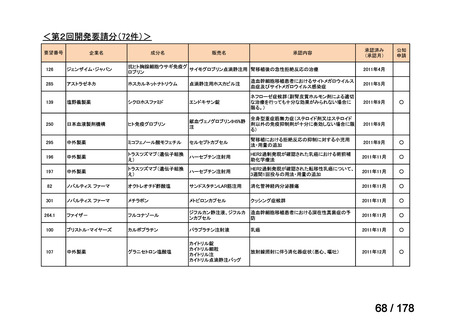
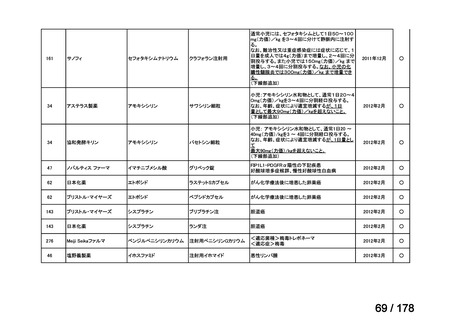
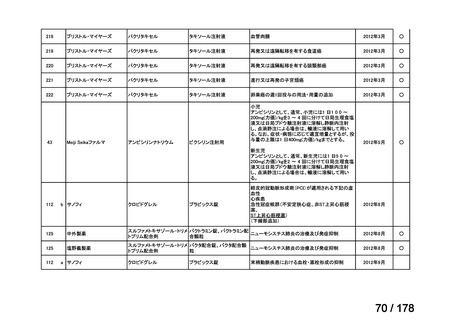
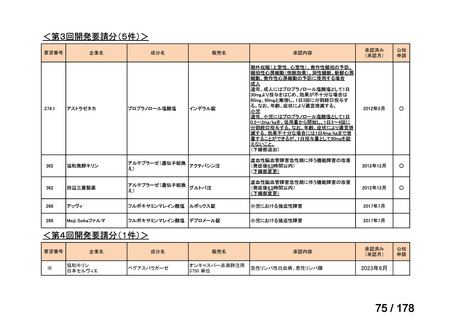
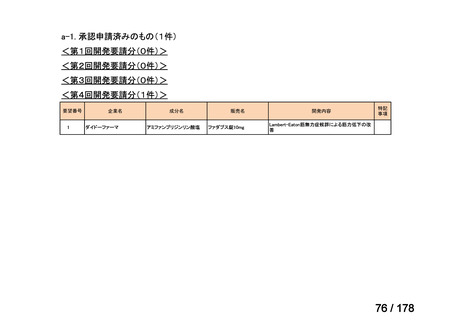
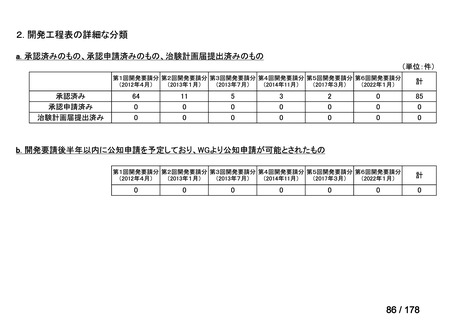
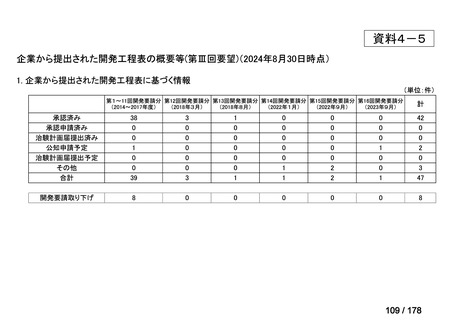
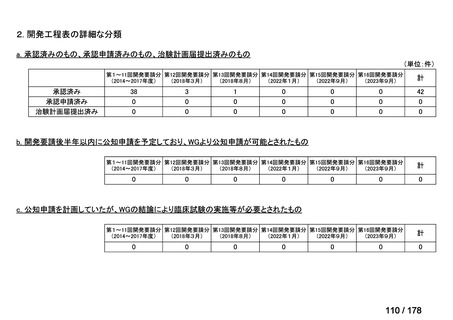
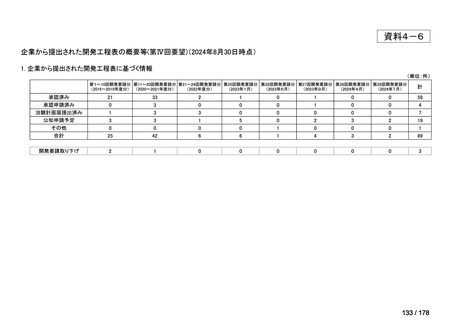
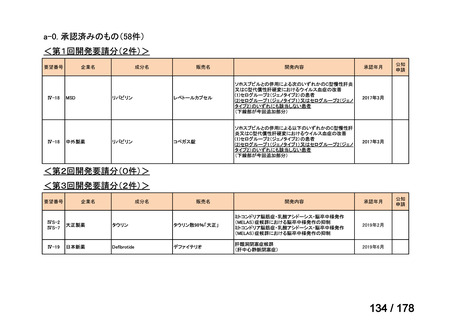
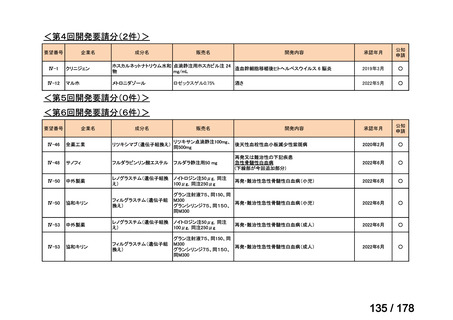
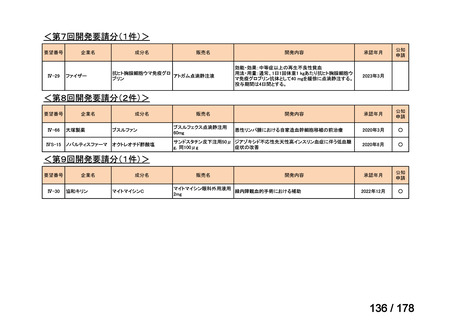
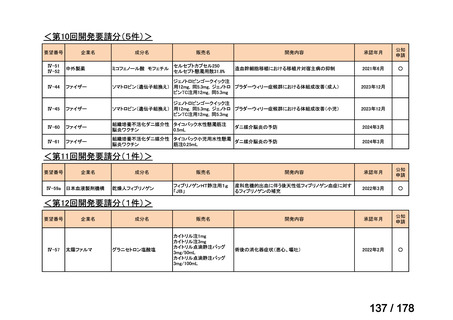
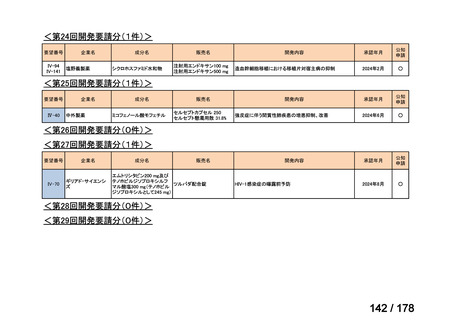
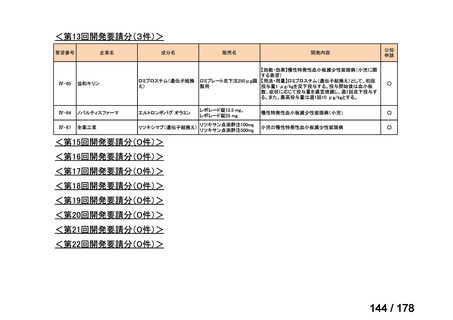
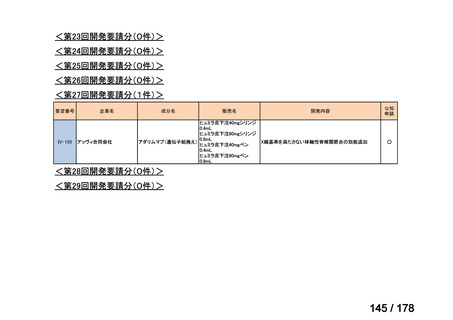
a. 承認済みのもの、承認申請済みのもの、治験計画届提出済みのもの
(単位:件)
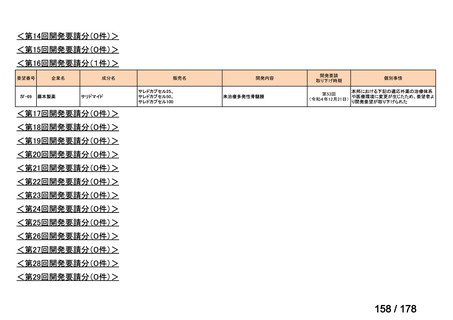
第1~11回開発要請分 第12回開発要請分 第13回開発要請分 第14回開発要請分 第15回開発要請分 第16回開発要請分
(2014~2017年度)
(2018年3月)
(2018年8月)
(2022年1月)
(2022年9月)
(2023年9月)
承認済み
承認申請済み
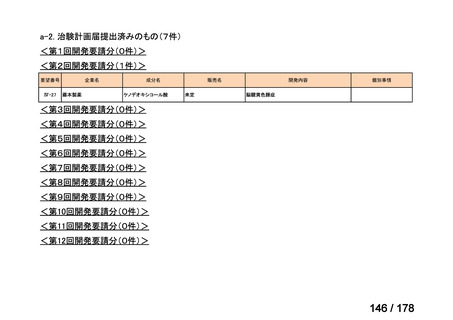
治験計画届提出済み
38
0
0
3
0
0
1
0
0
0
0
0
0
0
0
0
0
0
計
42
0
0
b. 開発要請後半年以内に公知申請を予定しており、WGより公知申請が可能とされたもの
第1~11回開発要請分 第12回開発要請分 第13回開発要請分 第14回開発要請分 第15回開発要請分 第16回開発要請分
(2014~2017年度)
(2018年3月)
(2018年8月)
(2022年1月)
(2022年9月)
(2023年9月)
0
0
0
0
0
0
計
0
c. 公知申請を計画していたが、WGの結論により臨床試験の実施等が必要とされたもの
第1~11回開発要請分 第12回開発要請分 第13回開発要請分 第14回開発要請分 第15回開発要請分 第16回開発要請分
(2014~2017年度)
(2018年3月)
(2018年8月)
(2022年1月)
(2022年9月)
(2023年9月)
0
0
0
0
0
0
計
0
110 / 178