会議資料 (113 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00034.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第60回 9/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
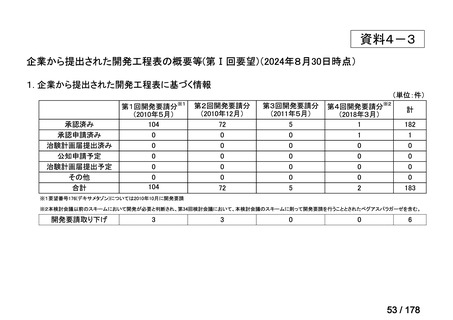
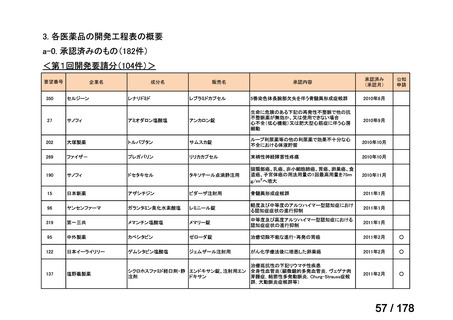
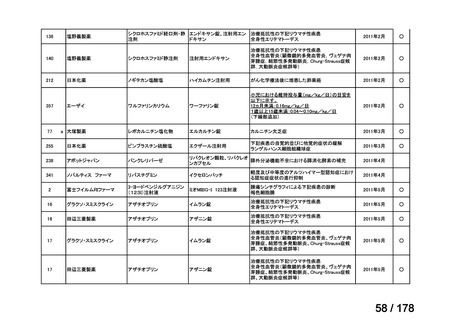
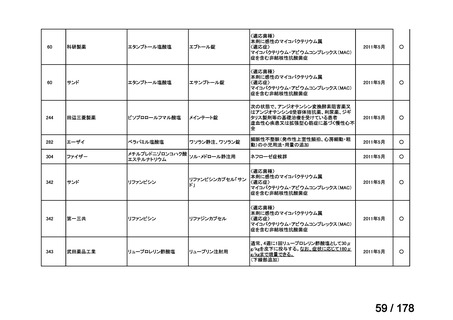
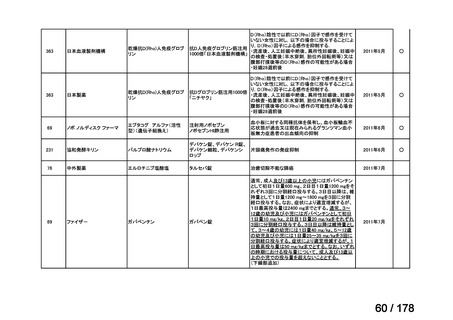
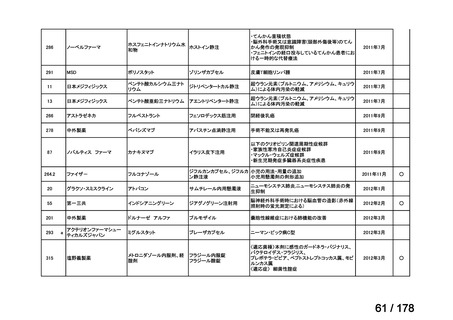
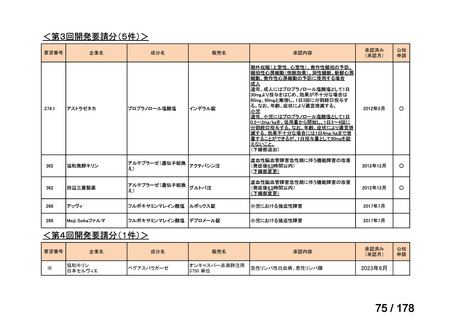
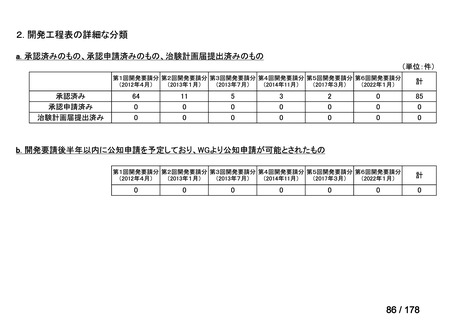
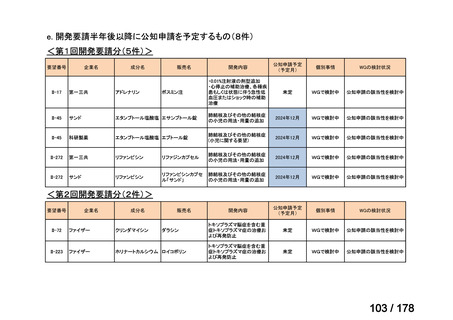
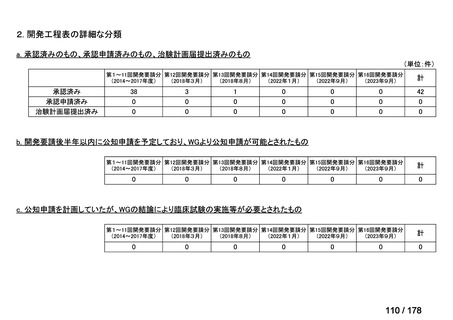
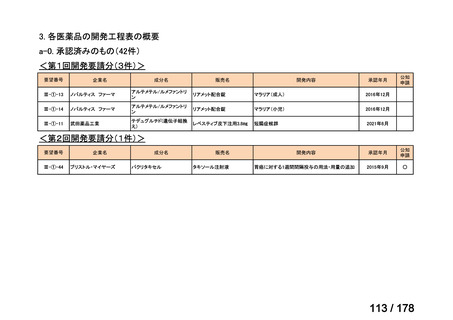
a-0. 承認済みのもの(42件)
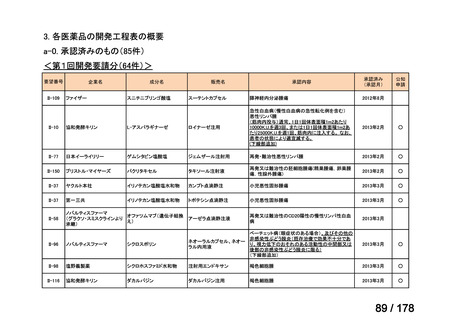
<第1回開発要請分(3件)>
要望番号
企業名
成分名
販売名
開発内容
承認年月
Ⅲ-①-13
ノバルティス ファーマ
アルテメテル/ルメファントリ
ン
リアメット配合錠
マラリア(成人)
2016年12月
Ⅲ-①-14
ノバルティス ファーマ
アルテメテル/ルメファントリ
ン
リアメット配合錠
マラリア(小児)
2016年12月
Ⅲ-①-11
武田薬品工業
テデュグルチド(遺伝子組換
え)
レベスティブ皮下注用3.8㎎
短腸症候群
2021年6月
公知
申請
<第2回開発要請分(1件)>
要望番号
Ⅲ-①-44
企業名
ブリストル・マイヤーズ
成分名
パクリタキセル
販売名
タキソール注射液
開発内容
承認年月
公知
申請
胃癌に対する1週間間隔投与の用法・用量の追加
2015年9月
○
113 / 178