よむ、つかう、まなぶ。
資料2-2 MID-NET・NDB の行政利活用の調査実施状況について[3.8MB] (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44308.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別添資料2-1
MID-NET を用いた調査結果の概要
®
2024 年 8 月 27 日
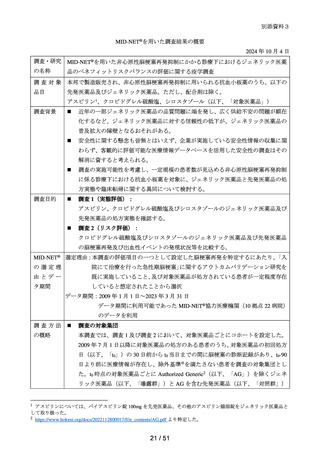
調査・研究
の名称
調査対象
品目
調査目的
MID-NET を用いたミロガバリンベシル酸塩による腎機能検査値異常のリスク評価(シ
グナル強化)
®
ミロガバリンベシル酸塩(以下、「ミロガバリン」)
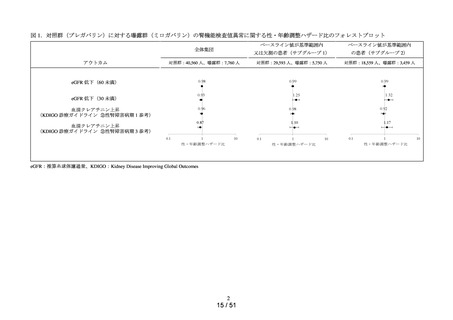
ミロガバリン処方後の腎機能検査値異常の発現頻度をプレガバリン処方後の腎機能検査
値異常の発現頻度と比較する*1。
*1 ミロガバリン及びプレガバリンの注意事項等情報において本調査で対象とする臨床検査値異常(ア
ウトカム)に関連する副作用は本調査計画時点で表 1 のとおり注意喚起されている。
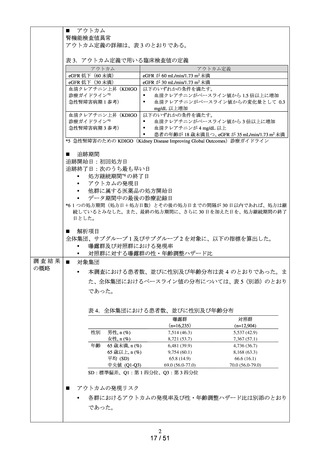
表 1.注意事項等情報におけるアウトカムに関連する副作用の注意喚起状況
アウトカムの
系統
一般名
ミロガバリン
プレガバリン
アウトカムに関連する
重大な副作用の注意喚起
関連する記載なし
0.1%未満:腎不全
腎機能
アウトカムに関連する
その他の副作用の注意喚起
関連する記載なし
0.3%以上 1%未満:血中クレア
チニン増加
頻度不明:乏尿
デ ー タ ソ MID-NET®
ース
(データ期間:2016 年 1 月 1 日~2022 年 6 月 30 日)
調 査 方 法 ◼ 調査対象集団
の概略
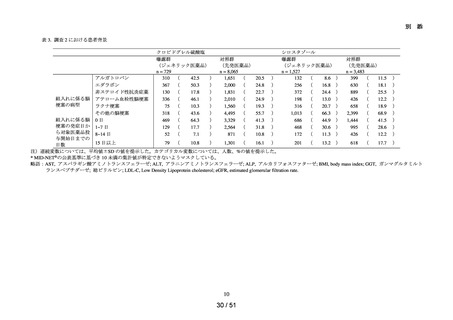
<全体集団>
データ期間中に曝露医薬品(ミロガバリン)又は対照医薬品(プレガバリン)が処方さ
れた患者(ただし、初回処方日*2 にミロガバリン及びプレガバリンの両方が処方された
患者は除く)のうち、データ期間中の最初の診療記録日が初回処方日の 181 日以上前に
ある患者を全体集団とした*3。初回処方日に処方された医薬品の種類に応じて、曝露群
(ミロガバリン群)と対照群(プレガバリン群)に分類した。
*2 データ期間中の曝露医薬品又は対照医薬品の処方日のうち、最も早い処方日。
*3 全体集団は、表 2 におけるベースライン値に関する条件がないため、ベースライン値においてアウ
トカムに該当する臨床検査値異常が既に認められている患者も含まれる。
<サブグループ 1>
全体集団のうち、アウトカムに関連するベースライン値が基準範囲内又は欠測の患者を
サブグループ 1 とした(表 2 における集計カテゴリが①、②又は④に該当する集団)。
<サブグループ 2>
全体集団のうち、アウトカムに関連するベースライン値が基準範囲内の患者をサブグル
ープ 2 とした(表 2 における集計カテゴリが①又は②に該当する集団)。
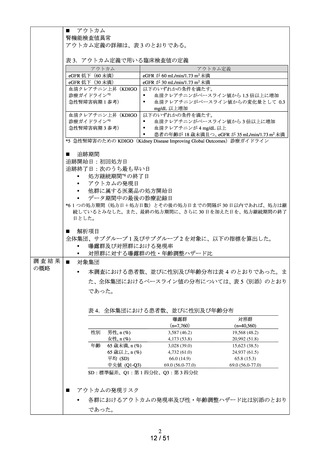
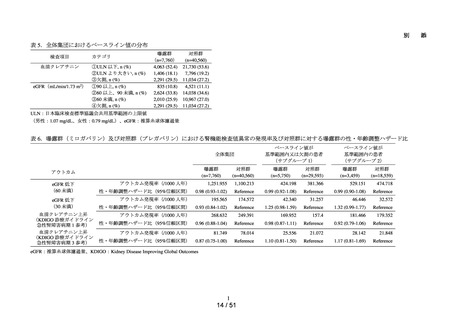
表 2.ベースライン値*4 の判定
検査項目
eGFR
集計カテゴリ
①90 mL/min/1.73 m2 以上
②60 mL/min/1.73 m2 以上、90 mL/min/1.73 m2 未満
③60 mL/min/1.73 m2 未満
④欠測
*4 ベースライン値は、初回処方日の 180 日前から初回処方日までの検査結果とした。なお、複数の検
査結果が存在する場合は、初回処方日に最も近い日の検査結果をベースライン値とした。
1
11 / 51
MID-NET を用いた調査結果の概要
®
2024 年 8 月 27 日
調査・研究
の名称
調査対象
品目
調査目的
MID-NET を用いたミロガバリンベシル酸塩による腎機能検査値異常のリスク評価(シ
グナル強化)
®
ミロガバリンベシル酸塩(以下、「ミロガバリン」)
ミロガバリン処方後の腎機能検査値異常の発現頻度をプレガバリン処方後の腎機能検査
値異常の発現頻度と比較する*1。
*1 ミロガバリン及びプレガバリンの注意事項等情報において本調査で対象とする臨床検査値異常(ア
ウトカム)に関連する副作用は本調査計画時点で表 1 のとおり注意喚起されている。
表 1.注意事項等情報におけるアウトカムに関連する副作用の注意喚起状況
アウトカムの
系統
一般名
ミロガバリン
プレガバリン
アウトカムに関連する
重大な副作用の注意喚起
関連する記載なし
0.1%未満:腎不全
腎機能
アウトカムに関連する
その他の副作用の注意喚起
関連する記載なし
0.3%以上 1%未満:血中クレア
チニン増加
頻度不明:乏尿
デ ー タ ソ MID-NET®
ース
(データ期間:2016 年 1 月 1 日~2022 年 6 月 30 日)
調 査 方 法 ◼ 調査対象集団
の概略
<全体集団>
データ期間中に曝露医薬品(ミロガバリン)又は対照医薬品(プレガバリン)が処方さ
れた患者(ただし、初回処方日*2 にミロガバリン及びプレガバリンの両方が処方された
患者は除く)のうち、データ期間中の最初の診療記録日が初回処方日の 181 日以上前に
ある患者を全体集団とした*3。初回処方日に処方された医薬品の種類に応じて、曝露群
(ミロガバリン群)と対照群(プレガバリン群)に分類した。
*2 データ期間中の曝露医薬品又は対照医薬品の処方日のうち、最も早い処方日。
*3 全体集団は、表 2 におけるベースライン値に関する条件がないため、ベースライン値においてアウ
トカムに該当する臨床検査値異常が既に認められている患者も含まれる。
<サブグループ 1>
全体集団のうち、アウトカムに関連するベースライン値が基準範囲内又は欠測の患者を
サブグループ 1 とした(表 2 における集計カテゴリが①、②又は④に該当する集団)。
<サブグループ 2>
全体集団のうち、アウトカムに関連するベースライン値が基準範囲内の患者をサブグル
ープ 2 とした(表 2 における集計カテゴリが①又は②に該当する集団)。
表 2.ベースライン値*4 の判定
検査項目
eGFR
集計カテゴリ
①90 mL/min/1.73 m2 以上
②60 mL/min/1.73 m2 以上、90 mL/min/1.73 m2 未満
③60 mL/min/1.73 m2 未満
④欠測
*4 ベースライン値は、初回処方日の 180 日前から初回処方日までの検査結果とした。なお、複数の検
査結果が存在する場合は、初回処方日に最も近い日の検査結果をベースライン値とした。
1
11 / 51