よむ、つかう、まなぶ。
資料2-2 MID-NET・NDB の行政利活用の調査実施状況について[3.8MB] (23 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44308.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
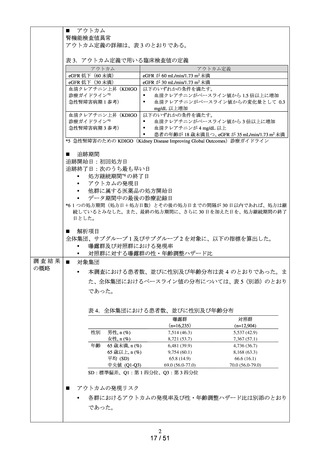
<安全性探索的評価項目 1:輸血又は止血処置を伴う出血性イベント>
以下の条件 1 かつ条件 2 を満たした場合
•
条件 1. 「頭蓋内出血、硬膜下血腫、眼底出血、鼻出血、肺出血、腹部血
腫、後腹膜出血、上部消化管出血、下部消化管出血」のいずれかの病名
が新規に付与された場合(疑い病名か否かは問わない)
•
条件 2. 条件 1 の病名が付与された、前後 30 日以内に輸血投与又は止血
処置が行われた場合
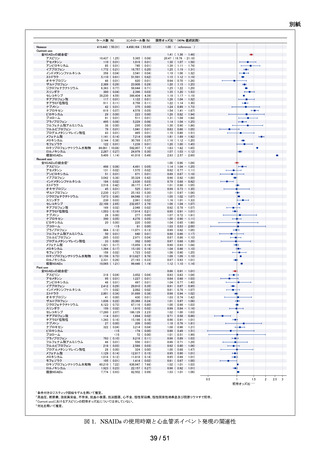
<安全性探索的評価項目 2:全ての出血性イベント>
「頭蓋内出血、硬膜下血腫、眼底出血、鼻出血、肺出血、腹部血腫、後腹膜出血、
上部消化管出血、下部消化管出血」のいずれかの病名が新規に付与された場合(疑
い病名か否かは問わない)
◼
解析を行う項目及び方法
調査 1(実態評価)
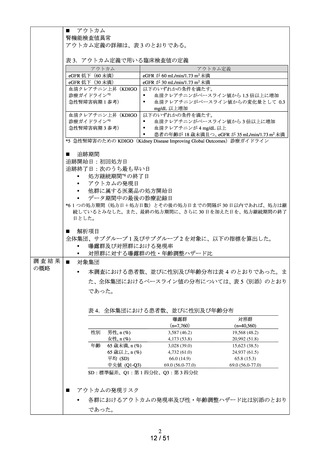
<処方実態等の確認>
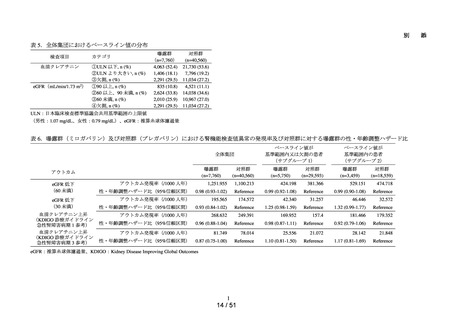
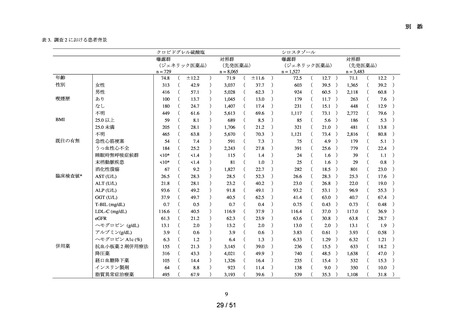
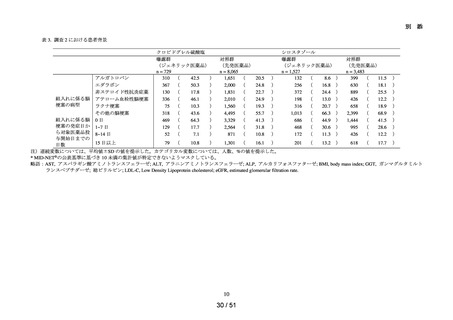
各コホートの曝露群と対照群における継続患者及び切替え患者 ※ をそれぞれ特定
し、継続患者については t0 を含む t0 前 90 日間、切替え患者については t0 を含む t0
前 90 日間及び切替え日を含む切替え日前 90 日間の患者背景(性別、年齢、医薬品
の処方歴及び疾患の既往歴等)及び追跡期間を集計した。なお、患者背景を確認す
る期間中に同じ検査項目が複数回測定されている場合には、t0 又は切替え日に最も
近い時点(t0 又は切替え日を含む)の検査値を集計対象とした。また、同日に同じ
検査項目が複数回測定されている場合には、臨床的に重症度の高い検査値を集計対
象とした。
※
切替え患者の定義:
追跡期間中に先発医薬品から同一有効成分のジェネリック医薬品に切り替えた患者、又はジ
ェネリック医薬品から同一有効成分の先発医薬品に切り替えた患者
調査 2(リスク評価)
➢
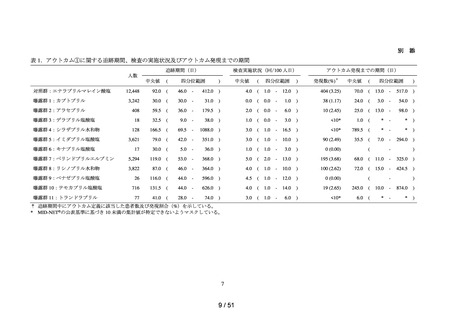
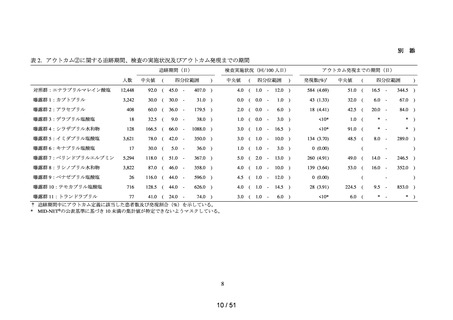
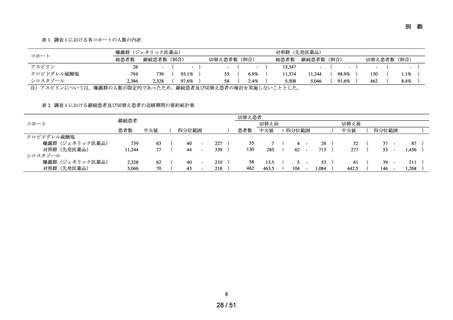
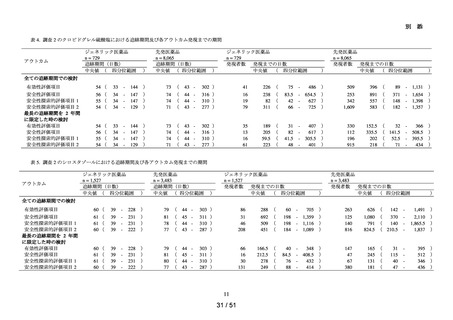
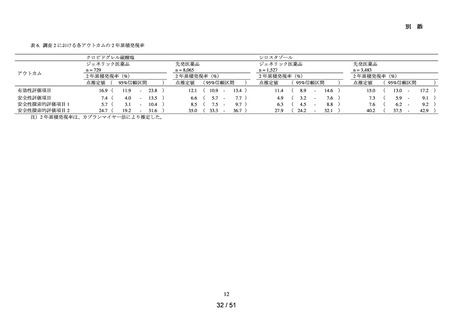
各コホートの曝露群及び対照群の患者数、追跡期間、アウトカムの発現数、ア
ウトカム発現までの期間等の要約統計量を算出した。
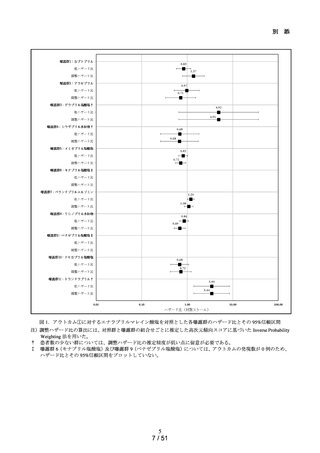
➢
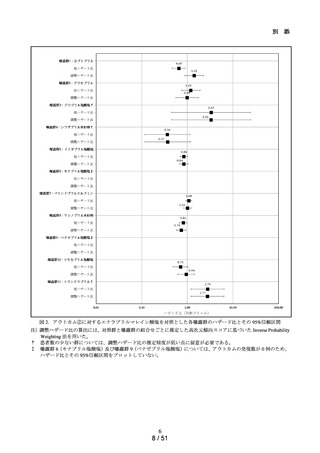
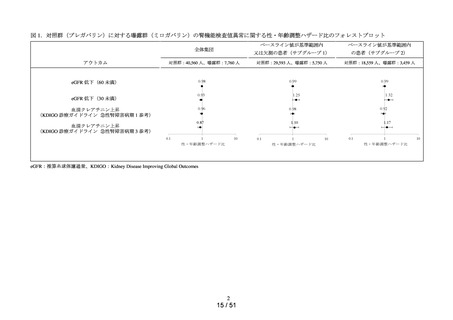
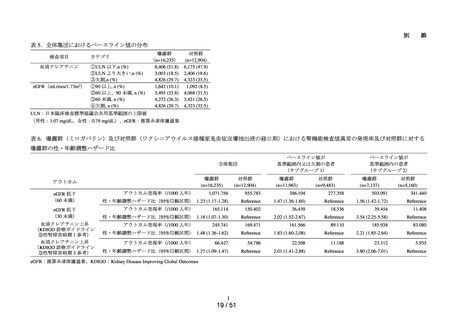
主解析として、Cox 比例ハザードモデルを用い、各アウトカム定義に関する粗
ハザード比及び調整ハザード比並びに各 95%信頼区間を推定した。調整ハザー
ド比に関しては、患者背景因子として集計した因子の中から、事前に規定した
25 種類の臨床的に重要と考えられる共変量について、各コホートの曝露群と対
照群の組合せごとに推定した傾向スコアに基づいた Standardized Mortality Ratio
Weight 法(以下、「SMRW 法」)を用いて重み付けを行って推定した。
調査結果 ◼
調査 1(実態評価)
3
23 / 51
以下の条件 1 かつ条件 2 を満たした場合
•
条件 1. 「頭蓋内出血、硬膜下血腫、眼底出血、鼻出血、肺出血、腹部血
腫、後腹膜出血、上部消化管出血、下部消化管出血」のいずれかの病名
が新規に付与された場合(疑い病名か否かは問わない)
•
条件 2. 条件 1 の病名が付与された、前後 30 日以内に輸血投与又は止血
処置が行われた場合
<安全性探索的評価項目 2:全ての出血性イベント>
「頭蓋内出血、硬膜下血腫、眼底出血、鼻出血、肺出血、腹部血腫、後腹膜出血、
上部消化管出血、下部消化管出血」のいずれかの病名が新規に付与された場合(疑
い病名か否かは問わない)
◼
解析を行う項目及び方法
調査 1(実態評価)
<処方実態等の確認>
各コホートの曝露群と対照群における継続患者及び切替え患者 ※ をそれぞれ特定
し、継続患者については t0 を含む t0 前 90 日間、切替え患者については t0 を含む t0
前 90 日間及び切替え日を含む切替え日前 90 日間の患者背景(性別、年齢、医薬品
の処方歴及び疾患の既往歴等)及び追跡期間を集計した。なお、患者背景を確認す
る期間中に同じ検査項目が複数回測定されている場合には、t0 又は切替え日に最も
近い時点(t0 又は切替え日を含む)の検査値を集計対象とした。また、同日に同じ
検査項目が複数回測定されている場合には、臨床的に重症度の高い検査値を集計対
象とした。
※
切替え患者の定義:
追跡期間中に先発医薬品から同一有効成分のジェネリック医薬品に切り替えた患者、又はジ
ェネリック医薬品から同一有効成分の先発医薬品に切り替えた患者
調査 2(リスク評価)
➢
各コホートの曝露群及び対照群の患者数、追跡期間、アウトカムの発現数、ア
ウトカム発現までの期間等の要約統計量を算出した。
➢
主解析として、Cox 比例ハザードモデルを用い、各アウトカム定義に関する粗
ハザード比及び調整ハザード比並びに各 95%信頼区間を推定した。調整ハザー
ド比に関しては、患者背景因子として集計した因子の中から、事前に規定した
25 種類の臨床的に重要と考えられる共変量について、各コホートの曝露群と対
照群の組合せごとに推定した傾向スコアに基づいた Standardized Mortality Ratio
Weight 法(以下、「SMRW 法」)を用いて重み付けを行って推定した。
調査結果 ◼
調査 1(実態評価)
3
23 / 51