資料2-4 緊急承認された医薬品の市販後安全対策について[10.9MB] (107 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
医薬品リスク管理計画書(RMP)の概要
販売名
ゾコーバ錠125mg
有効成分
エンシトレルビル フマル酸
製造販売業者
塩野義製薬株式会社
薬効分類
87625
提出年月日
令和5年7月20日
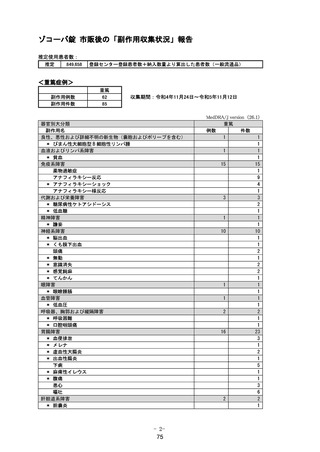
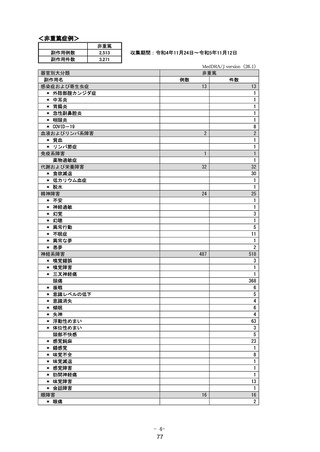
1.1. 安全性検討事項
【重要な特定されたリスク】
アナフィラキシー
【重要な潜在的リスク】
催奇形性
【重要な不足情報】
中等度以上の肝機能障害患者で
の安全性
1.2. 有効性に関する検討事項
国際共同第Ⅱ/Ⅲ相試験(T1221試験)の第Ⅲ相パートでの有効性
↓上記に基づく安全性監視のための活動
↓上記に基づくリスク最小化のための活動
2. 医薬品安全性監視計画の概要
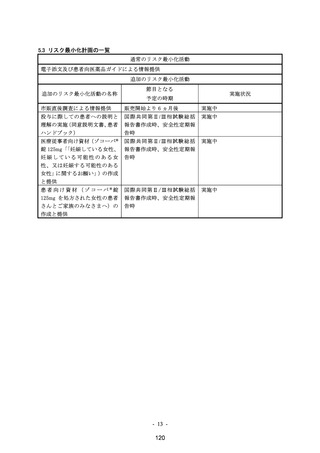
4. リスク最小化計画の概要
通常の医薬品安全性監視活動
通常のリスク最小化活動
追加の医薬品安全性監視活動
追加のリスク最小化活動
市販直後調査
市販直後調査による情報提供
一般使用成績調査
投与に際しての患者への説明と理解の実施(同意説
肝機能障害を有する被験者を対象とした臨床薬理試
明文書・患者ハンドブック)
験
医療従事者向け資材(ゾコーバ®錠125mg「「妊娠し
ている女性、妊娠している可能性のある女性、又は
妊娠する可能性のある女性」に関するお願い」)の
作成と提供
3. 有効性に関する調査・試験の計画の概要
患者向け資材(ゾコーバ®錠125mg を処方された女
国際共同第Ⅱ/Ⅲ相試験(T1221試験)
性の患者さんとご家族のみなさまへ)の作成と提供
各項目の内容は RMP の本文でご確認下さい。
107