資料2-4 緊急承認された医薬品の市販後安全対策について[10.9MB] (17 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
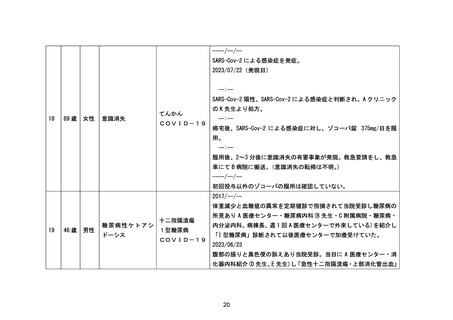
値:157~474) 1120、GDH(-)、トキシン(-)
2023/03/24
肺炎像あり。
2023/03/25
SARS-Cov2Ag 定性(-)、SARS-CoV-2RNA(+)、再燃したため、ゾコーバ錠
375mg/日を開始。ベクルリーは未処方。ゾコーバ錠は 3/25、26 処方。
加えて、抗真菌薬、抗菌薬等投与。
ゾコーバ錠を選んだ理由について、患者は橋本病の後遺症で舌が小さ
く、嚥下困難であるため、他剤に比べて錠剤が小さく服用しやすいゾ
コーバ錠を処方した。また、症状の程度について検討し、発熱、咳が
あったため、症状改善効果が期待できるゾコーバ錠を処方した。重症
化の恐れがある免疫抑制状態にある患者であった。
FluA RNA(-)、FluB RNA(-)
----/--/-意識障害及び失見当識あり。
2023/03/27(発現日)
フィニバックス点滴静注用
0.5g/日投与開始(使用理由未記載)。
劇症肝炎が発現。
AST、ALT、LDH 等の肝機能値が上昇し、劇症肝炎と診断したためゾコー
バ錠は 1 日分しか服薬していない。
(AST 上昇、ALT 上昇、LDH 上昇が
発現。)
ステロイドパルス療法を実施。
17