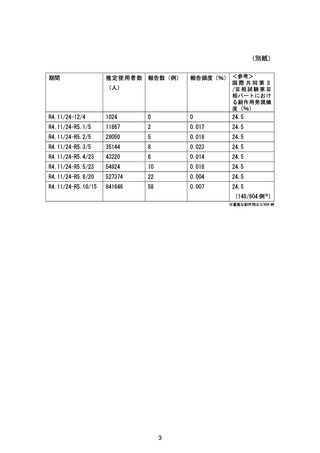
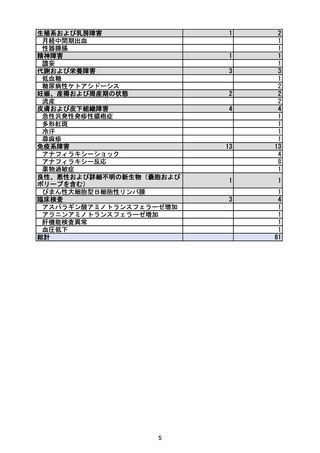
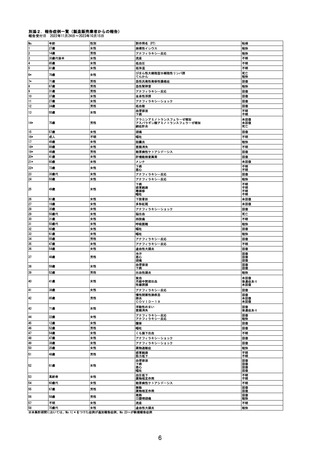
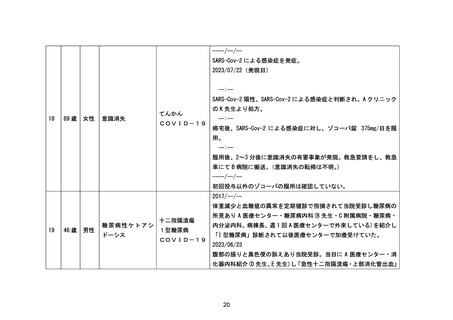
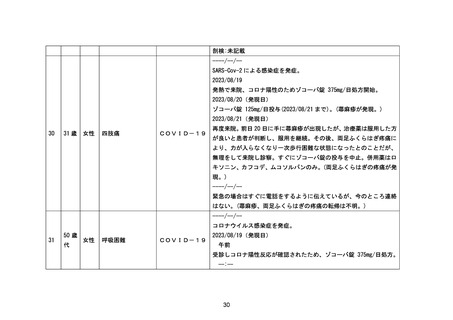
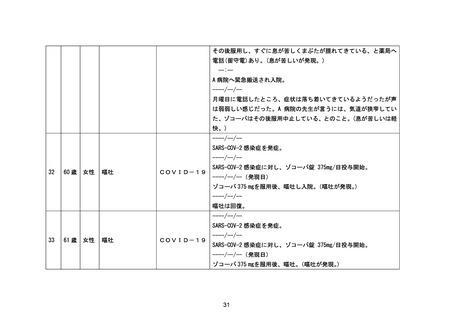
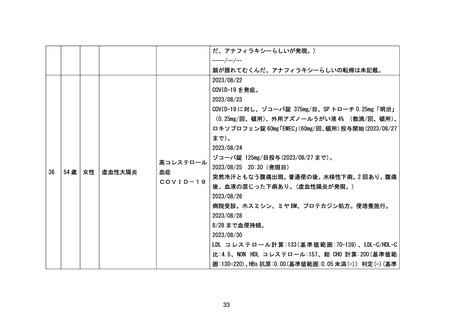
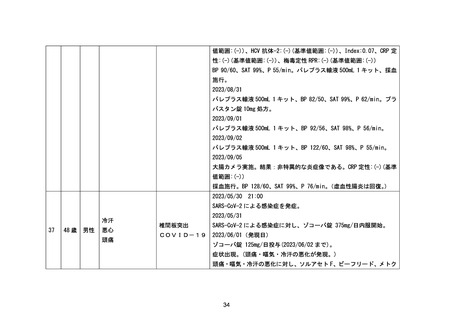
資料2-4 緊急承認された医薬品の市販後安全対策について[10.9MB] (51 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
----/--/-54
60 歳
代
女性
糖 尿 病 性ケ ト アシ 1型糖尿病
ドーシス
COVID-19
COVID-19 に対し、ゾコーバ錠(投与量未記載)投与開始。
----/--/--(発現日)
ゾコーバ錠投与 3 日目に糖尿病性ケトアシドーシスにて ICU 入院。(糖
尿病性ケトアシドーシスが発現。)
----/--/-糖尿病性ケトアシドーシスの転帰は未記載。
----/--/-不眠症に対し、ベルソムラ錠 20mg/日投与開始(2023/08/25 まで)。
統合失調症に対し、クエチアピン錠 300mg/日投与開始(継続)。
2023/08/24
SARS-CoV-2 による感染症を発症。
55
67 歳 男性
不眠症
SARS-CoV-2 による感染症にてゾコーバ錠が処方あり。
無動
小脳梗塞
自宅に帰宅後ゾコーバ錠 125mg3 錠(375mg/日)内服。もともと小脳梗
薬物相互作用
統合失調症
塞と統合失調症にて内服している薬剤があり。
COVID-19
2023/08/25(発現日)
--:-ゾコーバ錠 125mg/日投与(同日まで)。
03:00 頃
自宅トイレにて動けなくなっている本人を家族が発見。
自宅にて経過みていたが通常より動きが悪いため救急要請。
51