資料2-4 緊急承認された医薬品の市販後安全対策について[10.9MB] (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
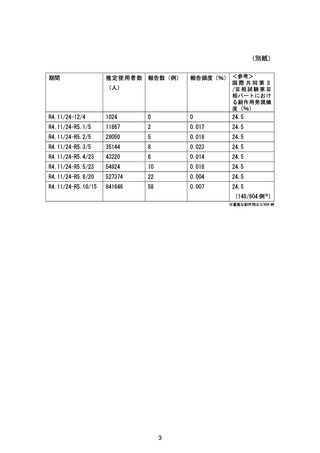
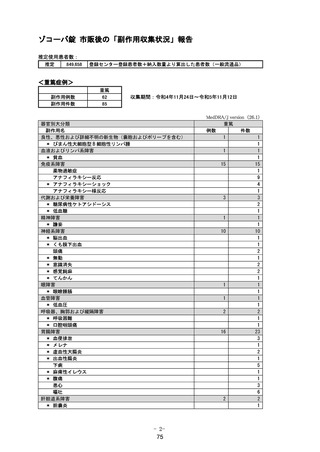
報告受付日
2022年11月24日~2023年10月15日
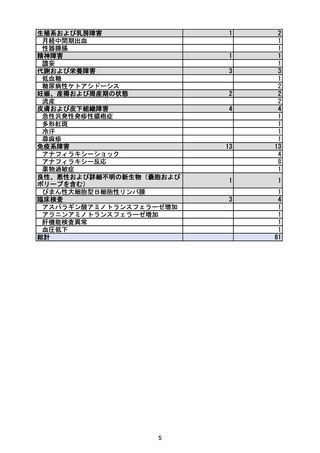
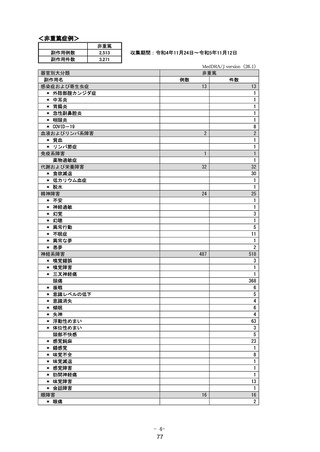
器官別大分類
副作用名
胃腸障害
メレナ
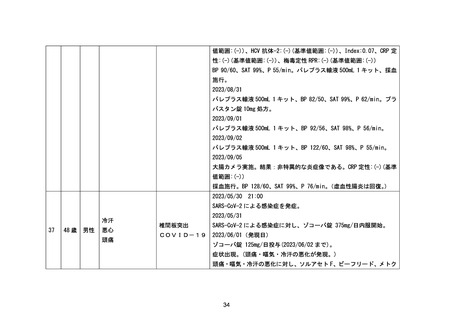
悪心
下痢
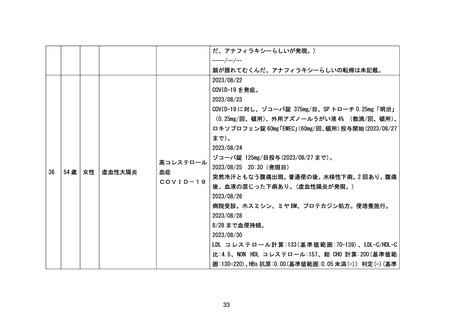
虚血性大腸炎
血便排泄
出血性腸炎
麻痺性イレウス
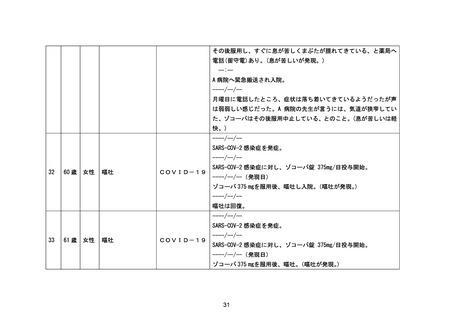
嘔吐
一般・全身障害および投与部位の状態
全身性浮腫
低体温
発熱
薬物相互作用
感染症および寄生虫症
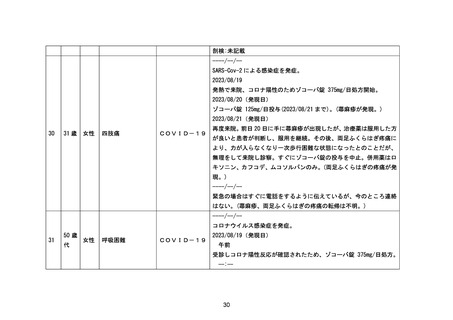
COVID-19
肺炎
肝胆道系障害
劇症肝炎
胆嚢炎
筋骨格系および結合組織障害
筋力低下
四肢痛
血液およびリンパ系障害
貧血
血管障害
低血圧
呼吸器、胸郭および縦隔障害
呼吸困難
口腔咽頭痛
慢性閉塞性肺疾患
傷害、中毒および処置合併症
下肢骨折
神経系障害
くも膜下出血
てんかん
意識消失
感覚鈍麻
頭痛
脳出血
浮動性めまい
無動
腎および尿路障害
急性腎障害
例数
件数
15
5
1
2
2
1
1
3
1
10
1
4
22
1
3
5
2
3
1
1
6
5
1
1
1
2
2
1
1
2
1
1
2
1
1
1
1
1
1
3
1
1
1
1
1
11
1
1
2
2
2
1
1
1
1
1