資料2-4 緊急承認された医薬品の市販後安全対策について[10.9MB] (34 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36611.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第2回 11/30)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
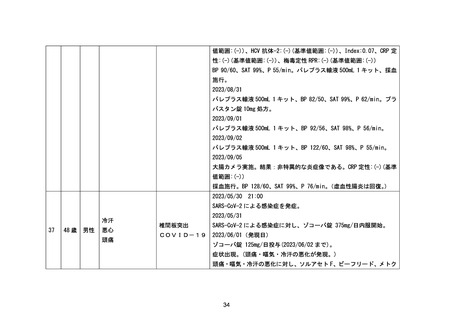
性:(-)(基準値範囲:(-))、梅毒定性 RPR:(-)(基準値範囲:(-))
BP 90/60、SAT 99%、P 55/min。パレプラス輸液 500mL 1 キット、採血
施行。
2023/08/31
パレプラス輸液 500mL 1 キット、BP 82/50、SAT 99%、P 62/min。プラ
バスタン錠 10mg 処方。
2023/09/01
パレプラス輸液 500mL 1 キット、BP 92/56、SAT 98%、P 56/min。
2023/09/02
パレプラス輸液 500mL 1 キット、BP 122/60、SAT 98%、P 55/min。
2023/09/05
大腸カメラ実施。結果:非特異的な炎症像である。CRP 定性:(-)(基準
値範囲:(-))
採血施行。BP 128/60、SAT 99%、P 76/min。(虚血性腸炎は回復。
)
2023/05/30
21:00
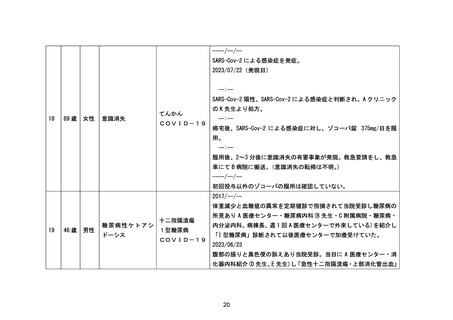
SARS-CoV-2 による感染症を発症。
冷汗
37
48 歳 男性
悪心
頭痛
2023/05/31
椎間板突出
SARS-CoV-2 による感染症に対し、ゾコーバ錠 375mg/日内服開始。
COVID-19
2023/06/01(発現日)
ゾコーバ錠 125mg/日投与(2023/06/02 まで)。
症状出現。(頭痛・嘔気・冷汗の悪化が発現。)
頭痛・嘔気・冷汗の悪化に対し、ソルアセト F、ビーフリード、メトク
34