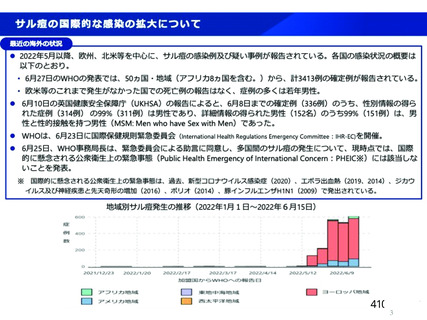
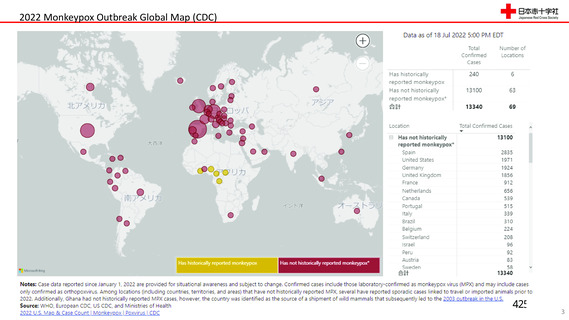
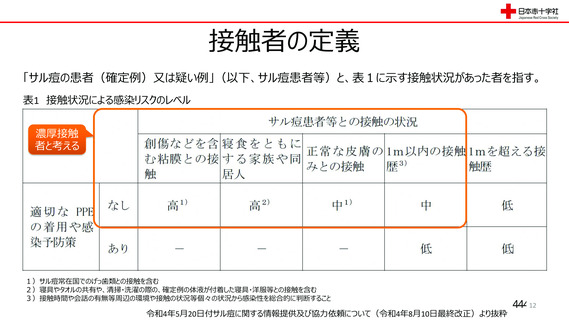
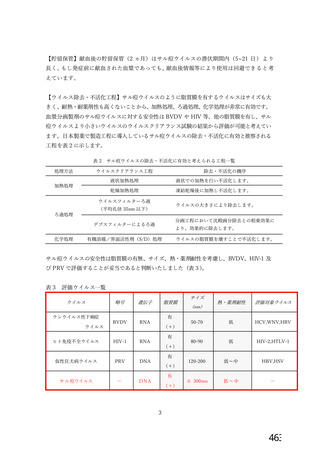
資 料4-2-➁ 令和4年度第2回安全技術調査会の審議結果について➁ (83 ページ)
出典
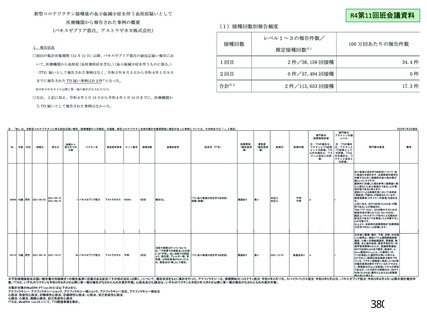
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_27906.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第2回 9/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
バキスゼブリア筋注(以下、本剤)は、非増殖性の弱毒化されたサル(チンパンジー)由来のアデノ
ウイルス
(ウイルスベクター)
に、SARS-CoV-2のスパイク糖タンパク質の遺伝子を組み込んだ新し
い製造方法によるワクチンです。
本剤は、本邦での早急なワクチン供給の必要性を踏まえて特例承認されたものであり、承認時にお
ける長期安定性等の情報は限られています。また、本剤接種後の長期の安全性に関する情報は得
られていないことから、製造販売後も引き続き慎重に情報収集を継続する必要があります。
本剤を安全にご使用いただくために、本剤のリスクおよび使用方法を十分ご理解いただくことが重
要であることから、本適正使用ガイドにおいて適正な被接種者の確認、接種方法、接種後の副反
応について解説を行っています。
本剤は、本適正使用ガイド、最新の添付文書を熟読の上、「予防接種実施規則」
および「新型コロ
ナウイルス感染症に係る臨時の予防接種実施要領」
に準拠してご使用ください。
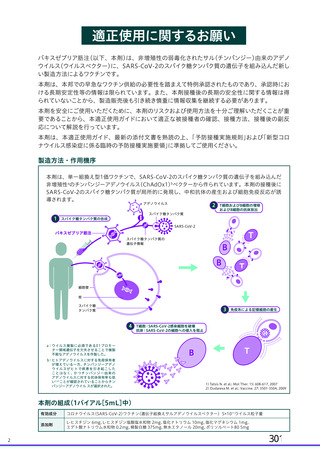
製造方法・作用機序
本剤は、単一組換え型1価ワクチンで、SARS-CoV-2のスパイク糖タンパク質の遺伝子を組み込んだ
非増殖性aのチンパンジーアデノウイルス
(ChAdOx1)bベクターから作られています。本剤の接種後に
SARS-CoV-2のスパイク糖タンパク質が局所的に発現し、中和抗体の産生および細胞免疫反応が誘
導されます。
アデノウイルス
1
2
スパイク糖タンパク質
スパイク糖タンパク質の合成
T細胞およびB細胞の増殖
およびB細胞の抗体放出
SARS-CoV-2
T
バキスゼブリア筋注
スパイク糖タンパク質の
遺伝子情報
B
B
細胞壁
核
スパイク糖
タンパク質
3
4
a:ウイルス複製に必須であるE1プロモー
ター領域遺伝子を欠失させることで複製
不能なアデノウイルスを作製した。
b:ヒトアデノウイルスに対する免疫保有者
が増えている一方、チンパンジーアデノ
ウイルスがヒトで疾患を引き起こした
ことはなく、かつチンパンジー由来の
アデノウイルスに対する抗体保有率も低
い1,2)ことが確認されていることからチン
パンジーアデノウイル スが選択された。
免疫系による記憶細胞の産生
T細胞:SARS-CoV-2感染細胞を破壊
抗体:SARS-CoV-2の細胞への侵入を阻止
B
T
1)Tatsis N. et al.: Mol Ther. 15: 608-617, 2007
2)Dudareva M. et al.: Vaccine. 27: 3501-3504, 2009
本剤の組成(1バイアル
[5mL]
中)
2
有効成分
コロナウイルス(SARS-CoV-2)ワクチン(遺伝子組換えサルアデノウイルスベクター) 5×1011ウイルス粒子量
添加剤
L-ヒスチジン 6mg、L-ヒスチジン塩酸塩水和物 2mg、塩化ナトリウム 10mg、塩化マグネシウム 1mg、
エデト酸ナトリウム水和物 0.2mg、精製白糖 375mg、無水エタノール 20mg、ポリソルベート80 5mg
301