よむ、つかう、まなぶ。
参考資料1-1 TERMS(第 8 版)と TERMS(第 9 版)改訂案の対比表[2.6MB] (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_40908.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会安全対策調査会(令和6年度第3回 6/25)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
頁
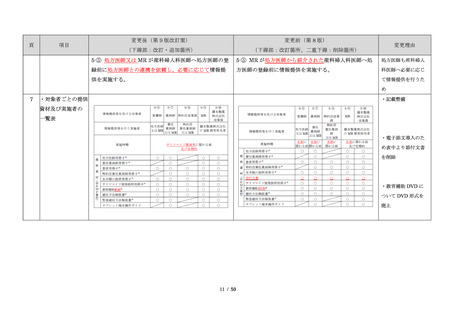
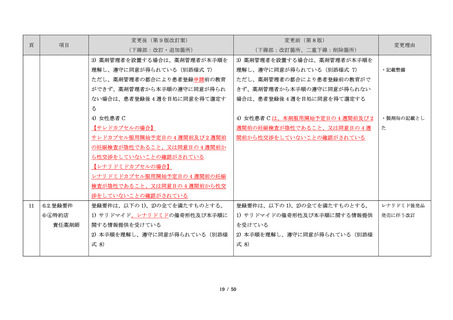
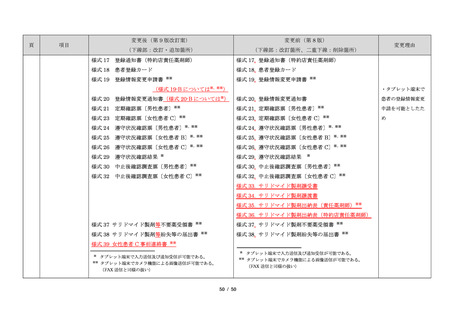
変更後(第 9 版改訂案)
変更前(第 8 版)
(下線部:改訂・追加箇所)
(下線部:改訂箇所、二重下線:削除箇所)
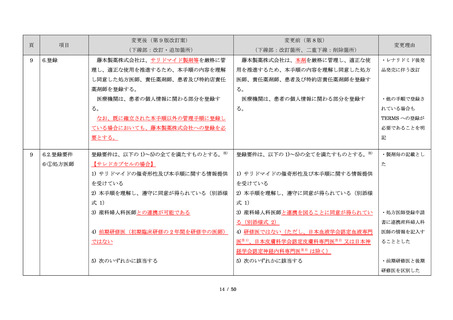
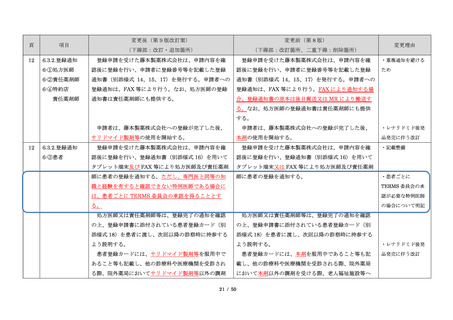
調査結果を踏まえ、患者の治療アクセスを阻害すること
このような状況のもと、藤本製薬株式会社は、サリド
項目
なく胎児曝露を防止するという観点から、必要な改訂を
マイド製剤(サレドカプセル)の製造販売開始にあた
行ってきた。
り、本邦の医療現場にあった安全管理手順が必要と考
2012 年 5 月に「らい性結節性紅斑」、2021 年 2 月に
え、関係者の意見を伺いながら、情報提供及び教育、登
「クロウ・深瀬(POEMS)症候群」の効能・効果の追加
録、中央一元管理、評価を重要な構成要素とする本手順
承認を取得し、その都度改訂を行ってきた。
を作成した。
このたび、新たに製造販売するレナリドミドカプセル
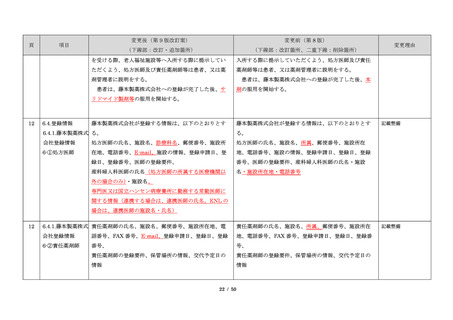
変更理由
サリドマイド製剤(サレドカプセル)が 2008 年 10 月
は、サリドマイドの誘導体を主成分としていることか
に「再発又は難治性の多発性骨髄腫」の治療薬として承
ら、サレドカプセルとレナリドミドカプセルの両方を厳
認を受けて以来、本手順の実施状況等の調査結果を踏ま
格に管理し、医療現場及び患者の負担を軽減するようサ
え、患者の治療アクセスを阻害せずに胎児曝露を防止す
リドマイド製剤等安全管理手順(TERMS®)に改訂した。
るという観点から、必要な改訂を行ってきた。
2012 年 5 月には「らい性結節性紅斑」の効能・効果の
追加承認による改訂を行い、さらに 2021 年 2 月に「クロ
ウ・深瀬(POEMS)症候群」の効能・効果の追加承認を
取得したことから、改訂を行った。
2022 年 7 月に医療現場の利便性を図るためにタブレッ
ト端末を追加導入したことにより、改訂を行った。
1
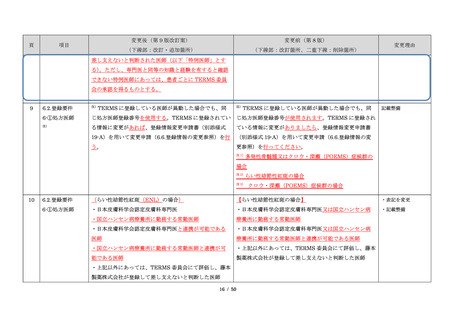
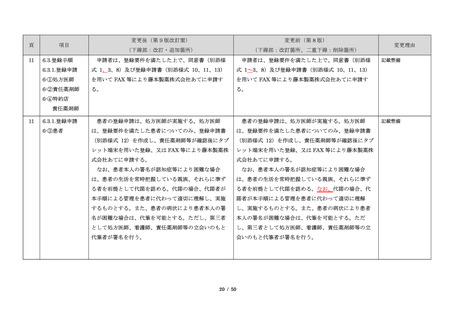
2.目的
本手順は、藤本製薬株式会社が製造販売承認を受けた
本手順は、藤本製薬株式会社が製造販売承認を受けた
サレドカプセル、レナリドミドカプセル(以下、
「サリド
サリドマイド製剤(サレドカプセル;以下、
「本剤」とい
マイド製剤等」という)を厳格に管理し、併せてこの厳
う)を厳格に管理し、併せてこの厳格な管理を基盤とし
格な管理を基盤としたサリドマイド製剤等の適正な使用
た本剤の適正な使用を推進し、本剤の胎児への曝露を防
を推進し、サリドマイド製剤等の胎児への曝露を防止す
止することを目的とする。
ることを目的とする。
3 / 50
レナリドミド後発品
発売に伴う改訂
変更後(第 9 版改訂案)
変更前(第 8 版)
(下線部:改訂・追加箇所)
(下線部:改訂箇所、二重下線:削除箇所)
調査結果を踏まえ、患者の治療アクセスを阻害すること
このような状況のもと、藤本製薬株式会社は、サリド
項目
なく胎児曝露を防止するという観点から、必要な改訂を
マイド製剤(サレドカプセル)の製造販売開始にあた
行ってきた。
り、本邦の医療現場にあった安全管理手順が必要と考
2012 年 5 月に「らい性結節性紅斑」、2021 年 2 月に
え、関係者の意見を伺いながら、情報提供及び教育、登
「クロウ・深瀬(POEMS)症候群」の効能・効果の追加
録、中央一元管理、評価を重要な構成要素とする本手順
承認を取得し、その都度改訂を行ってきた。
を作成した。
このたび、新たに製造販売するレナリドミドカプセル
変更理由
サリドマイド製剤(サレドカプセル)が 2008 年 10 月
は、サリドマイドの誘導体を主成分としていることか
に「再発又は難治性の多発性骨髄腫」の治療薬として承
ら、サレドカプセルとレナリドミドカプセルの両方を厳
認を受けて以来、本手順の実施状況等の調査結果を踏ま
格に管理し、医療現場及び患者の負担を軽減するようサ
え、患者の治療アクセスを阻害せずに胎児曝露を防止す
リドマイド製剤等安全管理手順(TERMS®)に改訂した。
るという観点から、必要な改訂を行ってきた。
2012 年 5 月には「らい性結節性紅斑」の効能・効果の
追加承認による改訂を行い、さらに 2021 年 2 月に「クロ
ウ・深瀬(POEMS)症候群」の効能・効果の追加承認を
取得したことから、改訂を行った。
2022 年 7 月に医療現場の利便性を図るためにタブレッ
ト端末を追加導入したことにより、改訂を行った。
1
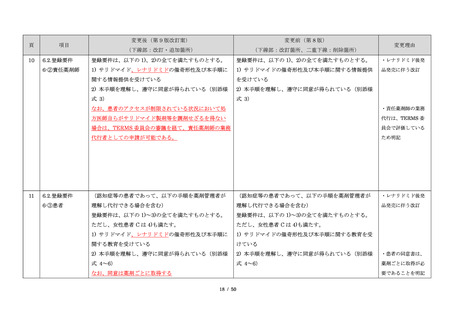
2.目的
本手順は、藤本製薬株式会社が製造販売承認を受けた
本手順は、藤本製薬株式会社が製造販売承認を受けた
サレドカプセル、レナリドミドカプセル(以下、
「サリド
サリドマイド製剤(サレドカプセル;以下、
「本剤」とい
マイド製剤等」という)を厳格に管理し、併せてこの厳
う)を厳格に管理し、併せてこの厳格な管理を基盤とし
格な管理を基盤としたサリドマイド製剤等の適正な使用
た本剤の適正な使用を推進し、本剤の胎児への曝露を防
を推進し、サリドマイド製剤等の胎児への曝露を防止す
止することを目的とする。
ることを目的とする。
3 / 50
レナリドミド後発品
発売に伴う改訂