会議資料 (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00033.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第59回 7/5)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
40
要望番号
Ⅳ-138
成分名
エトポシド
要望効能・効果
要望用法・用量
要望者
会社名
未承認薬
適応外薬
の分類
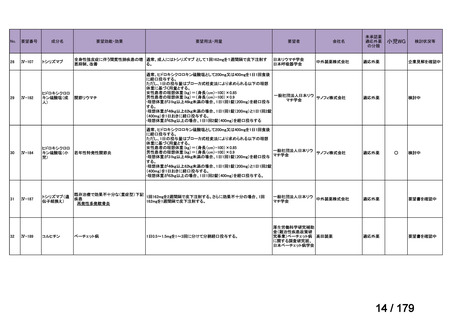
造血幹細胞移植の前治療
同種造血幹細胞移植前治療として、1日15~30mg/kgを点滴静注し、2日
間投与する。自己造血幹細胞移植前治療として、1日500mg/m2を点滴 日本造血・免疫細胞療
日本化薬
静注し、3日間投与、もしくは1日400mg/m2を点滴静注し、4日間投与す 法学会
る。疾患及び患者の状態により適宜減量する。
適応外薬
造血幹細胞移植の前治療
(小児)
同種造血幹細胞移植前治療として、
標準体重30kg未満:1日60 mg/kg、標準体重30kg以上:1日1800 mg/m2
日本造血・免疫細胞療
(最大3000 mg)を点滴静注し、1日間投与する。
日本化薬
法学会
自己造血幹細胞移植前治療として、
1日200 mg/m2 を点滴静注し、4日間投与する。疾患及び患者の状態に
より適宜減量する。
適応外薬
41
Ⅳ-139
エトポシド
42
Ⅳ-144
フルダラビンリン
酸エステル(成
造血幹細胞移植の前治療
人)
フルダラビンリン酸エステルとして、1日量30mg/m2(体表面積)を6日間
日本造血・免疫細胞療法学
連日点滴静注(約30分)する。なお、患者の状態により、投与量及び投与 会
サノフィ株式会社
日数は適宜減ずる。
適応外薬
43
Ⅳ-145
フルダラビンリン
酸エステル(小
造血幹細胞移植の前治療
児)
(小児) フルダラビンリン酸エステルとして、1日量30mg/m2(体表面積)を
日本造血・免疫細胞療法学
6日間連日点滴静注(約30分)する。なお、患者の状態により、投与量及 会
サノフィ株式会社
び投与日数は適宜減ずる。
適応外薬
Ⅳ-146
メルファラン(成
人)
造血幹細胞移植の前治療
成人
メルファランとして1日1回60mg/m2を3日間投与(メルファラン3日間総量
日本造血・免疫細胞療法学 アスペンジャパン株式会
180mg/m2)する。
会
社
多発性骨髄腫に対してはメルファランとして1日1回100mg/m2を2日間投
与(メルファラン2日間総量200mg/m2)も可とする。
適応外薬
45
Ⅳ-147
メルファラン(小
児)
造血幹細胞移植の前治療
小児
メルファランとして1日1回70mg/m2を3日間投与(メルファラン3日間総量
日本造血・免疫細胞療法学 アスペンジャパン株式会
210mg/m2)する。
会
社
なお、メルファラン総量及び1日投与量は、患者の状態、併用する薬剤、
全身放射線照射併用により適宜減量する。
適応外薬
46
Ⅳ-156
ベムラフェニブ
BRAF V600変異を有するエルドハイム・
チェスター病(Erdheim-Chester disease: ベムラフェニブとして1回960mgを1日2回経口投与する
ECD)
44
日本血液学会
中外製薬株式会社
適応外薬
小児WG
検討状況等
企業見解を確認中
○
企業見解を確認中
企業見解待ち
○
企業見解待ち
企業見解待ち
○
企業見解待ち
企業見解を確認中
16 / 179