会議資料 (39 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00033.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第59回 7/5)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
非盲検導入期及び二重盲検期を併合した本薬投与例における安全性について、有害事象
は本薬投与例の 77%(516/673 例)に認められ、発現割合の高かった有害事象は上咽頭炎
17%(117/673 例)
、上気道感染 12%(80/673 例)
、axSpA の悪化 9%(58/673 例)、頭痛 8%
(55/673 例)
、下痢 6%(42/673 例)であった。死亡は認められなかった。
重篤な有害事象は 4%(28/673 例)に認められた。
投与中止に至った有害事象は 3%(18/673 例)に認められた。
感染症は 53%(355/673 例)に認められ、そのうち重篤な感染症は 1%(7/673 例)に認め
られた。悪性腫瘍は、<1%(1/153 例〔胃腺癌〕
)に認められた。活動性結核、血管炎、う
っ血性心不全、脳卒中及びループス様症候群は認められなかった。
※4 主な組入れ基準:①axSpA の ASAS 分類基準を満たす、②AS に対する 1984 年改訂ニューヨーク基準の X
線検査基準を満たさない、③仙腸関節若しくは脊椎の MRI 所見での活動性炎症の客観的兆候又は高感度
CRP の上昇を認める、④ASDAS 2.1 以上、BASDAI 4 以上かつ総背部痛スコア(0~10 のスケール)4 以上
の活動性である、⑤線維筋痛症又は脊椎関節炎以外の病因による炎症性関節炎の既往歴がない、⑥生物製
剤を過去に使用していない
5.要望内容に係る国内外の公表文献・成書等について
(1)無作為化比較試験、薬物動態試験等の公表論文としての報告状況
文献の検索方法(検索式や検索時期等)、検索結果、文献等の選定理由の概略等は以下
のとおりである。
<海外における報告>
本薬の nr-axSpA 患者を対象とした無作為化比較試験、薬物動態試験等に関する公表文献
を以下の方法で検索した。
データベース:PubMed
検索日:2023 年 9 月 6 日
検索式:adalimumab and (non-radiographic or nonradiographic)
検索結果:55 報
55 報のうち、nr-axSpA 患者を対象とした無作為化比較試験及びそれらの非盲検継続投与
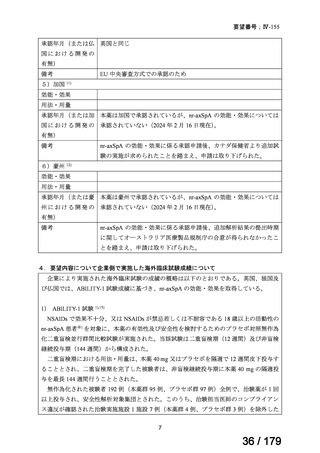
期に関する報告として、「4.要望内容について企業側で実施した海外臨床試験成績につ
いて」の項で記載した 3 報 1),13),14)が選定された。
<国内における報告>
本薬の nr-axSpA 患者を対象とした臨床試験及び症例報告等の観察研究に関する公表文献
を以下の 2 つの方法で検索した。
方法 1
データベース:PubMed
検索日:2024 年 2 月 8 日
検索式:adalimumab and (non-radiographic or nonradiographic)
10
39 / 179