会議資料 (175 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00033.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第59回 7/5)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
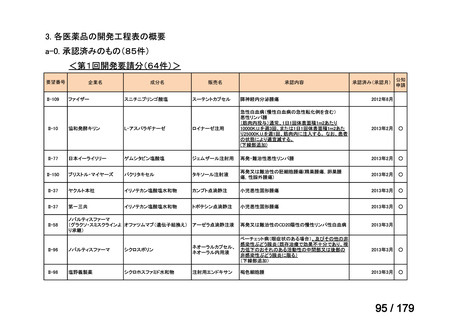
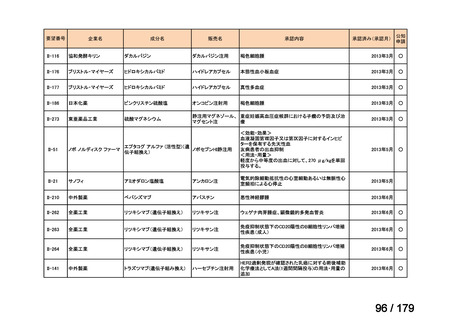
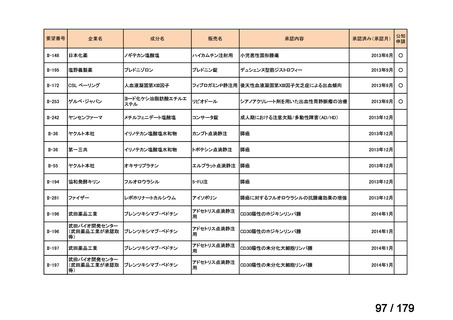
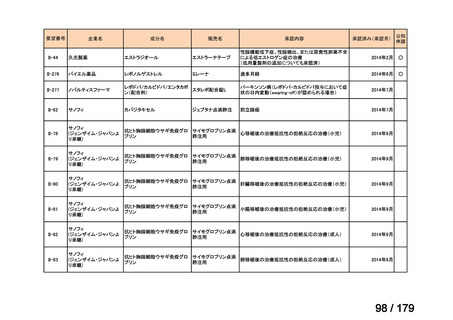
薬価専門部会(第209回)薬ー1
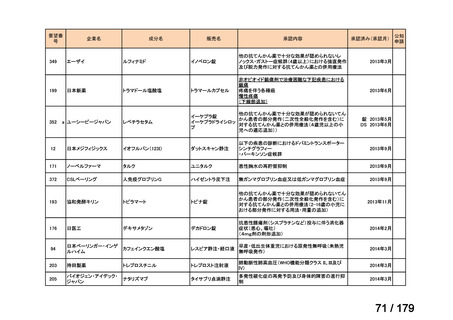
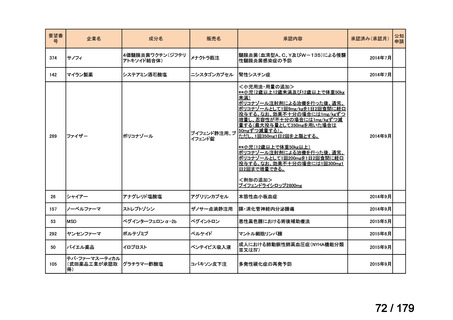
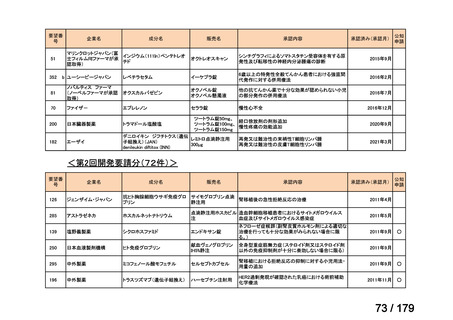
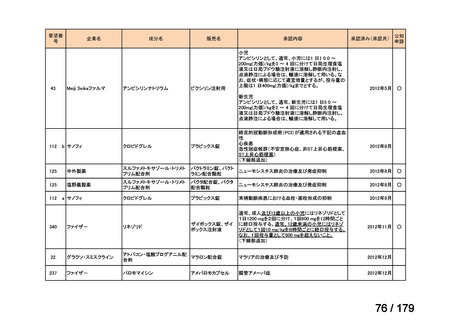
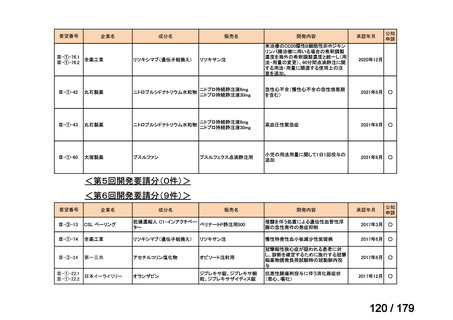
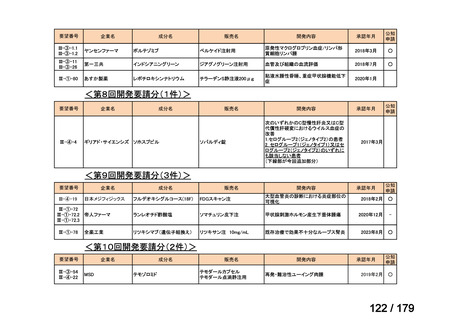
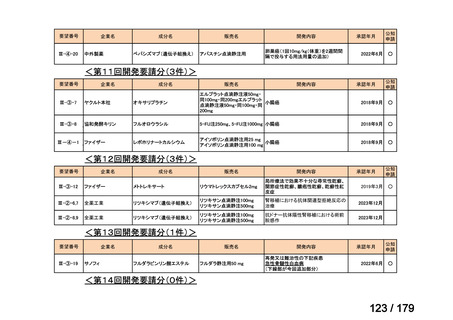
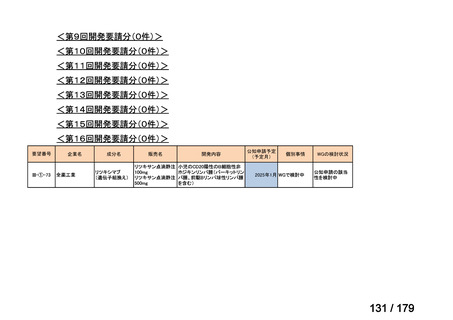
国内未承認薬(ドラッグ・ロス品目)に該当する治療薬
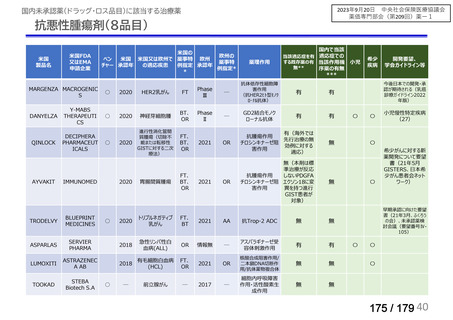
抗悪性腫瘍剤(8品目)
米国
製品名
米国FDA
又はEMA
申請企業
米国の
欧州の
ベン
米国 米国又は欧州で 薬事特 欧州
薬事特
チャー 承認年
の適応疾患
例指定 承認年
例指定*
*
MARGENZA MACROGENIC
S
○
2020
HER2乳がん
DANYELZA
Y-MABS
THERAPEUTI
CS
○
2020
QINLOCK
DECIPHERA
PHARMACEUT
ICALS
2020
AYVAKIT
○
IMMUNOMED
TRODELVY
BLUEPRINT
MEDICINES
ASPARLAS
2020
FT
Phase
Ⅲ
神経芽細胞腫
BT、
OR
Phase
Ⅱ
進行性消化管間
質腫瘍(切除不
能または転移性
GISTに対する二次
療法)
FT、
BT、
OR
胃腸間質腫瘍
FT、
BT、
OR
2021
2021
薬理作用
国内で当該
当該適応症を有 適応症での
する既存薬の有 当該作用機
無**
序薬の有無
***
―
抗体依存性細胞障
害作用
(抗HER2ヒト型モノク
ローナル抗体)
有
有
―
GD2結合モノク
ローナル抗体
有
有
OR
有(海外では
抗腫瘍作用
先行治療の無
チロシンキナーゼ阻
効例に対する
害作用
適応)
無
無(本剤は標
準治療が反応
抗腫瘍作用
しないPDGFA
チロシンキナーゼ阻 エクソン18に変
害作用
異を持つ進行
GIST患者が
対象)
無
OR
2020
トリプルネガティブ
乳がん
FT、
BT
2021
AA
抗Trop-2 ADC
無
無
SERVIER
PHARMA
2018
急性リンパ性白
血病(ALL)
OR
情報無
―
アスパラギナーゼ受
容体刺激作用
有
有
LUMOXITI
ASTRAZENEC
A AB
2018
有毛細胞白血病
(HCL)
FT、
OR
2021
OR
核酸合成阻害作用/
二本鎖DNA切断作
用/抗体薬物複合体
無
無
TOOKAD
STEBA
Biotech S.A
―
前立腺がん
―
2017
―
細胞内呼吸障害
作用・活性酸素生
成作用
無
無
○
○
小児
希少
疾病
開発要望、
学会ガイドライン等
今後日本での開発・承
認が期待される(乳癌
診療ガイドライン2022
年版)
〇
〇
小児慢性特定疾病
(27)
〇
〇
希少がんに対する新
薬開発について要望
書(21年5月
GISTERS、日本希
少がん患者会ネット
ワーク)
早期承認に向けた要望
書(21年3月、ふくろう
の会)、未承認薬検
討会議(要望番号Ⅳ105)
〇
〇
〇
175 / 179 40