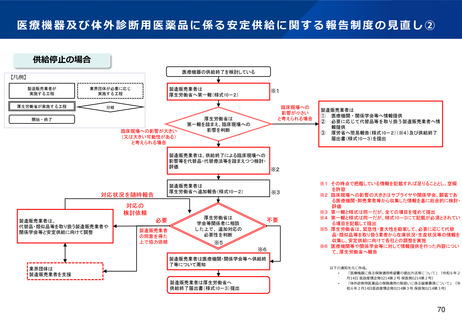
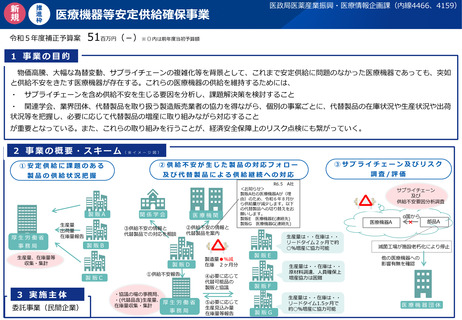
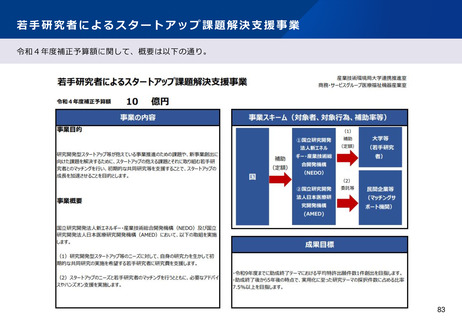
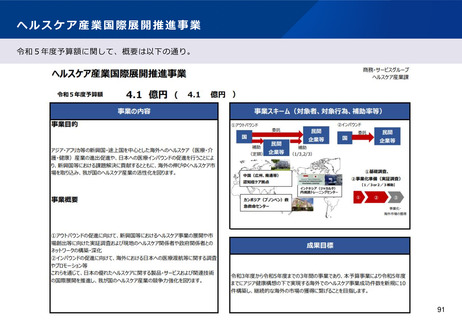
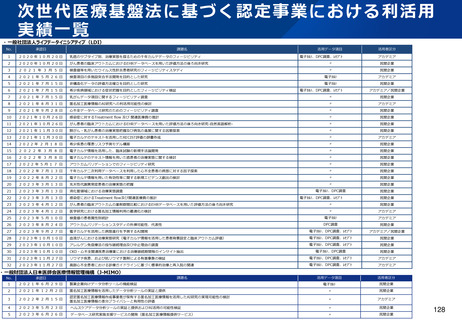
資料2-1 医療機器基本計画に関する各省における取り組みの状況について (19 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38515.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第4回 3/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
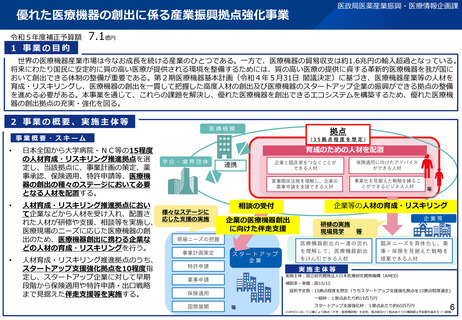
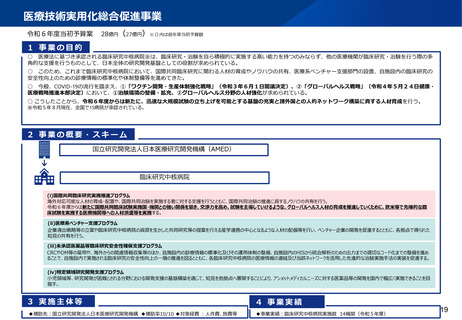
令和6年度当初予算案
28億円(27億円)※()内は前年度当初予算額
1 事業の目的
○ 医療法に基づき承認される臨床研究中核病院※は、臨床研究・治験を自ら積極的に実施する高い能力を持つのみならず、他の医療機関が臨床研究・治験を行う際の多
角的な支援を行うものとして、日本全体の研究開発基盤としての役割が求められている。
○ このため、これまで臨床研究中核病院において、国際共同臨床研究に関わる人材の育成やノウハウの共有、医療系ベンチャー支援部門の設置、自施設内の臨床研究の
安全性向上のための診療情報の標準化や体制整備等を進めてきた。
○ 今般、COVID-19の流行を踏まえ、①「ワクチン開発・生産体制強化戦略」(令和3年6月1日閣議決定)、②「グローバルヘルス戦略」(令和4年5月24日健康・
医療戦略推進本部決定)において、①治験環境の整備・拡充、②グローバルヘルス分野の人材強化が求められている。
○ こうしたことから、令和6年度からは新たに、迅速な大規模試験の立ち上げを可能とする基盤の充実と諸外国との人的ネットワーク構築に資する人材育成を行う。
※令和5年8月現在、全国で15病院が承認されている。
2 事業の概要・スキーム
国立研究開発法人日本医療研究開発機構(AMED)
臨床研究中核病院
(i)国際共同臨床研究実施推進プログラム
海外対応可能な人材の育成・配置や、国際共同治験を実施する者に対する支援を行うとともに、国際共同治験の推進に資するノウハウの共有を行う。
令和6年度からは新たに国際共同臨床試験実施国・機関との強い関係を築き、交渉力を高め、試験を主導していけるような、グローバルヘルス人材の育成を推進していくために、欧米等で先端的な臨
床試験を実施する医療機関等への人材派遣等を実施する。
(ii)医療系ベンチャー支援プログラム
企業導出戦略等の立案や臨床研究中核病院の資源を生かした共同研究等の提案を行える産学連携の中心となるような人材の配備等を行い、ベンチャー企業の開発を促進するとともに、各拠点で得られた
知見の共有を行う。
(iii)未承認医薬品等臨床研究安全性確保支援プログラム
CRCやDM等の雇用や、海外からの関連情報収集等のほか、自施設内の診療情報の標準化及びその運用体制の整備、自施設内のHISから統合解析のための出力までの適切なコード化までの整備を進め
ることで、自施設内で実施される臨床研究の安全性向上の一層の推進を図るとともに、各臨床研究中核病院の医療情報の連結及び当該ネットワークを活用した先進的な治験実施手法の実装を促進する。
(iv)特定領域研究開発支援プログラム
小児領域等、研究開発が困難とされる分野における開発支援の基盤構築を通じて、知見を他拠点へ展開することにより、アンメットメディカルニーズに対する医薬品等の開発を国内で幅広く実施できることを目
指す。
3 実施主体等
4 事業実績
◆補助先:国立研究開発法人日本医療研究開発機構 ◆補助率10/10 ◆対象経費 :人件費、旅費等
◆事業実績:臨床研究中核病院実施数 14機関(令和5年度)
19