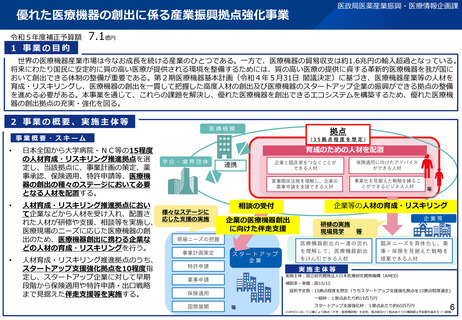
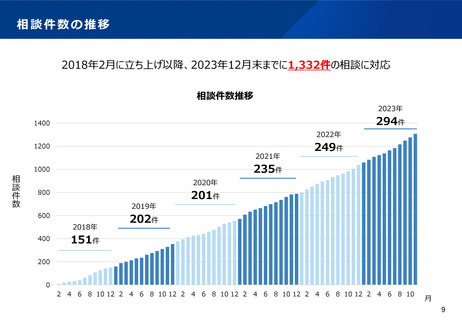
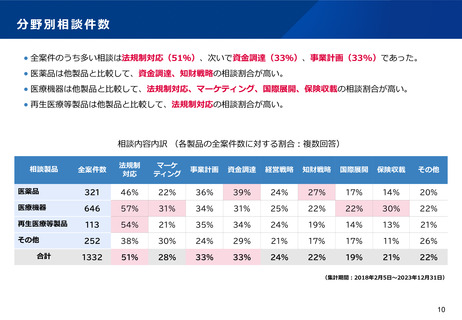
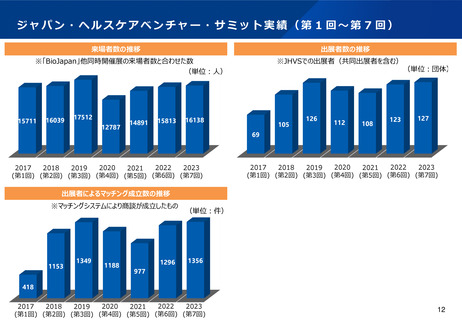
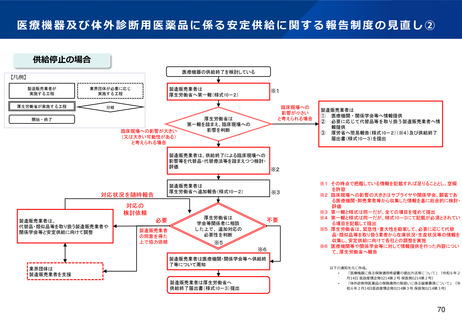
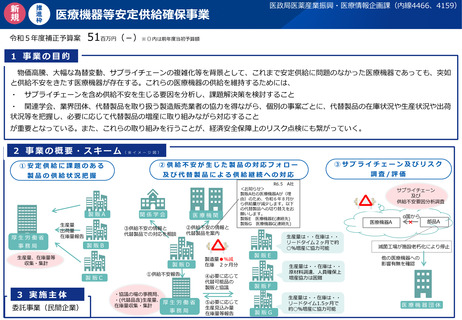
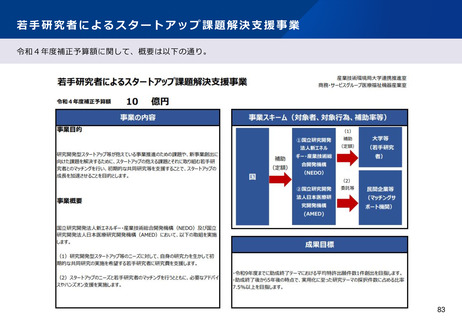
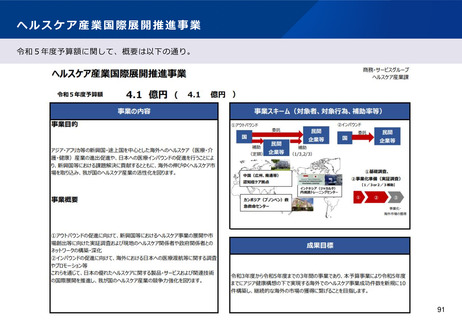
資料2-1 医療機器基本計画に関する各省における取り組みの状況について (51 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38515.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第4回 3/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
MDSAP参加国(日本、米国、カナダ、オーストラリア、ブラジル)が、QMS調査(医療機器の品質管理
に関する調査)を行うMDSAP調査機関を共同で評価・認定し、その質を一定程度に担保するとともに、
MDSAP認証機関が実施したQMS調査結果(MDSAP調査報告書)の各国での活用を目指す。
6.データのレビュー
MDSAP加盟国
MDSAP電子システム
1.認定申請
2.評価、認定
MDSAP調査機関
5. MDSAP調査結果
データアップロード
3. MDSAP調査申請
4. MDSAP調査
MDSAP報告書の発行
製造業者
MDSAP報告書を各国のQMS調査で活用。
日本では、H28.6~試行、R4.4~本格運用。
51
MDSAP = Medical Device Single Audit Program (医療機器単一調査プログラム)