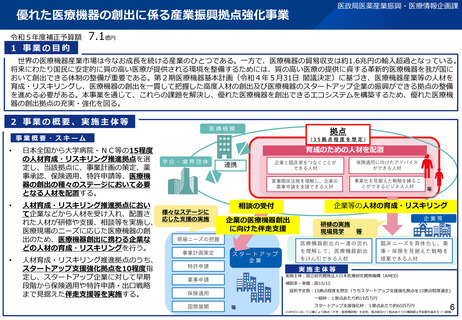
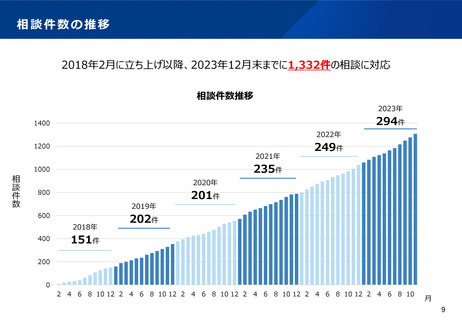
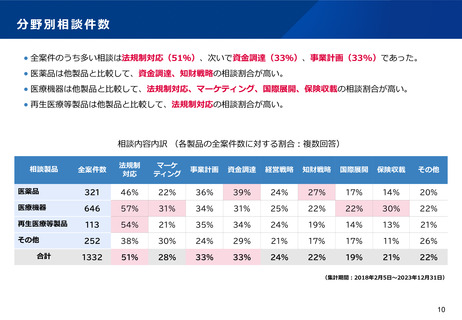
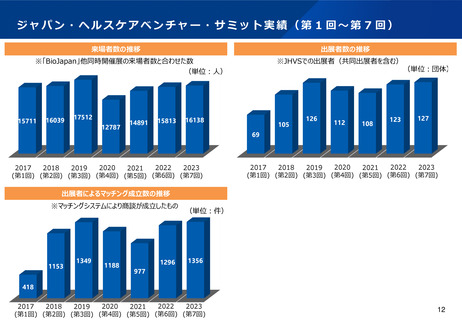
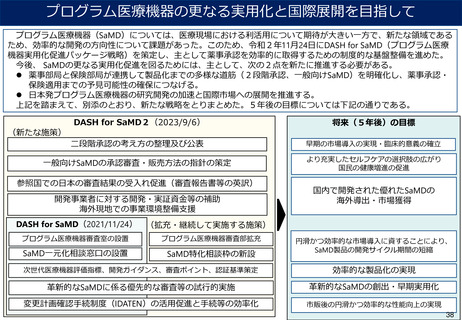
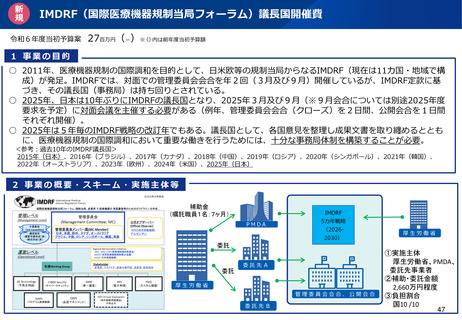
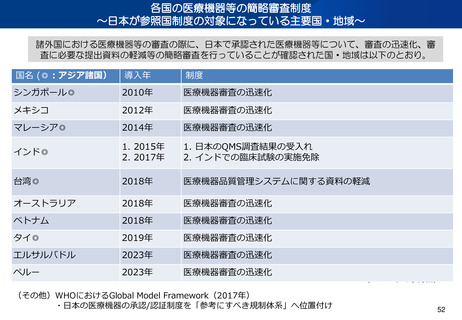
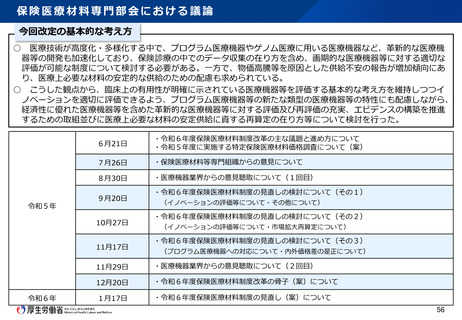
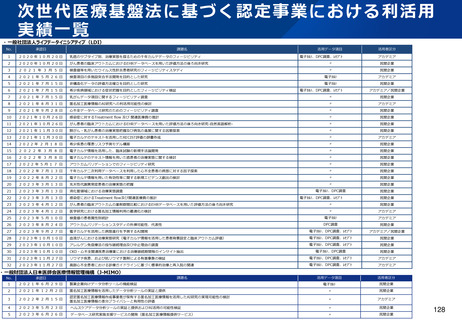
資料2-1 医療機器基本計画に関する各省における取り組みの状況について (45 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38515.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第4回 3/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(国際医療機器規制当局フォーラム: International Medical Device Regulators Forum)
◼ 2011年創設
◼ GHTF(※)の活動を基盤として、医療機器の開発、製造、販売がグ
ローバル化する中、11か国・地域の医療機器規制当局による国際調
和を促進するためのボランタリーな枠組み
※ GHTF…Global Harmonization Task Force 医療機器規制国際整合化会議
◼ IMDRFでの活動を通して、画期的・革新的な医療機器への患者アクセ
スの迅速化や適時適切な安全対策の措置等が可能になることを期待
◼ IMDRFは、安全で効果的な医療機器を世界中で利用可能にするという
共通の目標を掲げる地域組織やその他国際的な団体とも協力関係の
維持に努める
メンバー:日本、米国、EU、カナダ、オーストラリア、ブラジル、中国、ロシア、シンガポール、韓国、英国
公式オブザーバー:WHO、アルゼンチン、スイス
アフィリエイトメンバー:南アフリカ、台湾、キューバ、エジプト、イスラエル、チリ、モンテネグロ
45