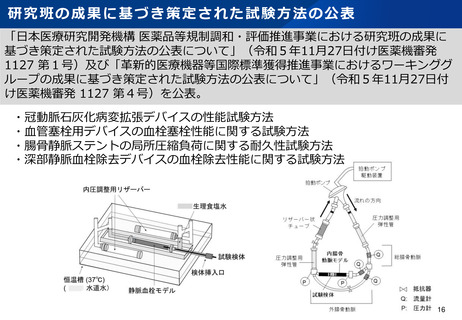
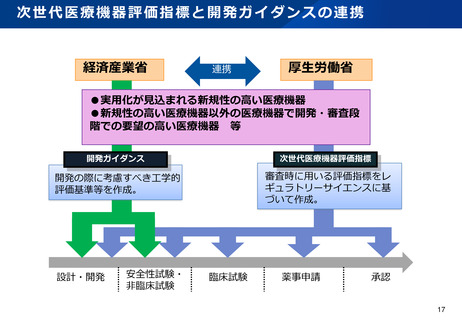
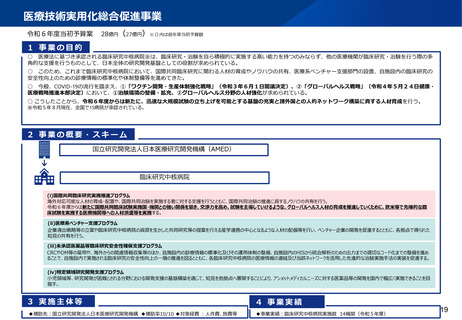
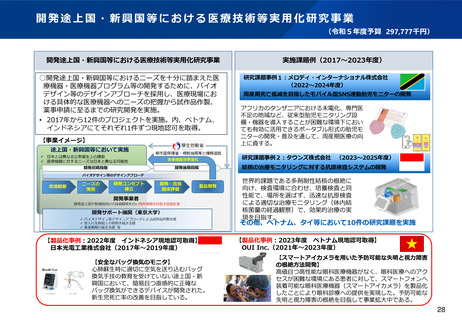
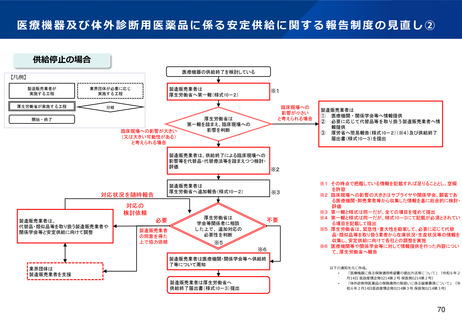
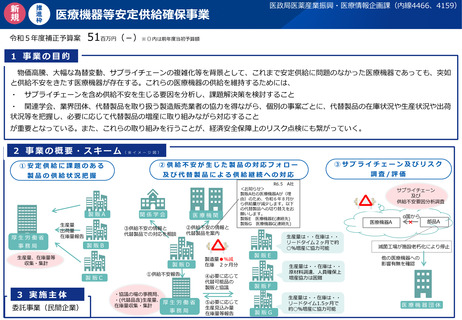
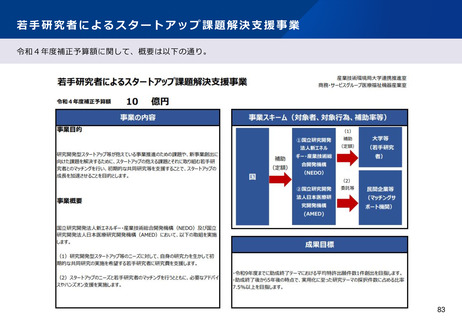
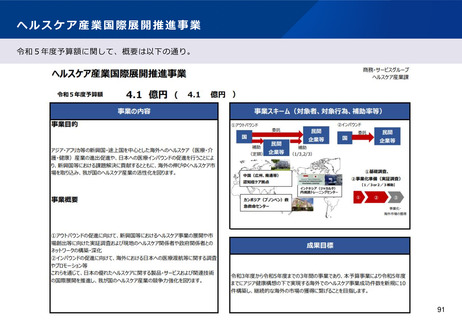
資料2-1 医療機器基本計画に関する各省における取り組みの状況について (59 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38515.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第4回 3/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
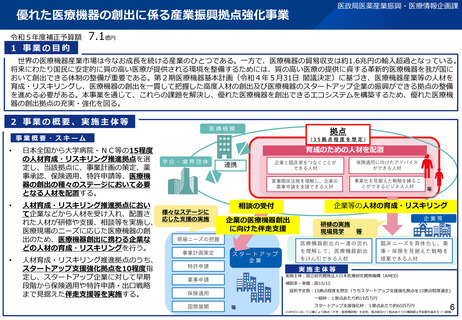
再製造単回使用医療機器使用加算の新設
➢ 再製造単回使用医療機器の使用を推進する観点から、再製造単回使用医療機器の使用に係る実績を有する医療機
関において、再製造単回使用医療機器である特定保険医療材料を手術に使用した場合の加算を新設する。
(新)
再製造単回使用医療機器使用加算
[算定要件]
別に厚生労働大臣が定める施設基準に適合しているものとして地方厚生局長等に届け出た保険医療機関において、再製造単回使用医療
機器(特定保険医療材料に限る。)を手術に使用した場合に、再製造単回使用医療機器使用加算として当該特定保険医療材料の所定点
数の100分の10に相当する点数を当該手術の所定点数に加算する。
[施設基準]
• 再製造単回使用医療機器(特定保険医療材料に限る。)を手術に使用した実績が5例以上あること。
• 再製造単回使用医療機器を使用することについて、あらかじめ文書を用いて患者に説明を行っていること。
• 再製造単回使用医療機器の原型医療機器の回収等について、再製造単回使用医療機器基準(平成 29 年厚生労働省告示第 261 号)第
4の1(5)に規定する「再製造単回使用医療機器の製造販売の承認の際に交付される承認書に記載された方法」に基づき、適切に
実施していること。
再製造SUDに関する仕組み
製造販売業者
管理
医療機関
使用済みSUD
を収集
製造業者
再製造SUDの品質、製造管理等の基準を新設
使用済みSUDを分解
PMDAによる定期的な確認(概ね年1回)
洗浄・一次滅菌 部
品
交
換
・
再
組
立
て
最
終
滅
菌
出
荷
判
定
出荷
医療機関
トレーサビリティの確保
59