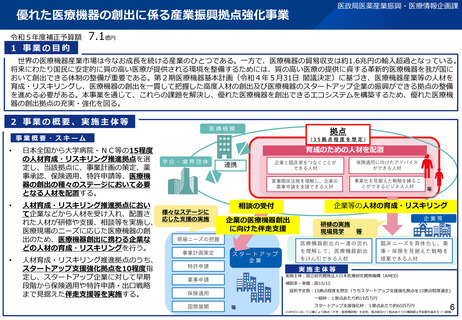
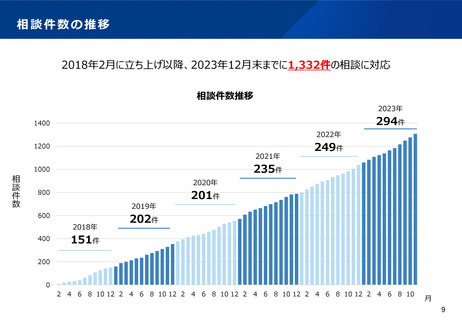
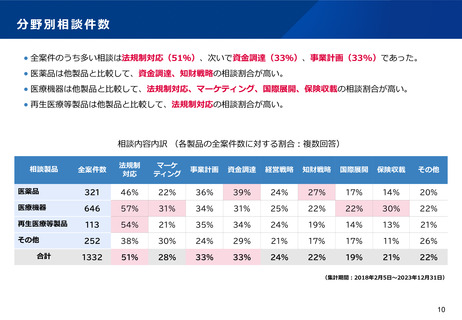
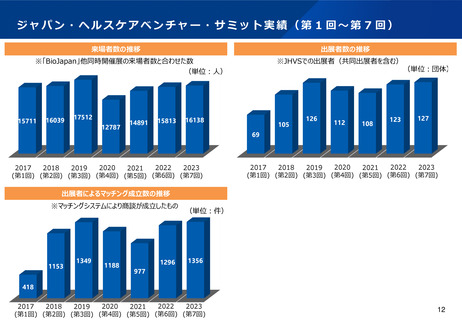
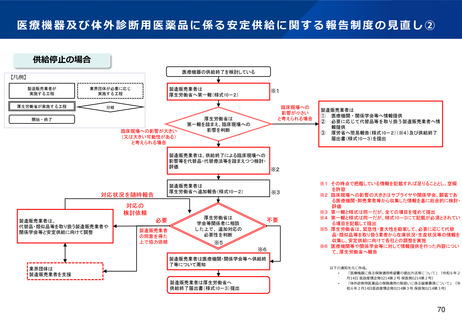
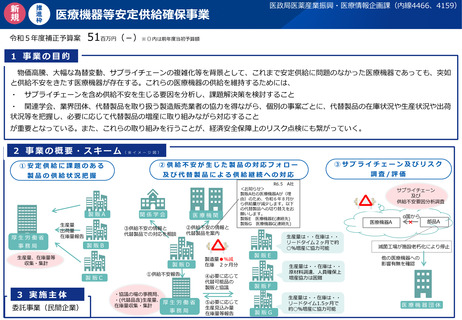
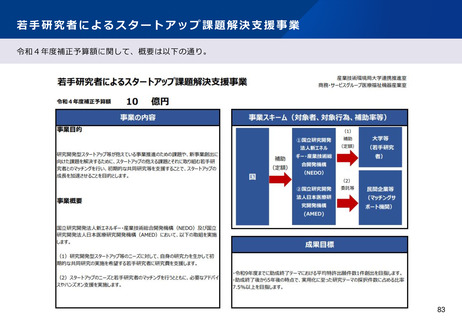
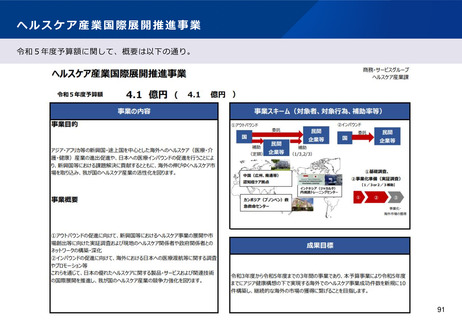
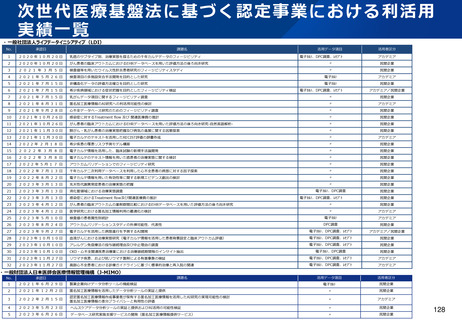
資料2-1 医療機器基本計画に関する各省における取り組みの状況について (40 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38515.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第4回 3/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
実施項目①
1.萌芽的シーズの早期把握と審査の考え方の公表
実施項目
(1)
萌芽的シーズに対する製品ライフサイクルを踏ま
えた相談の実施
① プログラム医療機器の開発及び薬事承認に必要な情報に関する動画をPMDAのホームページや
YouTube等を通じて発信する。
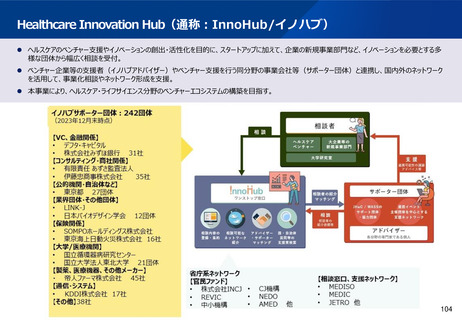
② PMDAがその他の相談事業(MEDISO、MEDIC、InnoHub等)と積極的に連携し、相談事業の
支援策等の効率化を図る。
③ スタートアップ企業と既存企業との連携を支援する。
(2)
医療機器開発等に資するガイドライン等の策定・
公表
① プログラム医療機器に係る次世代医療機器評価指標を策定する。
② プログラム医療機器に係る開発ガイダンスを策定する。
③ プログラム医療機器に係る審査のポイント及び認証基準等について、業界の要望等を踏まえて
策定する。
(3)
家庭(一般)向けSaMDの承認審査の考え方(医
療現場向けSaMDからの転用を含む)の整理・公
表
一般消費者を対象とした使用目的及び仕様等に対応させた家庭向けプログラム医療機器の薬事承認
申請の考え方について、医療現場向けプログラム医療機器の申請資料等の活用を含めた薬事承認の
あり方を整理・公表する。
2.SaMDの特性(※)を踏まえた実用化促進
実施項目
(1)
二段階承認の考え方の整理及び公表・承認事例の
公表
① プログラム医療機器に係る二段階承認の考え方を整理・公表する。
② 薬事承認におけるリアル・ワールドデータの利活用及び評価データの信頼性を確保する要件等
の課題を整理する。
(2)
変更計画確認手続制度(IDATEN)の活用促進と
手続等の効率化
プログラム医療機器の変更計画確認手続制度(IDATEN)の活用促進と手続等の効率化するため、
必要な申請書及び添付資料等の具体的な記載例を公表するとともに、質疑応答集を充実化させる。
(3)
革新的なSaMDに係る優先的な審査等の試行的実
施
① プログラム医療機器に係る優先的な審査等を試行的に実施する。
② 指定品目のうち、一定条件の中小企業等の要件を満たす企業に、当該要件を満たす品目に係る
相談手数料及び審査・調査手数料の全額納付後に5割を助成する「革新的医療機器等相談承認
申請支援事業」を実施する。
(4)
医療現場向け・家庭(一般)向けSaMDの販売方
法に関する明確化のための指針等の策定
医療現場向けプログラム医療機器と家庭(一般)向けプログラム医療機器の販売方法に関する明確
化に関する指針や考え方を検討する。
(5)
改良医療機器に関する審査報告書の作成・公表
プログラム医療機器に関して、新医療機器の審査報告書を公表しているが、改良医療機器の審査報
告書についても作成・公表を行う。
(6)
開発事業者に対する開発・実証資金等の補助(海
外展開に関する開発・実証を含む)
プログラム医療機器の国内外における開発及び実証に係る資金等を支援する。
(※)プログラム医療機器は有体物の医療機器よりも侵襲性が低いのでリスクが相対的に低く、また、市販後に性能等の改良・アップデートが頻繁かつ継続的に行われる。
40