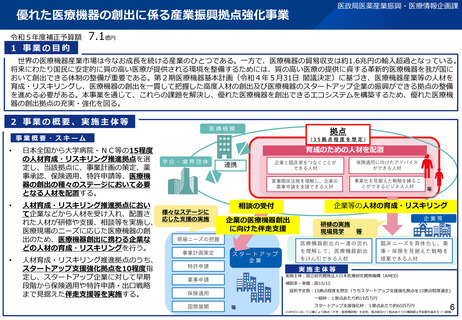
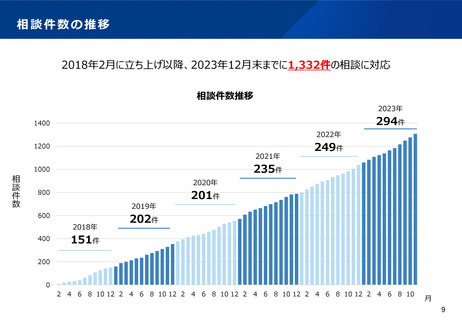
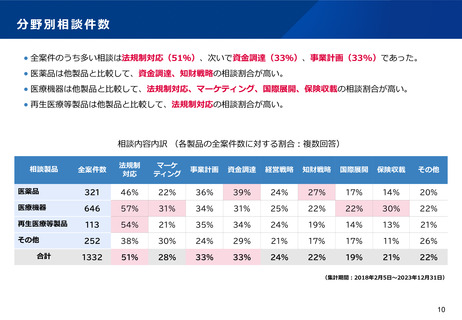
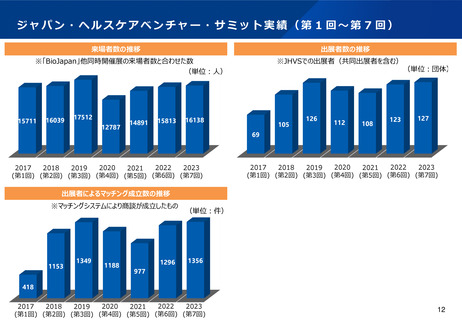
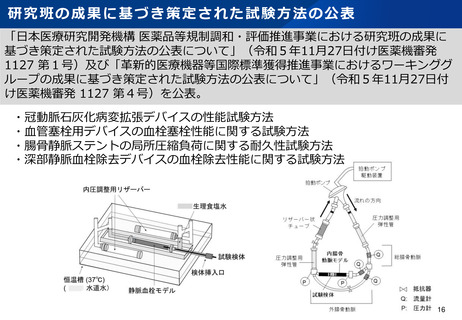
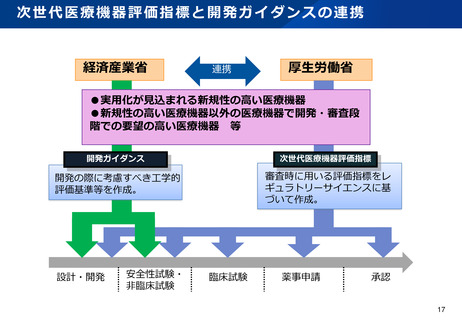
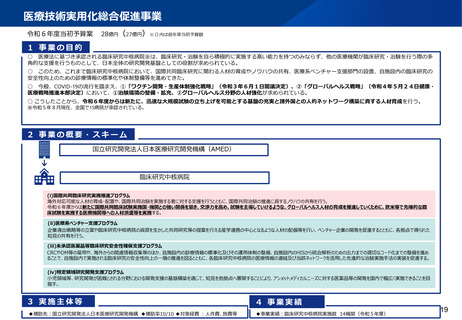
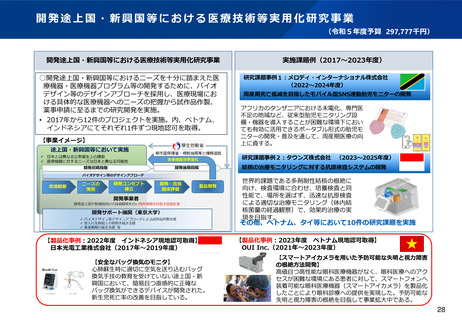
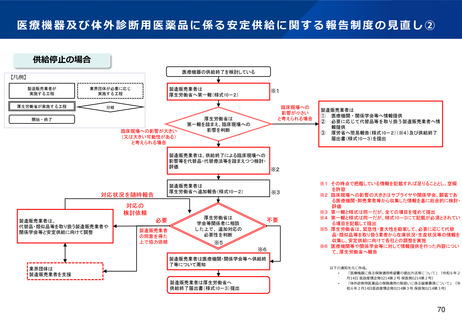
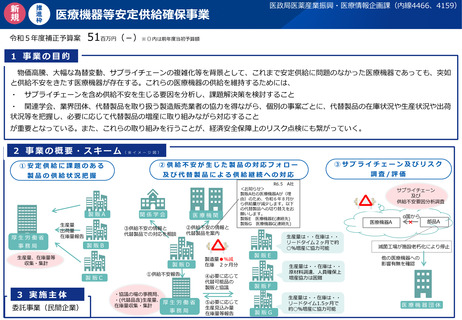
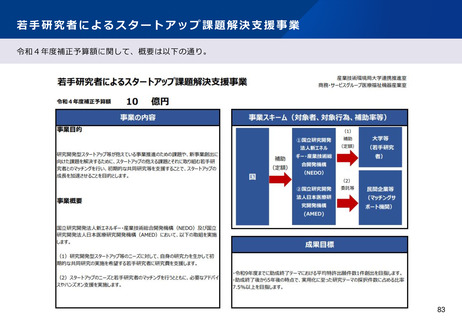
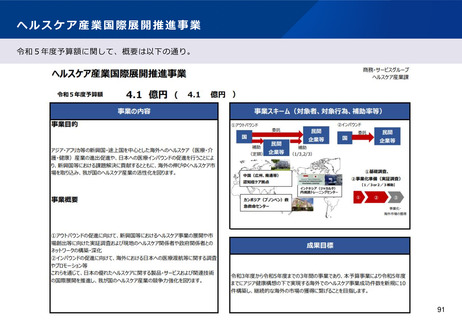
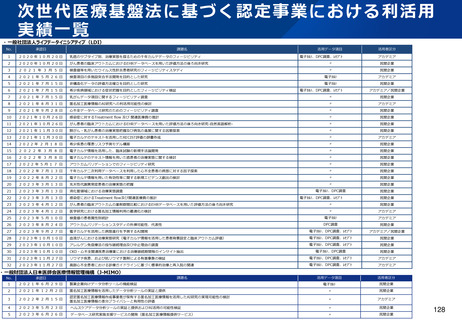
資料2-1 医療機器基本計画に関する各省における取り組みの状況について (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38515.html |
| 出典情報 | 国民が受ける医療の質の向上のための医療機器の研究開発及び普及の促進に関する検討会(第4回 3/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
管理レベル
公式オブザーバー
(Official Observer)
WHO(世界保健機関)、
アルゼンチン、スイス
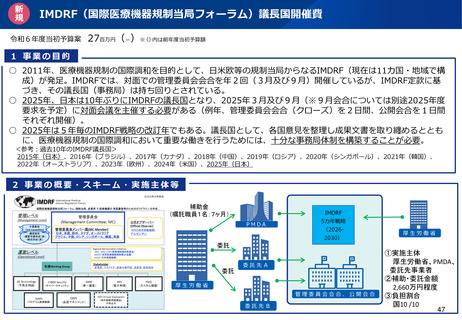
管理委員会
(Management Level)
(Management Committee; MC)
小委員会
(Sub Committee)
適宜設定
・運営手順作成
・様式作成
管理委員会メンバー国(MC Member)
日本、米国、欧州、 カナダ、豪州、英国
ブラジル、中国、ロシア、シンガポール、韓国
運営レベル
Regional Harmonization Initiatives
会合参加:Opt in/Opt out
成果受容:自発判断
意思決定:コンセンサス方式
(Operational Level)
各種Working Group
アフィリエイトメンバー
(Affiliate Member)
南アフリカ、台湾、キューバ、エジ
プト、イスラエル、チリ、モンテネグロ
APEC RHSC(APEC薬事規制調和委員会)
GHWP(世界医療機器規制整合会議)
PAHO(汎米保健機構)
AMDF(アフリカ医療機器フォーラム)
Stakeholder
産業界、アカデミア、医療の専門家、消費者・患者団体
AE Terminology
(不具合用語)
AI-ML
(人工知能・機械学習)
RPS
(電子申請)
GRRP
(単一審査)
SaMD
(プログラム医療機器)
PMD
(カスタム機器)
QMS
(品質管理)
IVD Clinical Evaluation
(体外診断用医薬品)
※休止中
46