よむ、つかう、まなぶ。
参考資料4-4 特例承認医薬品の市販直後調査報告書 (33 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29975.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第22回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
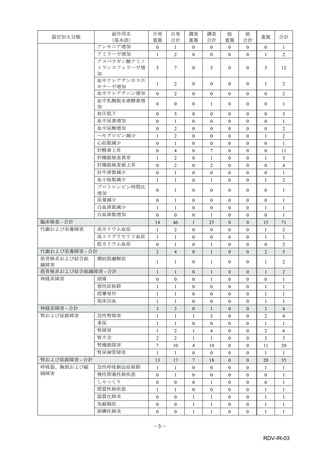
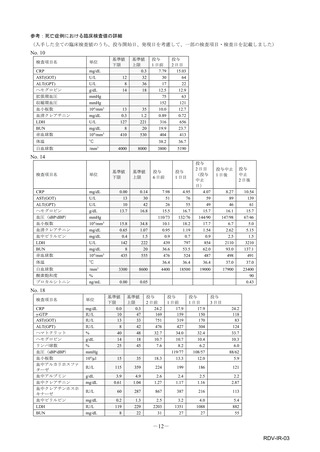
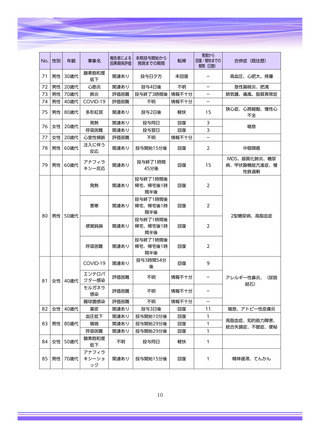
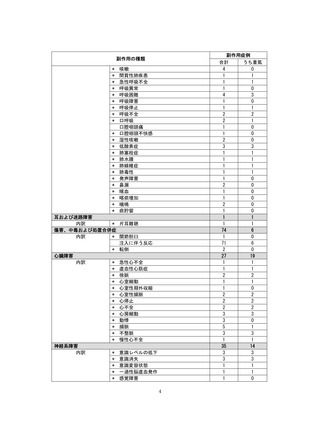
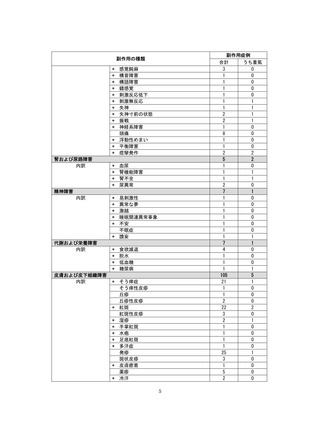
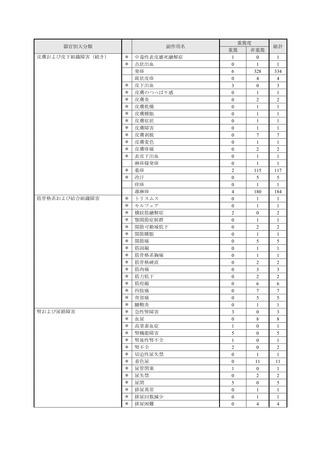
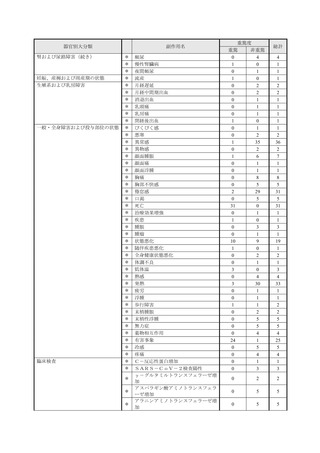
重篤性
副作用名
計
重篤
非重篤
* 血圧低下
4
6
10
* 血圧上昇
2
2
4
* 収縮期血圧低下
1
0
1
* 心拍数増加
* 酸素飽和度低下
* 白血球数減少
傷害、中毒および処置合併症
注入に伴う反応
外科および内科処置
* 入院
†
※
総計
0
1
1
26
4
30
1
0
1
11
26
37
11
26
37
2
0
2
2
0
2
120
491
611
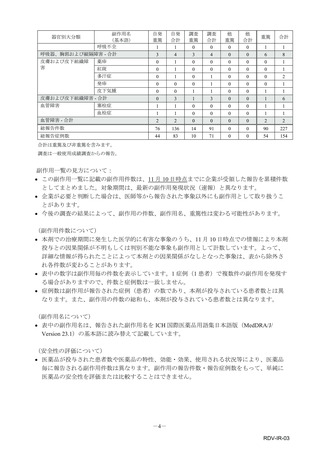
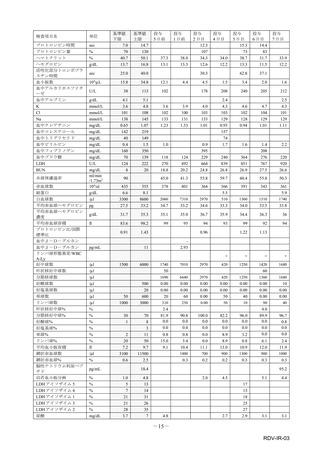
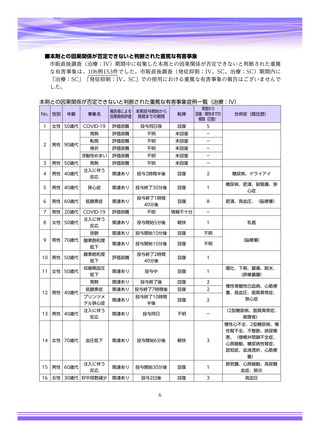
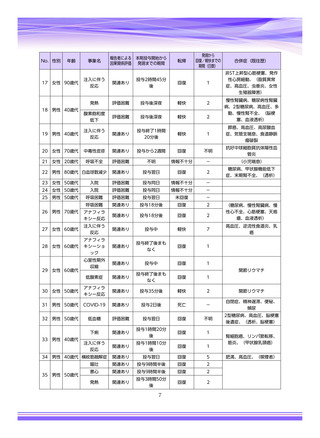
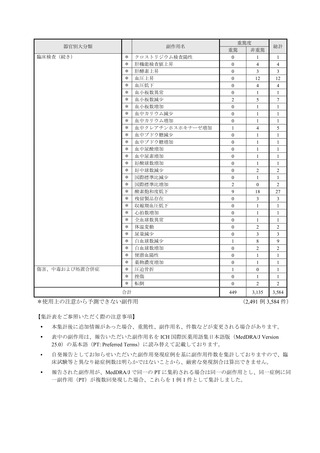
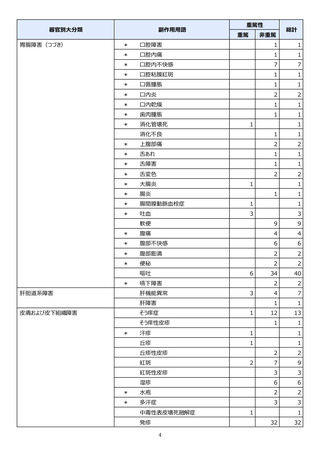
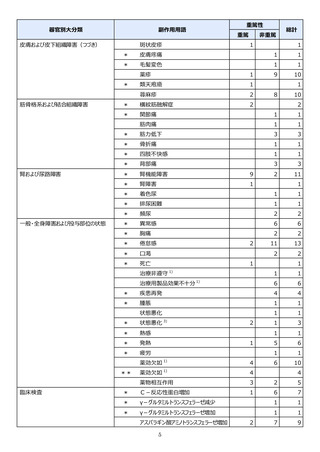
本件数表は、本剤との因果関係が否定できないと判断された有害事象の件数を集計したものです。1症例(1患者)で複数件の事象が報
告される場合があるため、件数と症例数(患者数)は一致しません。
電子化された添付文書の「11.副作用」から予測できない副作用に*をつけています。
■適正使用のお願い
本剤をご使用いただく際には、引き続き最新の電子化された添付文書、医薬品リスク管理計画書
(RMP)、適正使用ガイド等をご確認くださいますよう、お願い申し上げます。本剤の資材は弊
社医療関係者向けウェブサイトに掲載しております。
https://chugai-pharm.jp/product/ron/div/
市販直後調査集計結果について、以下の点をご留意ください。
① 市販直後調査で収集される副作用は、医療関係者の皆様等から自発的に弊社へご報告を頂いてお
り、必ずしも実際に発生した全ての副作用を網羅しているものではないため、副作用の発現頻度
を算出することはできません。
② 市販直後調査で収集される副作用は薬剤の投与期間が限定的(最大で6カ月)であることから、
投与開始から発現時期が早い副作用が中心であり、長期投与時における副作用は収集されにくい
傾向にあります。
15
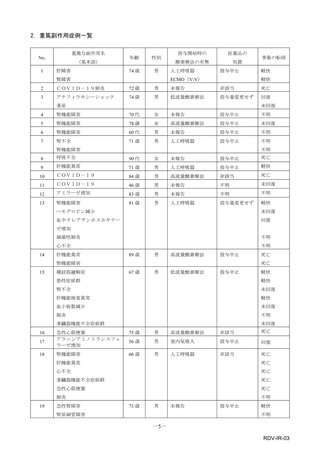
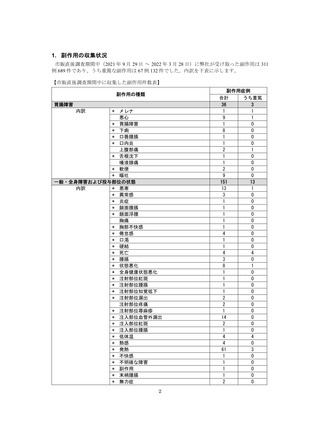
副作用名
計
重篤
非重篤
* 血圧低下
4
6
10
* 血圧上昇
2
2
4
* 収縮期血圧低下
1
0
1
* 心拍数増加
* 酸素飽和度低下
* 白血球数減少
傷害、中毒および処置合併症
注入に伴う反応
外科および内科処置
* 入院
†
※
総計
0
1
1
26
4
30
1
0
1
11
26
37
11
26
37
2
0
2
2
0
2
120
491
611
本件数表は、本剤との因果関係が否定できないと判断された有害事象の件数を集計したものです。1症例(1患者)で複数件の事象が報
告される場合があるため、件数と症例数(患者数)は一致しません。
電子化された添付文書の「11.副作用」から予測できない副作用に*をつけています。
■適正使用のお願い
本剤をご使用いただく際には、引き続き最新の電子化された添付文書、医薬品リスク管理計画書
(RMP)、適正使用ガイド等をご確認くださいますよう、お願い申し上げます。本剤の資材は弊
社医療関係者向けウェブサイトに掲載しております。
https://chugai-pharm.jp/product/ron/div/
市販直後調査集計結果について、以下の点をご留意ください。
① 市販直後調査で収集される副作用は、医療関係者の皆様等から自発的に弊社へご報告を頂いてお
り、必ずしも実際に発生した全ての副作用を網羅しているものではないため、副作用の発現頻度
を算出することはできません。
② 市販直後調査で収集される副作用は薬剤の投与期間が限定的(最大で6カ月)であることから、
投与開始から発現時期が早い副作用が中心であり、長期投与時における副作用は収集されにくい
傾向にあります。
15