よむ、つかう、まなぶ。
参考資料4-4 特例承認医薬品の市販直後調査報告書 (42 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29975.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第22回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
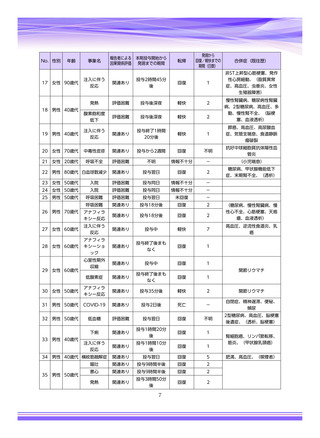
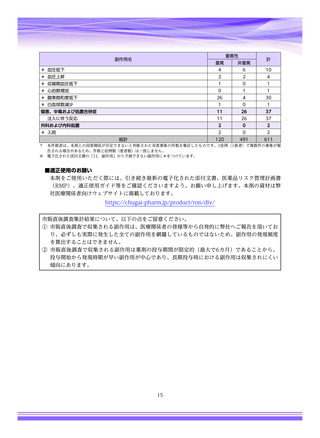
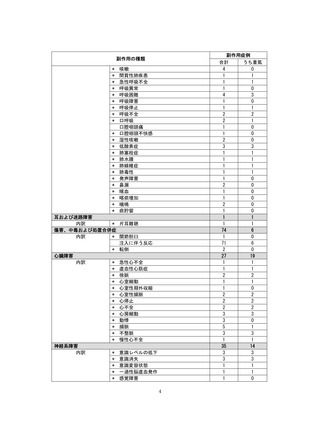
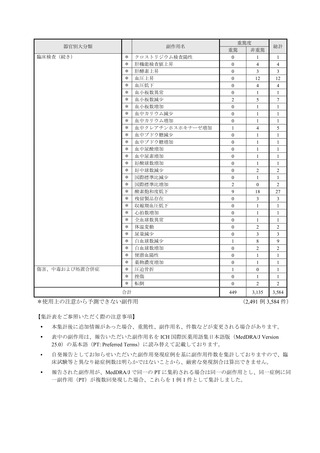
3. 本剤の医薬品リスク管理計画(RMP)
本剤のRMPにおいて、下表のとおり安全性検討事項を設定し、注意喚起を行っております。
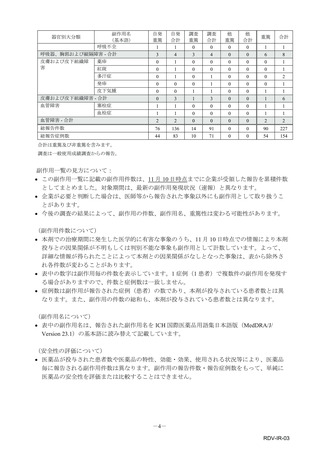
【安全性検討事項】
安全性検討事項
重要な特定されたリスク
重要な潜在的リスク
重要な不足情報
アナフィラキシー等の重篤
な過敏症、Infusion Reaction
該当なし
該当なし
2022年4月提出版より
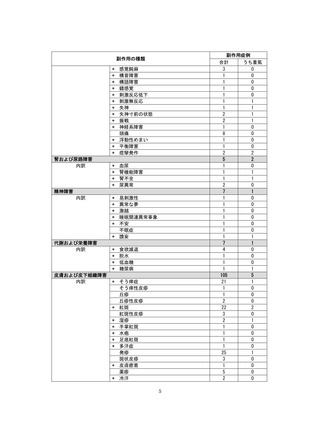
4. まとめ
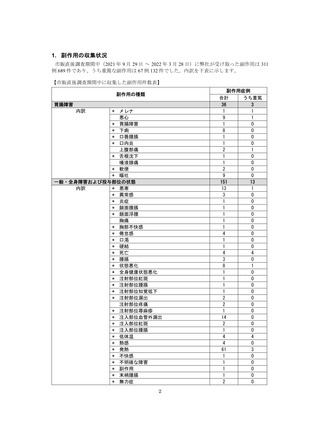
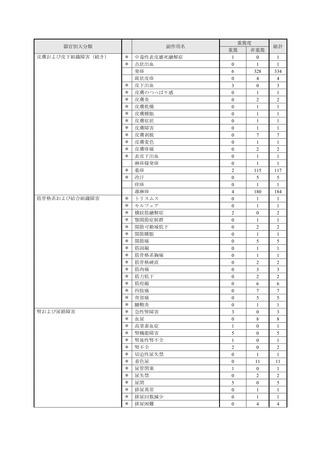
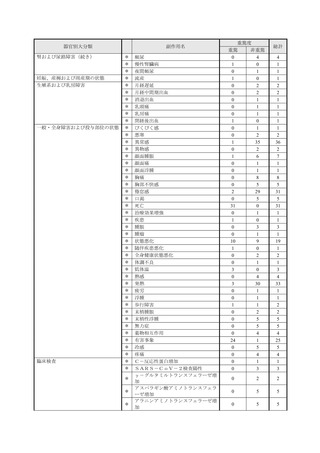
市販直後調査期間中、本剤による副作用は 311 例 689 件報告され、これらのうち、重篤例は 67
例 132 件でした。本剤の安全性プロファイルに影響を及ぼす新たな所見は認められず、本市販直
後調査の結果をもって、使用上の注意改訂等の安全確保措置を実施する必要はないと判断しまし
た。
「市販直後調査」終了時点では認められなかった使用上の注意から予測できない副作用が今後
発現することも考えられるため、引き続き安全性情報の収集・評価に努め、必要に応じて本剤の
適正使用につながる情報提供を行う所存でございます。
なお、本剤ご使用にあたっては、弊社医療関係者向け情報サイト『GSKpro』より、電子添文、
医薬品リスク管理計画等、最新の薬剤情報をご確認頂きますようお願い致します。
また、厚生労働省のホームページに掲載の「新型コロナ ウイルス感染症(COVID-19)診療の
手引き」など最新の知見も併せてご確認の上、適切な患者様へご使用いただきますよう引き続き
よろしくお願い申し上げます。
【GSKpro ゼビュディ製品ページ】
https://gskpro.com/ja-jp/products-info/xevudy/
【厚生労働省ホームページ】
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000121431_00111.html
以上
以上
〒107-0052 東京都港区赤坂 1−8−1
http://jp.gsk.com
PI-10191-
D2207N
作成年月 2022 年 7 月
PI-10191- D2207N
作成年月 2022 年 7 月
8
三校 _2022 年 7 月 4 日
本剤のRMPにおいて、下表のとおり安全性検討事項を設定し、注意喚起を行っております。
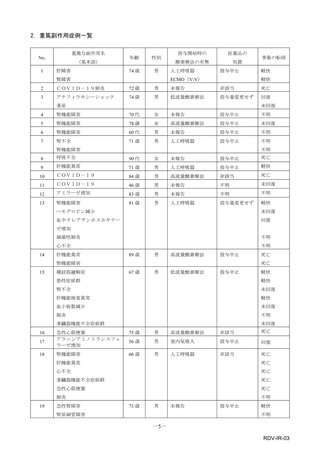
【安全性検討事項】
安全性検討事項
重要な特定されたリスク
重要な潜在的リスク
重要な不足情報
アナフィラキシー等の重篤
な過敏症、Infusion Reaction
該当なし
該当なし
2022年4月提出版より
4. まとめ
市販直後調査期間中、本剤による副作用は 311 例 689 件報告され、これらのうち、重篤例は 67
例 132 件でした。本剤の安全性プロファイルに影響を及ぼす新たな所見は認められず、本市販直
後調査の結果をもって、使用上の注意改訂等の安全確保措置を実施する必要はないと判断しまし
た。
「市販直後調査」終了時点では認められなかった使用上の注意から予測できない副作用が今後
発現することも考えられるため、引き続き安全性情報の収集・評価に努め、必要に応じて本剤の
適正使用につながる情報提供を行う所存でございます。
なお、本剤ご使用にあたっては、弊社医療関係者向け情報サイト『GSKpro』より、電子添文、
医薬品リスク管理計画等、最新の薬剤情報をご確認頂きますようお願い致します。
また、厚生労働省のホームページに掲載の「新型コロナ ウイルス感染症(COVID-19)診療の
手引き」など最新の知見も併せてご確認の上、適切な患者様へご使用いただきますよう引き続き
よろしくお願い申し上げます。
【GSKpro ゼビュディ製品ページ】
https://gskpro.com/ja-jp/products-info/xevudy/
【厚生労働省ホームページ】
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/0000121431_00111.html
以上
以上
〒107-0052 東京都港区赤坂 1−8−1
http://jp.gsk.com
PI-10191-
D2207N
作成年月 2022 年 7 月
PI-10191- D2207N
作成年月 2022 年 7 月
8
三校 _2022 年 7 月 4 日