よむ、つかう、まなぶ。
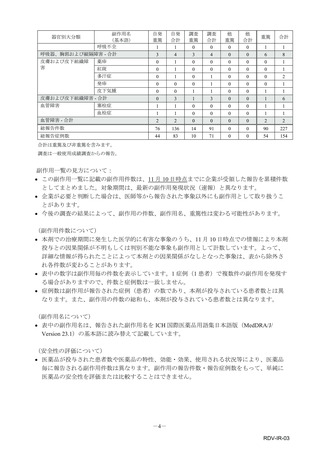
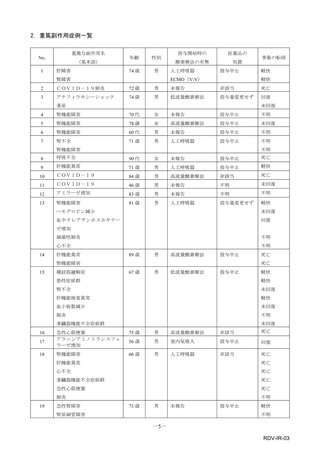
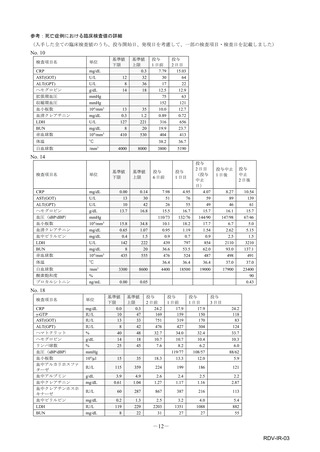
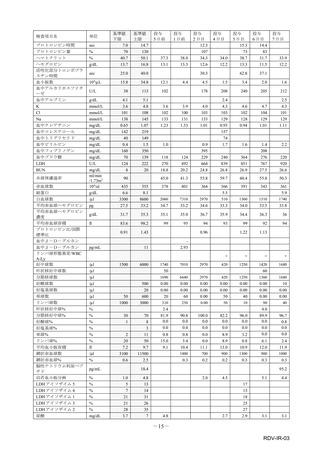
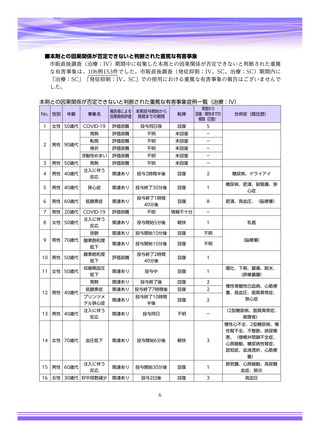
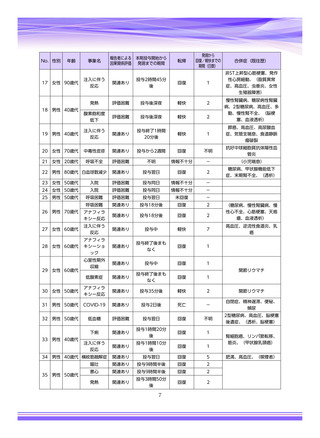
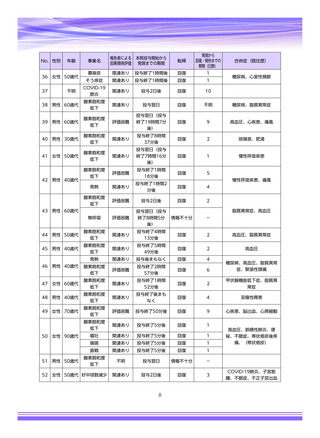
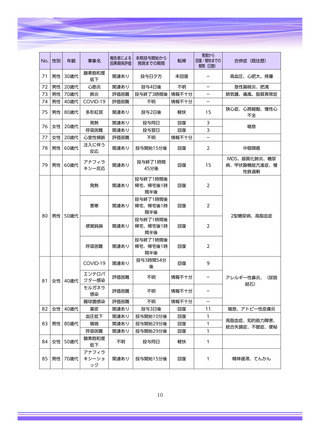
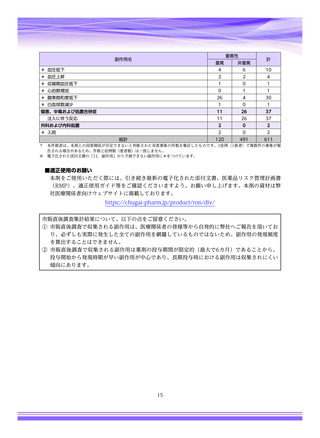
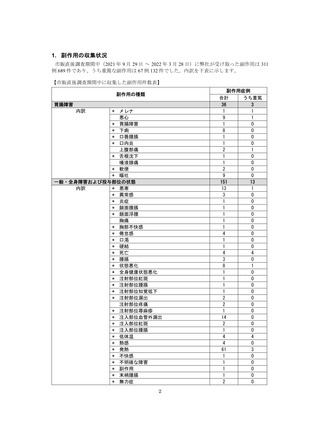
参考資料4-4 特例承認医薬品の市販直後調査報告書 (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29975.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第22回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
自発
重篤
1
自発
合計
1
調査
重篤
0
調査
合計
0
他
重篤
0
他
合計
0
呼吸器、胸郭および縦隔障害 - 合計
3
4
3
4
0
皮膚および皮下組織障
害
薬疹
0
1
0
0
0
紅斑
0
1
0
0
多汗症
0
1
0
1
発疹
0
0
0
皮下気腫
器官別大分類
副作用名
(基本語)
呼吸不全
重篤
合計
1
1
0
6
8
0
0
1
0
0
0
1
0
0
0
2
1
0
0
0
1
0
0
1
1
0
0
1
1
皮膚および皮下組織障害 - 合計
0
3
1
3
0
0
1
6
血管障害
塞栓症
1
1
0
0
0
0
1
1
血栓症
1
1
0
0
0
0
1
1
血管障害 - 合計
2
2
0
0
0
0
2
2
総報告件数
76
136
14
91
0
0
90
227
総報告症例数
44
83
10
71
0
0
54
154
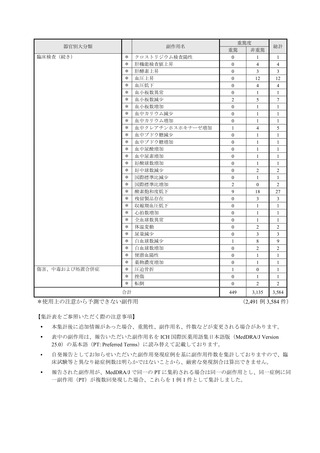
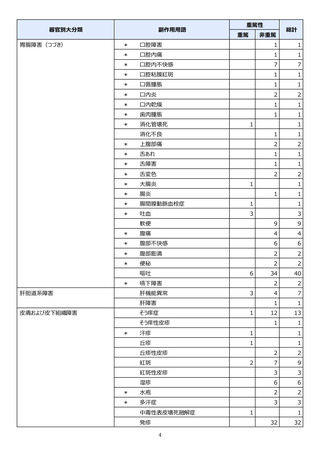
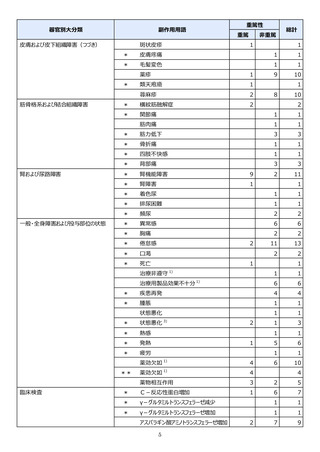
合計は重篤及び非重篤を含みます。
調査は一般使用成績調査からの報告。
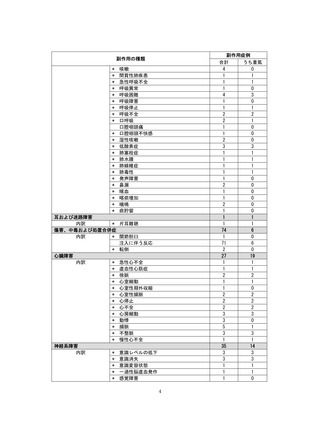
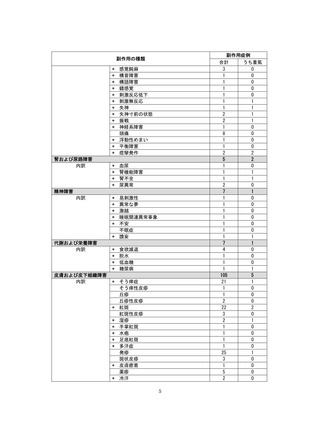
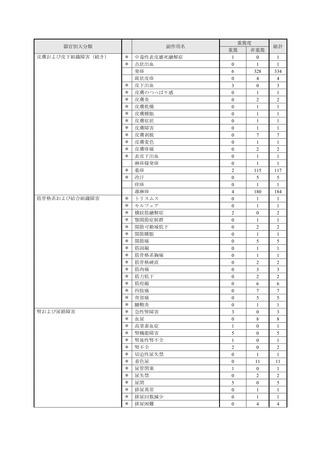
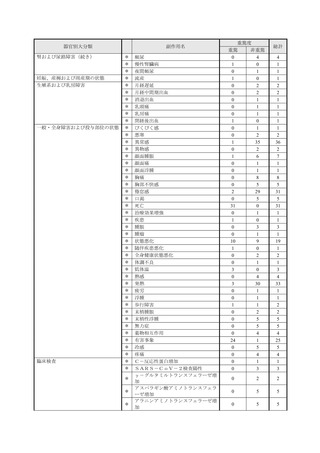
副作用一覧の見方について:
• この副作用一覧に記載の副作用件数は、11 月 10 日時点までに企業が受領した報告を累積件数
としてまとめました。対象期間は、最新の副作用発現状況(速報)と異なります。
• 企業が必要と判断した場合は、医師等から報告された事象以外にも副作用として取り扱うこ
とがあります。
• 今後の調査の結果によって、副作用の件数、副作用名、重篤性は変わる可能性があります。
(副作用件数について)
• 本剤での治療期間に発生した医学的に有害な事象のうち、11 月 10 日時点での情報により本剤
投与との因果関係が不明もしくは判別不能な事象も副作用として計数しています。よって、
詳細な情報が得られたことによって本剤との因果関係がなしとなった事象は、表から除外さ
れ各件数が変わることがあります。
• 表中の数字は副作用毎の件数を表示しています。1 症例(1 患者)で複数件の副作用を発現す
る場合がありますので、件数と症例数は一致しません。
• 症例数は副作用が報告された症例(患者)の数であり、本剤が投与されている患者数とは異
なります。また、副作用の件数の総和も、本剤が投与されている患者数とは異なります。
(副作用名について)
• 表中の副作用名は、報告された副作用名を ICH 国際医薬品用語集日本語版(MedDRA/J/
Version 23.1)の基本語に読み替えて記載しています。
(安全性の評価について)
• 医薬品が投与された患者数や医薬品の特性、効能・効果、使用される状況等により、医薬品
毎に報告される副作用件数は異なります。副作用の報告件数・報告症例数をもって、単純に
医薬品の安全性を評価または比較することはできません。
-4-
RDV-IR-03
重篤
1
自発
合計
1
調査
重篤
0
調査
合計
0
他
重篤
0
他
合計
0
呼吸器、胸郭および縦隔障害 - 合計
3
4
3
4
0
皮膚および皮下組織障
害
薬疹
0
1
0
0
0
紅斑
0
1
0
0
多汗症
0
1
0
1
発疹
0
0
0
皮下気腫
器官別大分類
副作用名
(基本語)
呼吸不全
重篤
合計
1
1
0
6
8
0
0
1
0
0
0
1
0
0
0
2
1
0
0
0
1
0
0
1
1
0
0
1
1
皮膚および皮下組織障害 - 合計
0
3
1
3
0
0
1
6
血管障害
塞栓症
1
1
0
0
0
0
1
1
血栓症
1
1
0
0
0
0
1
1
血管障害 - 合計
2
2
0
0
0
0
2
2
総報告件数
76
136
14
91
0
0
90
227
総報告症例数
44
83
10
71
0
0
54
154
合計は重篤及び非重篤を含みます。
調査は一般使用成績調査からの報告。
副作用一覧の見方について:
• この副作用一覧に記載の副作用件数は、11 月 10 日時点までに企業が受領した報告を累積件数
としてまとめました。対象期間は、最新の副作用発現状況(速報)と異なります。
• 企業が必要と判断した場合は、医師等から報告された事象以外にも副作用として取り扱うこ
とがあります。
• 今後の調査の結果によって、副作用の件数、副作用名、重篤性は変わる可能性があります。
(副作用件数について)
• 本剤での治療期間に発生した医学的に有害な事象のうち、11 月 10 日時点での情報により本剤
投与との因果関係が不明もしくは判別不能な事象も副作用として計数しています。よって、
詳細な情報が得られたことによって本剤との因果関係がなしとなった事象は、表から除外さ
れ各件数が変わることがあります。
• 表中の数字は副作用毎の件数を表示しています。1 症例(1 患者)で複数件の副作用を発現す
る場合がありますので、件数と症例数は一致しません。
• 症例数は副作用が報告された症例(患者)の数であり、本剤が投与されている患者数とは異
なります。また、副作用の件数の総和も、本剤が投与されている患者数とは異なります。
(副作用名について)
• 表中の副作用名は、報告された副作用名を ICH 国際医薬品用語集日本語版(MedDRA/J/
Version 23.1)の基本語に読み替えて記載しています。
(安全性の評価について)
• 医薬品が投与された患者数や医薬品の特性、効能・効果、使用される状況等により、医薬品
毎に報告される副作用件数は異なります。副作用の報告件数・報告症例数をもって、単純に
医薬品の安全性を評価または比較することはできません。
-4-
RDV-IR-03