よむ、つかう、まなぶ。
資料3-1 リツキシマブ(遺伝子組換え) (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
ースラインより 15%を超えて上昇していない場合とし、PR は、Upr/Ucr が 300 mg/mmol 未満
(ネフローゼ症候群を呈さない)でベースラインから 50%を超えて減少し、かつ血清クレア
チニン値がベースラインより 15%を超えて上昇しない場合とした。
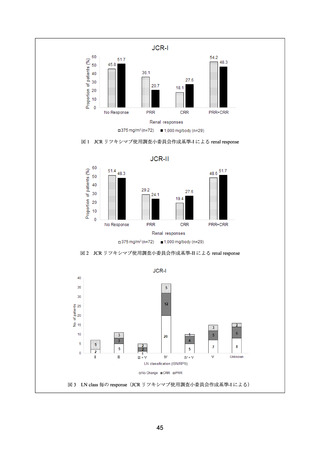
活動性の Class IV 又は Class IV+V が 40%(20 例)
、Class V が 44%(22 例)であった。50
例中 49 例が追跡可能で、観察期間中央値は 163 週間(範囲:52~237 週間)であった。
観察期間中に CR 又は PR が認められた症例は 45/50 例(90%)であり、奏効までの期間中
央値は 37 週間(範囲:4~200 週間)であった。26 週時点までに CR は 16/50 例(32%)
、PR
は 15/50 例(30%)に認められ、1 年時点までに CR は 26/50 例(52%)
、PR は 17/50 例(34%)
に認められた。
また、11 例(22%)で 12 回の再燃が認められ、すべてネフローゼ症候群を呈した。寛解か
ら再燃までの期間中央値は 65.1 週間(範囲:20~112 週間)であり、CR 例では 7 例で 8 回、
PR 例では 4 例で 4 回の再燃が認められた。再燃した 6 例(7 回)に対して本剤 1,000 mg を 2
回再投与したところ(メチルプレドニゾロンの併用あり又は併用なし)
、CR が 3 回、PR が 1
回認められたが、3 回は無効であった。
安全性について、入院を伴う有害事象は 9/50 例(18%)に認められた。5 例は感染症であ
り、そのうち 1 例は帯状疱疹であった。本剤とメチルプレドニゾロンによる寛解導入療法後
に 1 例で 2 型糖尿病が発現した。死亡例は 2 例(4%)で、1 例(61 歳)は本剤治療 31 カ月
後に重症の末梢血管障害に対する手術の合併症により死亡した(ループス腎炎は CR)
。別の
1 例(71 歳)は、本剤初回治療 28 カ月後に自宅で突然死した。本症例は、1 年時点で PR で
あったため再生検を実施し、18 カ月時点で本剤を再投与した。死亡時もループス腎炎は PR
であった。
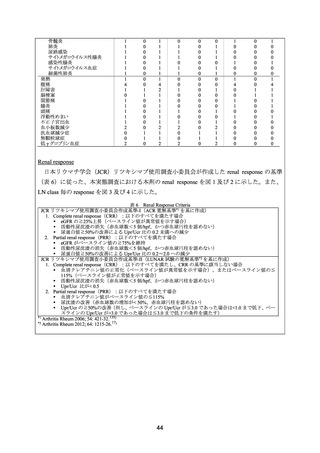
4) Tsanyan ME, et al. Clinical and morphological improvement of lupus nephritis treated with
rituximab. Folia Med 2014; 56: 245-52. 27)
ループス腎炎に対する本剤の臨床的及び形態学的な改善効果に関する報告。
ステロイド及び免疫抑制剤による標準治療に抵抗性を示すループス腎炎患者 45 例(23~36
歳)が対象とされた。WHO 分類(2003 年版)に基づく重症度分類は、Class IV が 32 例(71%)、
Class III が 8 例(18%)
、Class V 及び Class II が各 2 例(4%)
、Class I が 1 例(4%)であり、
全例でループス腎炎に関連した形態学的所見が確認された。
本剤は、500 mg を 1~4 回又は 1,000 mg を 1~2 回投与した。16 例はメチルプレドニゾロ
ン及び CY パルス療法を併用し、29 例は本剤単独投与であった。
本剤投与開始から 1 年以上後に腎生検が実施された患者は 16 例であり、フォローアップ期
間中に CR は 13 例(81.2%)、PR は 1 例(6.3%)に認められた。奏効が認められなかった 2
例のうち、1 例は本剤による治療で効果が得られず、別の 1 例では 1 年半後に再燃が認めら
れた。また、形態学的な改善は 16 例中 11 例で認められた。本剤による治療後に活動性スコ
アの改善が認められたが、慢性化スコアの改善は認められなかった。
安全性に関する記載はなし。
10
(ネフローゼ症候群を呈さない)でベースラインから 50%を超えて減少し、かつ血清クレア
チニン値がベースラインより 15%を超えて上昇しない場合とした。
活動性の Class IV 又は Class IV+V が 40%(20 例)
、Class V が 44%(22 例)であった。50
例中 49 例が追跡可能で、観察期間中央値は 163 週間(範囲:52~237 週間)であった。
観察期間中に CR 又は PR が認められた症例は 45/50 例(90%)であり、奏効までの期間中
央値は 37 週間(範囲:4~200 週間)であった。26 週時点までに CR は 16/50 例(32%)
、PR
は 15/50 例(30%)に認められ、1 年時点までに CR は 26/50 例(52%)
、PR は 17/50 例(34%)
に認められた。
また、11 例(22%)で 12 回の再燃が認められ、すべてネフローゼ症候群を呈した。寛解か
ら再燃までの期間中央値は 65.1 週間(範囲:20~112 週間)であり、CR 例では 7 例で 8 回、
PR 例では 4 例で 4 回の再燃が認められた。再燃した 6 例(7 回)に対して本剤 1,000 mg を 2
回再投与したところ(メチルプレドニゾロンの併用あり又は併用なし)
、CR が 3 回、PR が 1
回認められたが、3 回は無効であった。
安全性について、入院を伴う有害事象は 9/50 例(18%)に認められた。5 例は感染症であ
り、そのうち 1 例は帯状疱疹であった。本剤とメチルプレドニゾロンによる寛解導入療法後
に 1 例で 2 型糖尿病が発現した。死亡例は 2 例(4%)で、1 例(61 歳)は本剤治療 31 カ月
後に重症の末梢血管障害に対する手術の合併症により死亡した(ループス腎炎は CR)
。別の
1 例(71 歳)は、本剤初回治療 28 カ月後に自宅で突然死した。本症例は、1 年時点で PR で
あったため再生検を実施し、18 カ月時点で本剤を再投与した。死亡時もループス腎炎は PR
であった。
4) Tsanyan ME, et al. Clinical and morphological improvement of lupus nephritis treated with
rituximab. Folia Med 2014; 56: 245-52. 27)
ループス腎炎に対する本剤の臨床的及び形態学的な改善効果に関する報告。
ステロイド及び免疫抑制剤による標準治療に抵抗性を示すループス腎炎患者 45 例(23~36
歳)が対象とされた。WHO 分類(2003 年版)に基づく重症度分類は、Class IV が 32 例(71%)、
Class III が 8 例(18%)
、Class V 及び Class II が各 2 例(4%)
、Class I が 1 例(4%)であり、
全例でループス腎炎に関連した形態学的所見が確認された。
本剤は、500 mg を 1~4 回又は 1,000 mg を 1~2 回投与した。16 例はメチルプレドニゾロ
ン及び CY パルス療法を併用し、29 例は本剤単独投与であった。
本剤投与開始から 1 年以上後に腎生検が実施された患者は 16 例であり、フォローアップ期
間中に CR は 13 例(81.2%)、PR は 1 例(6.3%)に認められた。奏効が認められなかった 2
例のうち、1 例は本剤による治療で効果が得られず、別の 1 例では 1 年半後に再燃が認めら
れた。また、形態学的な改善は 16 例中 11 例で認められた。本剤による治療後に活動性スコ
アの改善が認められたが、慢性化スコアの改善は認められなかった。
安全性に関する記載はなし。
10