よむ、つかう、まなぶ。
資料3-1 リツキシマブ(遺伝子組換え) (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
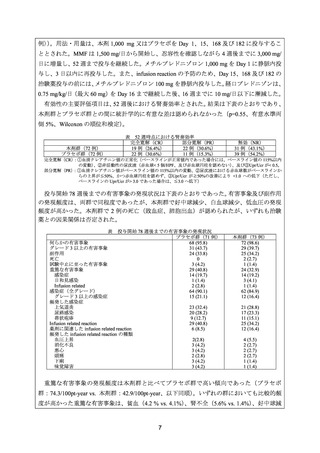
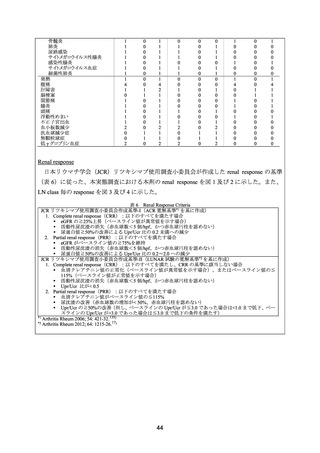
有効性について、CR は、尿蛋白が 0.5 g/日未満、血清クレアチニン及び血清アルブミンが
正常とし、PR は、尿蛋白が 50%以上改善し、血清クレアチニンが安定又は正常化と定義した。
12 カ月時点において、CR 及び PR は各 6 例(33.3%)であった。また、9 カ月時点では PR
であったものの、
12 カ月時点で尿蛋白の増加を伴う再発が認められた症例が 2 例認められた。
併用しているステロイドについて、6 例で中止、6 例で減量が可能であった(残りの 6 例は同
一用量を維持)
。
安全性について、治療に関連する有害事象の数は少なかった。1 カ月時点で高血圧に対す
るノンコンプライアンスにより 1 例が死亡した。また、1 年以内に、入院を要する感染症が 3
例(16.7%)に 4 件認められ、本剤投与 3 日後にカニューレ部の蜂巣炎を発現した 1 例、原疾
患による心外膜液貯留で入院後に尿性敗血症を発現した 1 例、腎外ループスの再燃に対して
ステロイドを増量した際に胸部感染症を発現し、本剤投与 1 年後に帯状疱疹を発現した 1 例
であった。
14) Davies RJ, et al. Rituximab in the treatment of resistant lupus nephritis: therapy failure in rapidly
progressive crescentic lupus nephritis. Lupus 2013; 22: 574-82. 11)
21~45 歳の既存治療抵抗性ループス腎炎患者 18 例を非盲検試験に組み入れ、
本剤 1,000 mg
を 2 週間間隔で 2 回投与した。本剤投与時に、CY 500 mg 及びメチルプレドニゾロン 500 mg
を併用した。
有効性について、CR は、尿蛋白が 0.5 g/日未満、血清クレアチニン及び血清アルブミンが
正常、尿沈渣正常とし、PR は、ベースライン時に異常が認められていたすべての腎機能評価
項目が 50%以上改善と定義した。
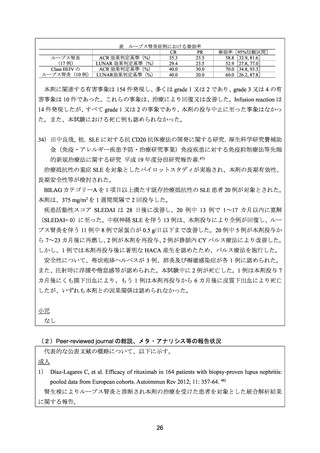
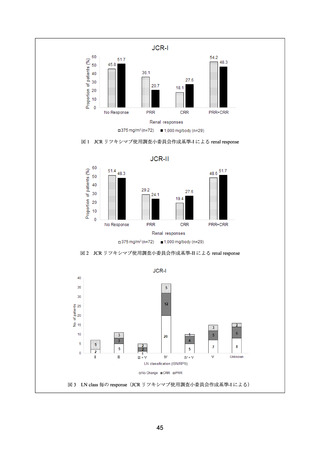
6 カ月時点で、18 例中 CR は 11 例(61.1%)
、PR は 2 例(11.1%)に認められた。6 カ月~6
年の間に、ループス腎炎又はネフローゼ症候群の再燃が 5 例(27.8%)に認められた。
安全性について、2 回目の本剤投与中に急性過敏症反応として一過性の唇の腫脹を認めた 1
例で本剤の投与を中止した。本症例は、長期血液透析中に重症の敗血症を発現し、本剤投与
から 6 年後に死亡した。1 例で MRSA による敗血症が発現したが、治療により回復した。そ
の他、本剤投与後に血球減少や血清異常は認められなかった。
15) Contis A, et al. Analysis of the effectiveness and safety of rituximab in patients with refractory
lupus nephritis: a chart review. Clin Rheumatol 2016; 35: 517-22. 34)
30~44 歳の CY を含む標準治療に抵抗性を示すループス腎炎患者 17 例に対して本剤
375 mg/m2 を 1 週間間隔で 4 回投与(10 例)
、又は 1,000 mg を 2 週間間隔で 2 回投与した(7
例)。全例でプレドニゾンパルス(100~750 mg)を併用した。
有効性について、CR は、尿蛋白が 0.2 g/日未満、GFR が安定又は 90 mL/分以上、尿沈渣正
常とし、PR は、尿蛋白が 0.2~0.5 g/日、GFR が安定又は 90 mL/分以上、尿沈渣正常と定義し
た。
52 週時点において、CR は 4 例(23.5%)
、PR は 5 例(29.4%)に認められた。
16
正常とし、PR は、尿蛋白が 50%以上改善し、血清クレアチニンが安定又は正常化と定義した。
12 カ月時点において、CR 及び PR は各 6 例(33.3%)であった。また、9 カ月時点では PR
であったものの、
12 カ月時点で尿蛋白の増加を伴う再発が認められた症例が 2 例認められた。
併用しているステロイドについて、6 例で中止、6 例で減量が可能であった(残りの 6 例は同
一用量を維持)
。
安全性について、治療に関連する有害事象の数は少なかった。1 カ月時点で高血圧に対す
るノンコンプライアンスにより 1 例が死亡した。また、1 年以内に、入院を要する感染症が 3
例(16.7%)に 4 件認められ、本剤投与 3 日後にカニューレ部の蜂巣炎を発現した 1 例、原疾
患による心外膜液貯留で入院後に尿性敗血症を発現した 1 例、腎外ループスの再燃に対して
ステロイドを増量した際に胸部感染症を発現し、本剤投与 1 年後に帯状疱疹を発現した 1 例
であった。
14) Davies RJ, et al. Rituximab in the treatment of resistant lupus nephritis: therapy failure in rapidly
progressive crescentic lupus nephritis. Lupus 2013; 22: 574-82. 11)
21~45 歳の既存治療抵抗性ループス腎炎患者 18 例を非盲検試験に組み入れ、
本剤 1,000 mg
を 2 週間間隔で 2 回投与した。本剤投与時に、CY 500 mg 及びメチルプレドニゾロン 500 mg
を併用した。
有効性について、CR は、尿蛋白が 0.5 g/日未満、血清クレアチニン及び血清アルブミンが
正常、尿沈渣正常とし、PR は、ベースライン時に異常が認められていたすべての腎機能評価
項目が 50%以上改善と定義した。
6 カ月時点で、18 例中 CR は 11 例(61.1%)
、PR は 2 例(11.1%)に認められた。6 カ月~6
年の間に、ループス腎炎又はネフローゼ症候群の再燃が 5 例(27.8%)に認められた。
安全性について、2 回目の本剤投与中に急性過敏症反応として一過性の唇の腫脹を認めた 1
例で本剤の投与を中止した。本症例は、長期血液透析中に重症の敗血症を発現し、本剤投与
から 6 年後に死亡した。1 例で MRSA による敗血症が発現したが、治療により回復した。そ
の他、本剤投与後に血球減少や血清異常は認められなかった。
15) Contis A, et al. Analysis of the effectiveness and safety of rituximab in patients with refractory
lupus nephritis: a chart review. Clin Rheumatol 2016; 35: 517-22. 34)
30~44 歳の CY を含む標準治療に抵抗性を示すループス腎炎患者 17 例に対して本剤
375 mg/m2 を 1 週間間隔で 4 回投与(10 例)
、又は 1,000 mg を 2 週間間隔で 2 回投与した(7
例)。全例でプレドニゾンパルス(100~750 mg)を併用した。
有効性について、CR は、尿蛋白が 0.2 g/日未満、GFR が安定又は 90 mL/分以上、尿沈渣正
常とし、PR は、尿蛋白が 0.2~0.5 g/日、GFR が安定又は 90 mL/分以上、尿沈渣正常と定義し
た。
52 週時点において、CR は 4 例(23.5%)
、PR は 5 例(29.4%)に認められた。
16