よむ、つかう、まなぶ。
資料3-1 リツキシマブ(遺伝子組換え) (32 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
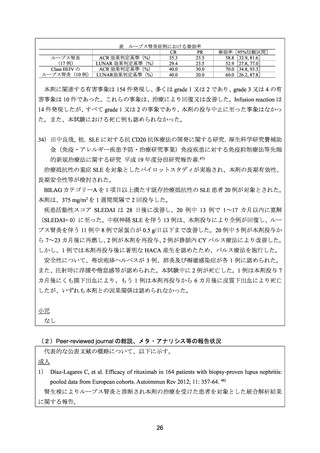
に腎フレアが認められた。腎フレアに対して本剤を再投与した 20 例中 18 例(90%)で
腎奏効が認められた。
本剤の初回治療コースにおいて、有害事象は 32/134 例(23.9%)に認められた。感染症
は 22 例(16.4%)、infusion reaction は 5 例(3.7%)に認められた。重症の感染症は 8 例(6%)
に認められ、その内訳は敗血症 4 例、腸感染、肺感染各 2 例であった。免疫抑制剤やス
テロイドの併用の有無により、有害事象の発現頻度に差は認められなかった。しかしな
がら、静注メチルプレドニゾロン併用例では感染症の発現割合が高く(併用あり:13.6%、
併用なし:0%)、シクロスポリン併用例では敗血症の発現割合が高かった(併用あり:
50%、併用なし:7.9%)
。
2 回目の治療コースにおいて、有害事象は 15/45 例(33.3%)に認められた。感染症は 10
例(22.2%)に認められ、3 例(6.7%)は重症の感染症(上気道 2 例、中枢神経系 1 例)
であった。3 回目の治療コースにおいて、有害事象は 5/13 例(38.5%)に認められた。感
染症は 3 例(23.1%)に認められたが、いずれも軽度であった。Infusion reaction は 2 コー
ス目では 5 例(11.1%)、3 コース目では 2 例(15.3%)に認められた。
いずれの治療コースにおいても重症の infusion reaction は認められず、死亡も認められな
かった。
小児
9) Vazzana
KM,
et
al.
Principles
of
pediatric
lupus
nephritis
in
a
prospective
contemporary multi-center cohort. Lupus 2021; 30: 1660-70. 53)
The Childhood Arthritis and Rheumatology Research Alliance(CARRA)レジストリに登録され
た小児 SLE 患者 677 例を対象として、小児 SLE におけるループス腎炎の合併頻度、診断時期、
短期的な腎アウトカム、本剤の導入療法としての使用頻度が検討された。
本剤に関する結果の概要を以下に示す。
CARRA レジストリに登録された小児 SLE 患者 677 例のうち、216 例(32%)がループス
腎炎を有していた。
本剤は、小児ループス腎炎患者 55 例(25.5%)
、ループス腎炎を合併しない小児 SLE 患
者 55 例(12%)に投与されていた。ループス腎炎の病型や年齢、人種、民族、性別等の
患者背景により、本剤の投与頻度に違いは認められなかった。
本剤投与例では免疫抑制剤が併用されていることが多く、87.3%でミコフェノール酸、
67.3%で CY が併用されていた。
10) Mahmoud I, et al. Efficacy and Safety of Rituximab in the Management of Pediatric Systemic
Lupus Erythematosus: A Systematic Review. J Pediatr 2017; 187: 213-9. 54)
小児 SLE に対する本剤の有効性及び安全性を評価することを目的として、システマティッ
ク・レビューが実施された。MEDLINE、Scopus、Web of Knowledge、the Cochrane Library、
ACR 及び EULAR のデータベースを検索し、本剤が投与された 18 歳未満の SLE 患者を対象
32
腎奏効が認められた。
本剤の初回治療コースにおいて、有害事象は 32/134 例(23.9%)に認められた。感染症
は 22 例(16.4%)、infusion reaction は 5 例(3.7%)に認められた。重症の感染症は 8 例(6%)
に認められ、その内訳は敗血症 4 例、腸感染、肺感染各 2 例であった。免疫抑制剤やス
テロイドの併用の有無により、有害事象の発現頻度に差は認められなかった。しかしな
がら、静注メチルプレドニゾロン併用例では感染症の発現割合が高く(併用あり:13.6%、
併用なし:0%)、シクロスポリン併用例では敗血症の発現割合が高かった(併用あり:
50%、併用なし:7.9%)
。
2 回目の治療コースにおいて、有害事象は 15/45 例(33.3%)に認められた。感染症は 10
例(22.2%)に認められ、3 例(6.7%)は重症の感染症(上気道 2 例、中枢神経系 1 例)
であった。3 回目の治療コースにおいて、有害事象は 5/13 例(38.5%)に認められた。感
染症は 3 例(23.1%)に認められたが、いずれも軽度であった。Infusion reaction は 2 コー
ス目では 5 例(11.1%)、3 コース目では 2 例(15.3%)に認められた。
いずれの治療コースにおいても重症の infusion reaction は認められず、死亡も認められな
かった。
小児
9) Vazzana
KM,
et
al.
Principles
of
pediatric
lupus
nephritis
in
a
prospective
contemporary multi-center cohort. Lupus 2021; 30: 1660-70. 53)
The Childhood Arthritis and Rheumatology Research Alliance(CARRA)レジストリに登録され
た小児 SLE 患者 677 例を対象として、小児 SLE におけるループス腎炎の合併頻度、診断時期、
短期的な腎アウトカム、本剤の導入療法としての使用頻度が検討された。
本剤に関する結果の概要を以下に示す。
CARRA レジストリに登録された小児 SLE 患者 677 例のうち、216 例(32%)がループス
腎炎を有していた。
本剤は、小児ループス腎炎患者 55 例(25.5%)
、ループス腎炎を合併しない小児 SLE 患
者 55 例(12%)に投与されていた。ループス腎炎の病型や年齢、人種、民族、性別等の
患者背景により、本剤の投与頻度に違いは認められなかった。
本剤投与例では免疫抑制剤が併用されていることが多く、87.3%でミコフェノール酸、
67.3%で CY が併用されていた。
10) Mahmoud I, et al. Efficacy and Safety of Rituximab in the Management of Pediatric Systemic
Lupus Erythematosus: A Systematic Review. J Pediatr 2017; 187: 213-9. 54)
小児 SLE に対する本剤の有効性及び安全性を評価することを目的として、システマティッ
ク・レビューが実施された。MEDLINE、Scopus、Web of Knowledge、the Cochrane Library、
ACR 及び EULAR のデータベースを検索し、本剤が投与された 18 歳未満の SLE 患者を対象
32