よむ、つかう、まなぶ。
資料3-1 リツキシマブ(遺伝子組換え) (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
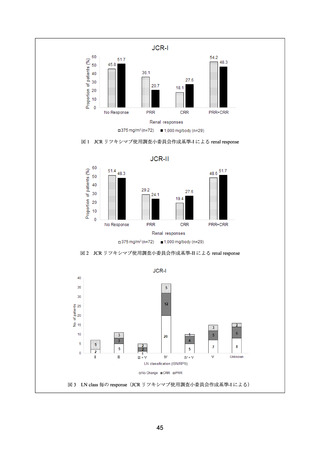
CR は 5/22 例、PR は 7/22 例であった。また、6 例では奏効(CR 又は PR)とは判定されな
かったものの、1 つ以上の腎機能の評価項目の改善が認められた。
安全性について、21/22 例では、本剤投与による重篤な感染症や有害事象を示唆する臨床所
見は認められなかった。しかし、1 例において、本剤治療開始 70 日目に、糖尿病に関連した
重篤な代謝性アシドーシス及び肺炎を発現し、その 48 時間後にびまん性の肺浸潤による呼吸
不全で死亡した。検死の結果、肺に広範囲な出血を伴うヒストプラズマ浸潤を認め、冠動脈
にムコール症が認められた。
9) Goswami RP, et al. Cyclophosphamide Versus Mycophenolate Versus Rituximab in Lupus
Nephritis Remission Induction: A Historical Head-to-Head Comparative Study. J Clin Rheumatol
2019; 25: 28-35. 29)
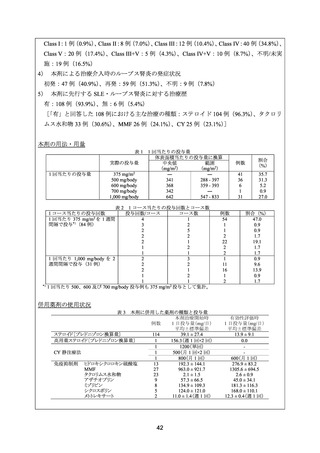
高用量 CY、低用量 CY、MMF 及び本剤のループス腎炎に対する有効性を比較するため、
後方視的観察研究が実施された。
CY 500 mg を隔週で 6 回投与し、その後アザチオプリン(50~100 mg/日)又は MMF(1,000
~1,500 mg/日)を投与(低用量 CY)
、CY 750~1,200 mg を月 1 回で 6 回投与(高用量 CY)、
MMF 1,500~3,000 mg/日、又は本剤による治療を受けたループス腎炎患者を対象とした。有
効性評価時点は治療開始 6 カ月後とし、CR は血清クレアチニンが 1.3 mg/dL 未満、尿検査が
正常及び 24 時間尿蛋白が 500 mg/dL 未満、PR は血清クレアチニンが 1.3 mg/dL 未満、尿検査
が正常及び 24 時間尿蛋白が 500 mg/dL 以上 2,000 mg/dL 未満かつ 50%を超える減少と定義し
た。
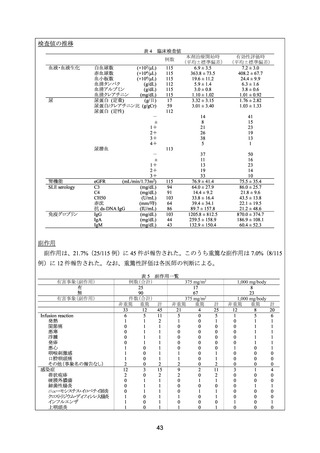
222 例(平均年齢 25.9 歳)が対象とされ、このうち低用量 CY(総曝露量 3 g)が 26 例、高
用量 CY(総曝露量平均 5.1 g)が 113 例、MMF(平均投与量 2.2 g/日)が 61 例、本剤(総曝
露量平均 1.9 g)が 22 例であった。本剤投与例のうち、6 例は本剤単独投与、16 例は MMF 又
は CY との併用投与であった。再発又は難治性のループス腎炎に対しては 1 例が低用量 CY、
11 例が高用量 CY、10 例が MMF、14 例が本剤による治療を受けた。
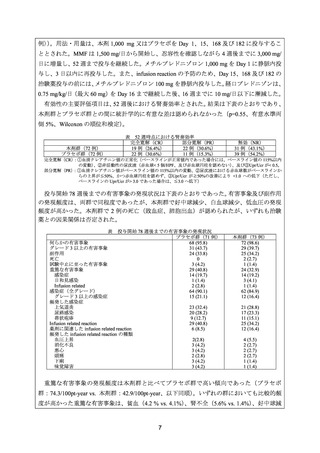
腎奏効率(CR 又は PR)は、低用量 CY:73.1%(19/26 例)
、高用量 CY:90.3%(102/113
例)、MMF:72.1%(44/61 例)、本剤:90.9%(20/22)例であった。再発又は難治性のループ
ス腎炎に対する腎奏効率(CR 又は PR)は、低用量 CY:50%(1/2 例)
、高用量 CY:72.7%
(8/11 例)
、MMF:50%(5/10 例)、本剤:100%(14/14)例であった。
安全性について、有害事象の発現割合は低用量 CY:34.6%(9/26 例)
、高用量 CY:26.5%
(30/113 例)
、MMF:77%(47/61 例)
、本剤:31.8%(7/22 例)
、入院を要する重篤な有害事
象の発現割合は低用量 CY:7.7%(2/26 例)
、高用量 CY:4.4%(5/113 例)
、MMF:6.6%(4/61
例)、本剤:9.1%(2/22 例)
、感染症の発現割合は低用量 CY:23.1%(6/26 例)、高用量 CY:
20.4%(23/113 例)、MMF:14.7%(9/61 例)
、本剤:27.3%(6/22 例)であった。また、本剤
投与例の 1 例でてんかん発作が認められた。
10) Melander C, et al. Rituximab in severe lupus nephritis: early B-cell depletion affects long-term
13
かったものの、1 つ以上の腎機能の評価項目の改善が認められた。
安全性について、21/22 例では、本剤投与による重篤な感染症や有害事象を示唆する臨床所
見は認められなかった。しかし、1 例において、本剤治療開始 70 日目に、糖尿病に関連した
重篤な代謝性アシドーシス及び肺炎を発現し、その 48 時間後にびまん性の肺浸潤による呼吸
不全で死亡した。検死の結果、肺に広範囲な出血を伴うヒストプラズマ浸潤を認め、冠動脈
にムコール症が認められた。
9) Goswami RP, et al. Cyclophosphamide Versus Mycophenolate Versus Rituximab in Lupus
Nephritis Remission Induction: A Historical Head-to-Head Comparative Study. J Clin Rheumatol
2019; 25: 28-35. 29)
高用量 CY、低用量 CY、MMF 及び本剤のループス腎炎に対する有効性を比較するため、
後方視的観察研究が実施された。
CY 500 mg を隔週で 6 回投与し、その後アザチオプリン(50~100 mg/日)又は MMF(1,000
~1,500 mg/日)を投与(低用量 CY)
、CY 750~1,200 mg を月 1 回で 6 回投与(高用量 CY)、
MMF 1,500~3,000 mg/日、又は本剤による治療を受けたループス腎炎患者を対象とした。有
効性評価時点は治療開始 6 カ月後とし、CR は血清クレアチニンが 1.3 mg/dL 未満、尿検査が
正常及び 24 時間尿蛋白が 500 mg/dL 未満、PR は血清クレアチニンが 1.3 mg/dL 未満、尿検査
が正常及び 24 時間尿蛋白が 500 mg/dL 以上 2,000 mg/dL 未満かつ 50%を超える減少と定義し
た。
222 例(平均年齢 25.9 歳)が対象とされ、このうち低用量 CY(総曝露量 3 g)が 26 例、高
用量 CY(総曝露量平均 5.1 g)が 113 例、MMF(平均投与量 2.2 g/日)が 61 例、本剤(総曝
露量平均 1.9 g)が 22 例であった。本剤投与例のうち、6 例は本剤単独投与、16 例は MMF 又
は CY との併用投与であった。再発又は難治性のループス腎炎に対しては 1 例が低用量 CY、
11 例が高用量 CY、10 例が MMF、14 例が本剤による治療を受けた。
腎奏効率(CR 又は PR)は、低用量 CY:73.1%(19/26 例)
、高用量 CY:90.3%(102/113
例)、MMF:72.1%(44/61 例)、本剤:90.9%(20/22)例であった。再発又は難治性のループ
ス腎炎に対する腎奏効率(CR 又は PR)は、低用量 CY:50%(1/2 例)
、高用量 CY:72.7%
(8/11 例)
、MMF:50%(5/10 例)、本剤:100%(14/14)例であった。
安全性について、有害事象の発現割合は低用量 CY:34.6%(9/26 例)
、高用量 CY:26.5%
(30/113 例)
、MMF:77%(47/61 例)
、本剤:31.8%(7/22 例)
、入院を要する重篤な有害事
象の発現割合は低用量 CY:7.7%(2/26 例)
、高用量 CY:4.4%(5/113 例)
、MMF:6.6%(4/61
例)、本剤:9.1%(2/22 例)
、感染症の発現割合は低用量 CY:23.1%(6/26 例)、高用量 CY:
20.4%(23/113 例)、MMF:14.7%(9/61 例)
、本剤:27.3%(6/22 例)であった。また、本剤
投与例の 1 例でてんかん発作が認められた。
10) Melander C, et al. Rituximab in severe lupus nephritis: early B-cell depletion affects long-term
13