よむ、つかう、まなぶ。
資料3-1 リツキシマブ(遺伝子組換え) (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
症例が 27 例、ループス腎炎の再燃が 22 例、治療抵抗性が 5 例であった。重症の血小板減少
が認められた 3 例を除く 51 例に腎生検を実施し、
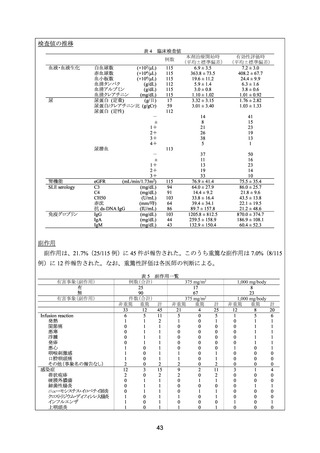
ISN/RPS 基準に基づく評価を行ったところ、
Class III が 9 例、Class IV が 26 例、Class V が 2 例、Class III+IV が 4 例、Class IV+V が 10 例
であった。
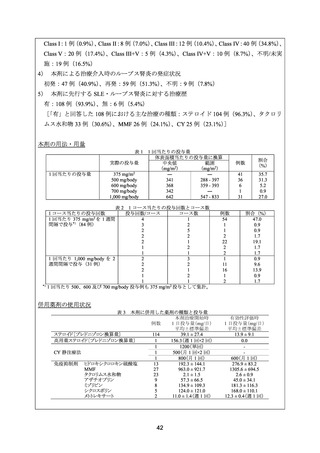
登録された 54 例は、本剤(17 例)
、MMF(17 例)又は CY パルス療法(20 例)による治
療を受け、全例でステロイドを併用した。ステロイドは、メチルプレドニゾロンパルス療法
を 3 日間実施し、プレドニゾン 0.5~0.75 mg/kg/日を 1 カ月間経口投与した後、医師の判断で
漸減した。本剤は、メチルプレドニゾロンパルス療法 3 日目の終了時と day 18 に 1,000 mg を
2 回投与した。MMF は、2,000~2,500 mg/日を投与した。CY は、500 mg/回を 2 週間間隔で 6
回投与した。治療開始から 4 カ月後に維持療法として、MMF(1,000~2,000 mg/日)
、アザチ
オプリン(1~2 mg/kg/日)又はシクロスポリン(1~2 mg/kg/日)をプレドニゾンに追加して
投与した。
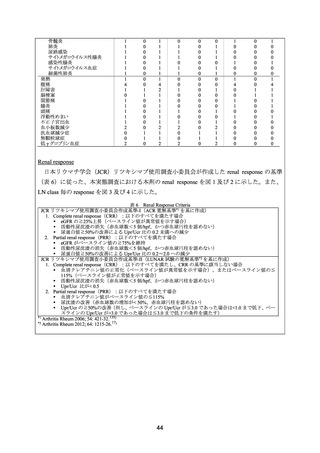
有効性の主要評価項目は 3 カ月時点の奏効及び 12 カ月時点の CR とされた。3 カ月時点の
奏効は、血清クレアチニンの改善、尿蛋白及び顕微鏡的血尿の 50%の減少と定義した。12 カ
月時点の CR は、血清クレアチニン値が 1.2 mg/dL 未満(又は慢性腎不全患者ではベースライ
ンまでの回復)
、尿蛋白が 0.5 g/日未満及び尿中赤血球数が 5 個未満/hpf と定義した。
ループス腎炎の平均罹患期間は、MMF 群(3.1 年)及び CY パルス群(1.62 年)と比較し
て、本剤群(7.1 年)で長く、登録前の平均再発回数も MMF 治療群(0.82 回)及び CY パル
ス群(0.2 回)と比較して、本剤治療群(2.5 回)で多かった。
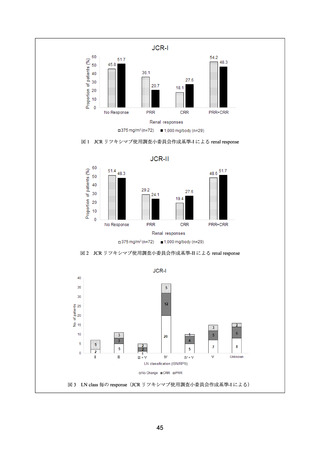
3 カ月時点における奏効率は、本剤群 58.8%(10/17 例)
、MMF 群 64.7%(11/17 例)
、CY パ
ルス群 63.1%(12/19 例)であった。12 カ月時点における CR は、本剤群 70.6%(12/17 例)
、
MMF 群 52.9%(9/17 例)
、CY パルス群 65%(13/20 例)であった。
安全性について、本剤群では、1 例で 2 回目投与時にアレルギー反応、2 例で本剤投与から
数週間後に軽度の感染症(インフルエンザ症候群及び胃腸炎)、1 例で耳炎及び殿部膿瘍が認
められ、他の 1 例で数週間にわたるびまん性の掻痒感についての訴えがあった。
3) Condon MB, et al. Prospective observational single-centre cohort study to evaluate the
effectiveness of treating lupus nephritis with rituximab and mycophenolate mofetil but no oral
steroids. Ann Rheum Dis 2013; 72: 1280-6. 26)
ループス腎炎患者に対して本剤と MMF の併用療法を実施した単施設前方視的観察試験が
実施された。
腎生検で ISN/RPS 基準の Class III/IV/V のループス腎炎と診断され、長期の経口ステロイド
治療を行っていない 50 例(19~75 歳)を対象とした。本剤 1,000 mg 及びメチルプレドニゾ
ロン 500 mg を day 1 及び day 15 に投与し、MMF は 500 mg の 1 日 2 回投与から開始し、ミコ
フェノール酸の 12 時間トラフ値が 1.2~2.4 mg/L となるよう投与量を調整した
(最大 1,500 mg
を 1 日 2 回)。
効果判定の定義として、CR は、Upr/Ucr が 50 mg/mmol 未満かつ血清クレアチニン値がベ
9
が認められた 3 例を除く 51 例に腎生検を実施し、
ISN/RPS 基準に基づく評価を行ったところ、
Class III が 9 例、Class IV が 26 例、Class V が 2 例、Class III+IV が 4 例、Class IV+V が 10 例
であった。
登録された 54 例は、本剤(17 例)
、MMF(17 例)又は CY パルス療法(20 例)による治
療を受け、全例でステロイドを併用した。ステロイドは、メチルプレドニゾロンパルス療法
を 3 日間実施し、プレドニゾン 0.5~0.75 mg/kg/日を 1 カ月間経口投与した後、医師の判断で
漸減した。本剤は、メチルプレドニゾロンパルス療法 3 日目の終了時と day 18 に 1,000 mg を
2 回投与した。MMF は、2,000~2,500 mg/日を投与した。CY は、500 mg/回を 2 週間間隔で 6
回投与した。治療開始から 4 カ月後に維持療法として、MMF(1,000~2,000 mg/日)
、アザチ
オプリン(1~2 mg/kg/日)又はシクロスポリン(1~2 mg/kg/日)をプレドニゾンに追加して
投与した。
有効性の主要評価項目は 3 カ月時点の奏効及び 12 カ月時点の CR とされた。3 カ月時点の
奏効は、血清クレアチニンの改善、尿蛋白及び顕微鏡的血尿の 50%の減少と定義した。12 カ
月時点の CR は、血清クレアチニン値が 1.2 mg/dL 未満(又は慢性腎不全患者ではベースライ
ンまでの回復)
、尿蛋白が 0.5 g/日未満及び尿中赤血球数が 5 個未満/hpf と定義した。
ループス腎炎の平均罹患期間は、MMF 群(3.1 年)及び CY パルス群(1.62 年)と比較し
て、本剤群(7.1 年)で長く、登録前の平均再発回数も MMF 治療群(0.82 回)及び CY パル
ス群(0.2 回)と比較して、本剤治療群(2.5 回)で多かった。
3 カ月時点における奏効率は、本剤群 58.8%(10/17 例)
、MMF 群 64.7%(11/17 例)
、CY パ
ルス群 63.1%(12/19 例)であった。12 カ月時点における CR は、本剤群 70.6%(12/17 例)
、
MMF 群 52.9%(9/17 例)
、CY パルス群 65%(13/20 例)であった。
安全性について、本剤群では、1 例で 2 回目投与時にアレルギー反応、2 例で本剤投与から
数週間後に軽度の感染症(インフルエンザ症候群及び胃腸炎)、1 例で耳炎及び殿部膿瘍が認
められ、他の 1 例で数週間にわたるびまん性の掻痒感についての訴えがあった。
3) Condon MB, et al. Prospective observational single-centre cohort study to evaluate the
effectiveness of treating lupus nephritis with rituximab and mycophenolate mofetil but no oral
steroids. Ann Rheum Dis 2013; 72: 1280-6. 26)
ループス腎炎患者に対して本剤と MMF の併用療法を実施した単施設前方視的観察試験が
実施された。
腎生検で ISN/RPS 基準の Class III/IV/V のループス腎炎と診断され、長期の経口ステロイド
治療を行っていない 50 例(19~75 歳)を対象とした。本剤 1,000 mg 及びメチルプレドニゾ
ロン 500 mg を day 1 及び day 15 に投与し、MMF は 500 mg の 1 日 2 回投与から開始し、ミコ
フェノール酸の 12 時間トラフ値が 1.2~2.4 mg/L となるよう投与量を調整した
(最大 1,500 mg
を 1 日 2 回)。
効果判定の定義として、CR は、Upr/Ucr が 50 mg/mmol 未満かつ血清クレアチニン値がベ
9