よむ、つかう、まなぶ。
資料3-1 リツキシマブ(遺伝子組換え) (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
症の 1 例が、18 カ月後に拡張型心筋症により死亡した。また、治療抵抗性の重症かつ生命を
脅かす自己免疫性溶血性貧血を発現した 1 例に同種幹細胞移植を行ったが、本剤治療の 35 カ
月後にカンジダ感染により死亡した。その他の 26 例においては、本剤投与後に重症のアレル
ギー反応や有害事象は認められなかった。
18) Kotagiri P, et al. Single-dose rituximab in refractory lupus nephritis. Intern Med J 2016; 46:
899-901. 36)
難治性ループス腎炎患者(Class III/IV±V、年齢の中央値 33 歳〈四分位範囲:24~39 歳〉)
14 例を対象とした前方視的研究。本剤 375 mg/m2 を 1 回投与した。免疫抑制剤は継続し、担
当医の判断により適宜漸減した。
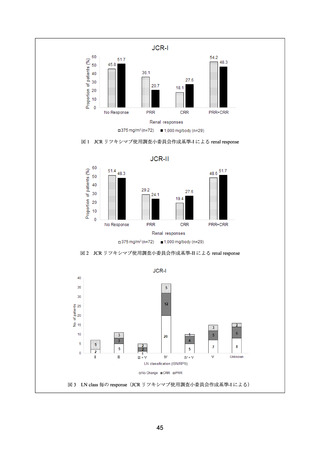
ループス腎炎に関する有効性について、CR は、Upr/Ucr が 35 mg/mmol 以下、血清クレア
チニン及び血清アルブミンが正常値、尿沈渣正常とし、PR:ベースライン時に異常を認めて
いた腎機能評価項目が 50%以上改善し、悪化を認めない場合と定義した。
5 カ月時点(中央値、四分位範囲:4~8 カ月)で、CR 又は PR は 11 例(79%)
(CR:2 例、
PR:9 例)に認められた。観察期間終了時点(中央値 23 カ月、四分位範囲:14~24 カ月)で
6 例(55%)が寛解を維持していた。
安全性について、治療開始後 1 年以内に、入院を必要とする感染症は 3 例(帯状疱疹、蜂
巣炎、大腸菌敗血症)が認められた。進行性多層性白質脳症や好中球減少症は認められなか
った。
19) Catapano F, et al. Long-term efficacy and safety of rituximab in refractory and relapsing systemic
lupus erythematosus. Nephrol Dial Transplant 2010; 25: 3586-92. 37)
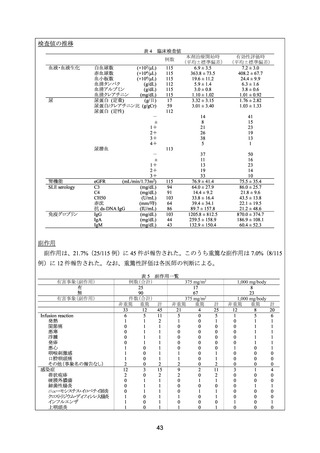
13~61 歳の再発又は難治性の SLE 患者 31 例(ループス腎炎合併例 11 例を含む)を対象と
した後方視的研究。本剤 375 mg/m2 を 1 週間間隔で 4 回投与(15 例)
、又は 1,000 mg を 2 週
間間隔で 2 回投与した(16 例)。本剤が無効又は再燃した 15 例に対して本剤を再投与した。
また、7 例では本剤 1,000 mg を 6 カ月毎に 2 年間投与した。
ループス腎炎に関する有効性について、CR は、尿蛋白が 0.5 g/日未満、尿沈渣正常、血清
クレアチニンが安定又は低下とし、PR は、尿蛋白が 50%以上改善、尿沈渣の赤血球数/hpf が
30 個未満、血清クレアチニンが安定又は低下と定義した。
ループス腎炎合併例 11 例のうち、奏効は 10 例(CR:4 例、PR:6 例)に認められた。
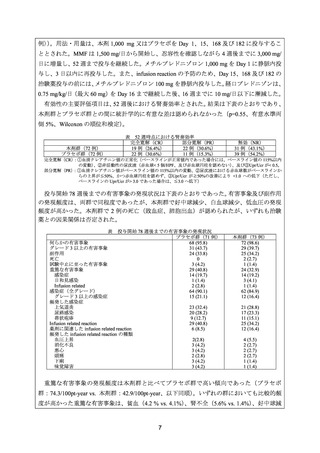
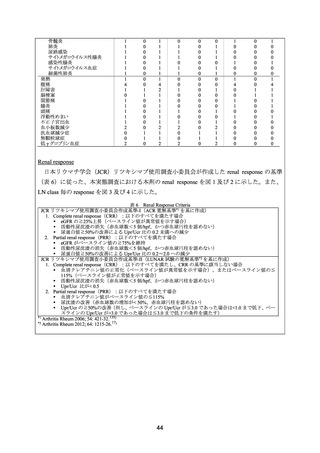
安全性について、infusion reaction は 14 例(45%)で 20 件認められた。重篤な infusion reaction
は 7 例(23%)に認められた。重篤な感染症は 8 例(26%)で 11 件(胸部感染症 9 件、帯状
疱疹、敗血症各 1 件)認められたが、いずれも治療により回復した。1 例に、本剤初回投与
から 3 週間後と 2 回目治療の 4.5 カ月後に一過性の好中球減少が認められた。本剤投与後に 3
例が死亡した(活動性 SLE 及び感染症、突然の心停止、末期腎不全による重篤な敗血症)
。
20) Boletis JN, et al. Rituximab and mycophenolate mofetil for relapsing proliferative lupus
18
脅かす自己免疫性溶血性貧血を発現した 1 例に同種幹細胞移植を行ったが、本剤治療の 35 カ
月後にカンジダ感染により死亡した。その他の 26 例においては、本剤投与後に重症のアレル
ギー反応や有害事象は認められなかった。
18) Kotagiri P, et al. Single-dose rituximab in refractory lupus nephritis. Intern Med J 2016; 46:
899-901. 36)
難治性ループス腎炎患者(Class III/IV±V、年齢の中央値 33 歳〈四分位範囲:24~39 歳〉)
14 例を対象とした前方視的研究。本剤 375 mg/m2 を 1 回投与した。免疫抑制剤は継続し、担
当医の判断により適宜漸減した。
ループス腎炎に関する有効性について、CR は、Upr/Ucr が 35 mg/mmol 以下、血清クレア
チニン及び血清アルブミンが正常値、尿沈渣正常とし、PR:ベースライン時に異常を認めて
いた腎機能評価項目が 50%以上改善し、悪化を認めない場合と定義した。
5 カ月時点(中央値、四分位範囲:4~8 カ月)で、CR 又は PR は 11 例(79%)
(CR:2 例、
PR:9 例)に認められた。観察期間終了時点(中央値 23 カ月、四分位範囲:14~24 カ月)で
6 例(55%)が寛解を維持していた。
安全性について、治療開始後 1 年以内に、入院を必要とする感染症は 3 例(帯状疱疹、蜂
巣炎、大腸菌敗血症)が認められた。進行性多層性白質脳症や好中球減少症は認められなか
った。
19) Catapano F, et al. Long-term efficacy and safety of rituximab in refractory and relapsing systemic
lupus erythematosus. Nephrol Dial Transplant 2010; 25: 3586-92. 37)
13~61 歳の再発又は難治性の SLE 患者 31 例(ループス腎炎合併例 11 例を含む)を対象と
した後方視的研究。本剤 375 mg/m2 を 1 週間間隔で 4 回投与(15 例)
、又は 1,000 mg を 2 週
間間隔で 2 回投与した(16 例)。本剤が無効又は再燃した 15 例に対して本剤を再投与した。
また、7 例では本剤 1,000 mg を 6 カ月毎に 2 年間投与した。
ループス腎炎に関する有効性について、CR は、尿蛋白が 0.5 g/日未満、尿沈渣正常、血清
クレアチニンが安定又は低下とし、PR は、尿蛋白が 50%以上改善、尿沈渣の赤血球数/hpf が
30 個未満、血清クレアチニンが安定又は低下と定義した。
ループス腎炎合併例 11 例のうち、奏効は 10 例(CR:4 例、PR:6 例)に認められた。
安全性について、infusion reaction は 14 例(45%)で 20 件認められた。重篤な infusion reaction
は 7 例(23%)に認められた。重篤な感染症は 8 例(26%)で 11 件(胸部感染症 9 件、帯状
疱疹、敗血症各 1 件)認められたが、いずれも治療により回復した。1 例に、本剤初回投与
から 3 週間後と 2 回目治療の 4.5 カ月後に一過性の好中球減少が認められた。本剤投与後に 3
例が死亡した(活動性 SLE 及び感染症、突然の心停止、末期腎不全による重篤な敗血症)
。
20) Boletis JN, et al. Rituximab and mycophenolate mofetil for relapsing proliferative lupus
18