よむ、つかう、まなぶ。
資料3-1 リツキシマブ(遺伝子組換え) (12 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
た。
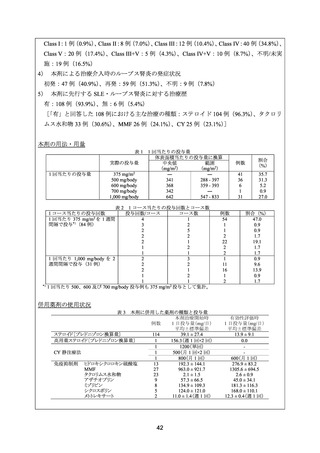
25 例中 20 例では、本剤 375 mg/m2 を 1 週間間隔で 4 回投与し、このうち 16 例は CY 併用
(1 回目及び 4 回目の本剤投与時に 500 mg を静注)
、2 例は MMF 併用、2 例は本剤単独投与
であった。3 回目の本剤投与開始時に infusion reaction が発現した 1 例では、本剤の投与回数
は 3 回、CY の投与回数は 1 回であった。また、25 例中 5 例では、本剤 1,000 mg を 2 週間間
隔で 2 回投与した。ステロイドは治療中に増量し(~0.5 mg/kg)
、その後漸減した。
観察期間の平均値は 36 カ月(範囲:9~95 カ月)であった。ベースライン時及び 6 カ月時
点における腎機能を評価した結果、クレアチニン平均値には差が認められなかったが(100
nmol/L 及び 84 nmol/L)、血清アルブミン平均値の上昇(27 g/L 及び 33 g/L)
、24 時間尿蛋白平
均値の減少(3 g/日及び 1.1 g/日)が認められた。また、追跡が可能であった 17 例について、
24 時間尿蛋白平均値は、12 カ月時点(1.1 g/日)及び 24 カ月時点(0.5 g/日)でさらに減少傾
向が認められ、36 カ月時点まで追跡可能であった 14 例の尿蛋白平均値は 0.1 g/日まで減少し
た。
ベースライン時及び再生検時(生検までの平均期間 8 カ月(範囲:3~12 カ月)
)において
組織学的評価を行った結果、再生検時に多くの患者で組織学的改善が認められ、活動性の指
標は 4.5 から 2.3 に減少したが、慢性化の指標に変化は認められなかった。
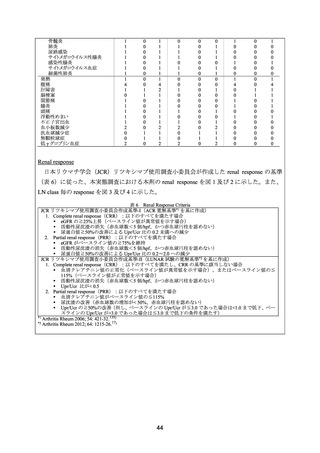
効果判定は、BILAG(British Isles Lupus Assessment Group)の活動性指標により評価し、
BILAG C を PR、BILAG D を CR とした。観察期間中央値 12 カ月(範囲:6~36 カ月)にお
いて、25 例中 22 例で奏効(CR 又は PR)が認められ、観察期間中央値 24 カ月(範囲:6~
36 カ月)では 16 例が CR であった。なお、再燃を認めた症例は 6 例(CR:3 例、PR:1 例、
無効:2 例)であり、再燃までの平均期間は 29 カ月(範囲:10~64 カ月)であった。17 カ
月以内に再燃した 4 例は全例が Class III/IV の症例であり、60 カ月以降に再燃した 2 例はいず
れも Class V の症例であった。
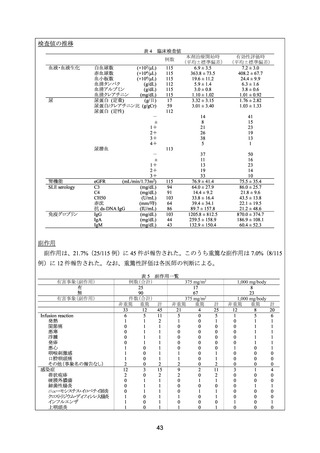
安全性について、有害事象は、最初の 6 カ月間で、尿路感染が 3 例、サルモネラ感染が 1
例、帯状疱疹の再活性化が 2 例、infusion reaction が 3 例(軽度 2 例、中等度 1 例)に認めら
れた。また、重篤な有害事象は 4 例で認められ、本剤及び CY の最終投与から 1 週間後に発
熱性好中球減少症を発現した 1 例、重篤な好中球減少症を発現した 2 例、治療の 5 カ月後に
重篤な壊疽性筋膜炎及び敗血症が発現した 1 例であった。
8) Vigna-Perez M, et al. Clinical and immunological effects of Rituximab in patients with lupus
nephritis refractory to conventional therapy: a pilot study. Arthritis Res Ther 2006; 8: R83. 28)
既存治療に抵抗性を示し、WHO 分類に基づき活動性ループス腎炎と診断された 22 例(9
~56 歳、Class III:2 例、Class IV:18 例、Class V:2 例)が非盲検試験に組み入れられた。
免疫抑制剤による治療が全例で継続され、本剤は 500~1,000 mg を day 1 及び day 15 に 2 回投
与した。
CR は、尿蛋白が 0.5 g/日未満、血清クレアチニン値の正常化及び尿沈渣が正常の場合とし、
PR は試験開始時に異常を認めた腎機能評価項目が 40%を超えて改善した場合と定義した。
12
25 例中 20 例では、本剤 375 mg/m2 を 1 週間間隔で 4 回投与し、このうち 16 例は CY 併用
(1 回目及び 4 回目の本剤投与時に 500 mg を静注)
、2 例は MMF 併用、2 例は本剤単独投与
であった。3 回目の本剤投与開始時に infusion reaction が発現した 1 例では、本剤の投与回数
は 3 回、CY の投与回数は 1 回であった。また、25 例中 5 例では、本剤 1,000 mg を 2 週間間
隔で 2 回投与した。ステロイドは治療中に増量し(~0.5 mg/kg)
、その後漸減した。
観察期間の平均値は 36 カ月(範囲:9~95 カ月)であった。ベースライン時及び 6 カ月時
点における腎機能を評価した結果、クレアチニン平均値には差が認められなかったが(100
nmol/L 及び 84 nmol/L)、血清アルブミン平均値の上昇(27 g/L 及び 33 g/L)
、24 時間尿蛋白平
均値の減少(3 g/日及び 1.1 g/日)が認められた。また、追跡が可能であった 17 例について、
24 時間尿蛋白平均値は、12 カ月時点(1.1 g/日)及び 24 カ月時点(0.5 g/日)でさらに減少傾
向が認められ、36 カ月時点まで追跡可能であった 14 例の尿蛋白平均値は 0.1 g/日まで減少し
た。
ベースライン時及び再生検時(生検までの平均期間 8 カ月(範囲:3~12 カ月)
)において
組織学的評価を行った結果、再生検時に多くの患者で組織学的改善が認められ、活動性の指
標は 4.5 から 2.3 に減少したが、慢性化の指標に変化は認められなかった。
効果判定は、BILAG(British Isles Lupus Assessment Group)の活動性指標により評価し、
BILAG C を PR、BILAG D を CR とした。観察期間中央値 12 カ月(範囲:6~36 カ月)にお
いて、25 例中 22 例で奏効(CR 又は PR)が認められ、観察期間中央値 24 カ月(範囲:6~
36 カ月)では 16 例が CR であった。なお、再燃を認めた症例は 6 例(CR:3 例、PR:1 例、
無効:2 例)であり、再燃までの平均期間は 29 カ月(範囲:10~64 カ月)であった。17 カ
月以内に再燃した 4 例は全例が Class III/IV の症例であり、60 カ月以降に再燃した 2 例はいず
れも Class V の症例であった。
安全性について、有害事象は、最初の 6 カ月間で、尿路感染が 3 例、サルモネラ感染が 1
例、帯状疱疹の再活性化が 2 例、infusion reaction が 3 例(軽度 2 例、中等度 1 例)に認めら
れた。また、重篤な有害事象は 4 例で認められ、本剤及び CY の最終投与から 1 週間後に発
熱性好中球減少症を発現した 1 例、重篤な好中球減少症を発現した 2 例、治療の 5 カ月後に
重篤な壊疽性筋膜炎及び敗血症が発現した 1 例であった。
8) Vigna-Perez M, et al. Clinical and immunological effects of Rituximab in patients with lupus
nephritis refractory to conventional therapy: a pilot study. Arthritis Res Ther 2006; 8: R83. 28)
既存治療に抵抗性を示し、WHO 分類に基づき活動性ループス腎炎と診断された 22 例(9
~56 歳、Class III:2 例、Class IV:18 例、Class V:2 例)が非盲検試験に組み入れられた。
免疫抑制剤による治療が全例で継続され、本剤は 500~1,000 mg を day 1 及び day 15 に 2 回投
与した。
CR は、尿蛋白が 0.5 g/日未満、血清クレアチニン値の正常化及び尿沈渣が正常の場合とし、
PR は試験開始時に異常を認めた腎機能評価項目が 40%を超えて改善した場合と定義した。
12