よむ、つかう、まなぶ。
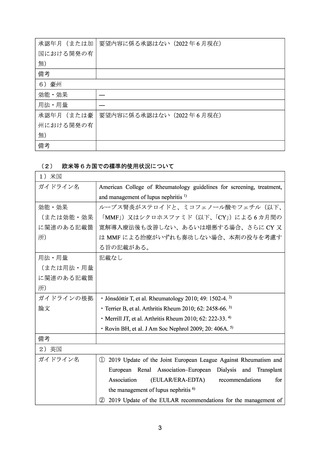
資料3-1 リツキシマブ(遺伝子組換え) (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00026.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第54回 2/15)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
例〉)
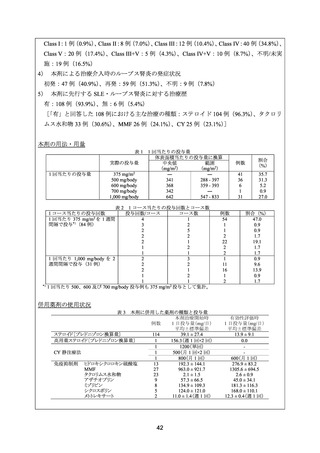
。用法・用量は、本剤 1,000 mg 又はプラセボを Day 1、15、168 及び 182 に投与するこ
ととされた。MMF は 1,500 mg/日から開始し、忍容性を確認しながら 4 週後までに 3,000 mg/
日に増量し、52 週まで投与を継続した。メチルプレドニゾロン 1,000 mg を Day 1 に静脈内投
与し、3 日以内に再投与した。また、infusion reaction の予防のため、Day 15、168 及び 182 の
治験薬投与の前には、メチルプレドニゾロン 100 mg を静脈内投与した。経口プレドニゾンは、
0.75 mg/kg/日(最大 60 mg)を Day 16 まで継続した後、16 週までに 10 mg/日以下に漸減した。
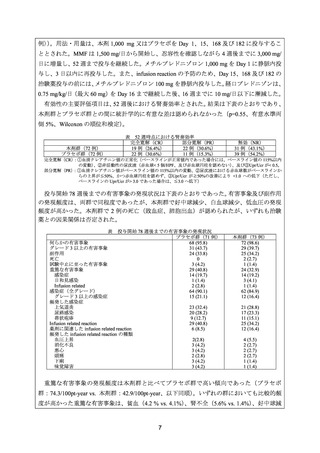
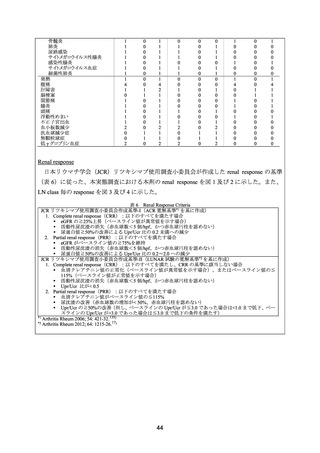
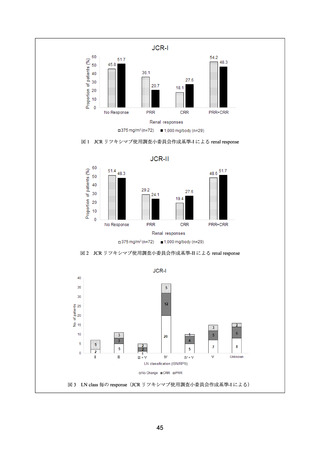
有効性の主要評価項目は、52 週後における腎奏効率とされた。結果は下表のとおりであり、
本剤群とプラセボ群との間に統計学的に有意な差は認められなかった(p=0.55、有意水準両
側 5%、Wilcoxon の順位和検定)。
表
本剤群(72 例)
プラセボ群(72 例)
52 週時点における腎奏効率
完全寛解(CR)
部分寛解(PR)
19 例(26.4%)
22 例(30.6%)
22 例(30.6%)
11 例(15.3%)
無効(NR)
31 例(43.1%)
39 例(54.2%)
完全寛解(CR)
:①血清クレアチニン値の正常化(ベースラインが正常値内であった場合には、ベースライン値の 115%以内
の変動)、②非活動性の尿沈渣(赤血球< 5 個/HPF、及び赤血球円柱を認めない)、及び③Upr/Ucr が< 0.5。
部分寛解(PR)
:①血清クレアチニン値がベースライン値の 115%以内の変動、②尿沈渣における赤血球数がベースラインか
らの上昇が≦50%、かつ赤血球円柱を認めず、③Upr/Ucr が≧50%の改善により <1.0 への低下(ただし、
ベースラインの Upr/Ucr が> 3.0 であった場合は、≦3.0 へ低下)
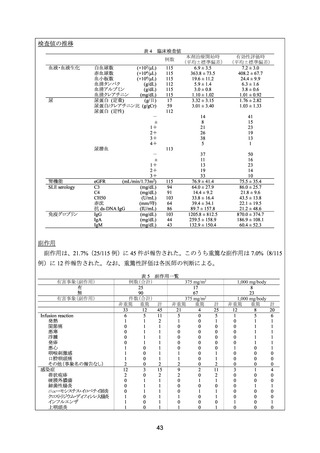
投与開始 78 週後までの有害事象の発現状況は下表のとおりであった。有害事象及び副作用
の発現頻度は、両群で同程度であったが、本剤群で好中球減少、白血球減少、低血圧の発現
頻度が高かった。本剤群で 2 例の死亡(敗血症、肺胞出血)が認められたが、いずれも治験
薬との因果関係は否定された。
表
投与開始 78 週後までの有害事象の発現状況
プラセボ群(71 例)
68 (95.8)
31 (43.7)
24 (33.8)
0
3 (4.2)
29 (40.8)
14 (19.7)
1 (1.4)
2 (2.8)
64 (90.1)
15 (21.1)
何らかの有害事象
グレード 3 以上の有害事象
副作用
死亡
試験中止に至った有害事象
重篤な有害事象
感染症
日和見感染
Infusion related
感染症(全グレード)
グレード 3 以上の感染症
頻発した感染症
上気道炎
尿路感染
帯状疱疹
Infusion related reaction
薬剤に関連した infusion related reaction
頻発した infusion related reaction の種類
血圧上昇
消化不良
悪心
頭痛
下痢
味覚障害
本剤群(73 例)
72 (98.6)
29 (39.7)
25 (34.2)
2 (2.7)
1 (1.4)
24 (32.9)
14 (19.2)
3 (4.1)
1 (1.4)
62 (84.9)
12 (16.4)
23 (32.4)
20 (28.2)
9 (12.7)
29 (40.8)
6 (8.5)
21 (28.8)
17 (23.3)
11 (15.1)
25 (34.2)
12 (16.4)
2(2.8)
3 (4.2)
3 (4.2)
2 (2.8)
3 (4.2)
3 (4.2)
4 (5.5)
2 (2.7)
2 (2.7)
2 (2.7)
1 (1.4)
1 (1.4)
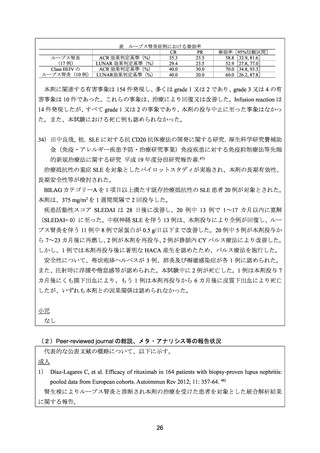
重篤な有害事象の発現頻度は本剤群と比べてプラセボ群で高い傾向であった(プラセボ
群:74.3/100pt-year vs. 本剤群:42.9/100pt-year、以下同順)
。いずれの群においても比較的頻
度が高かった重篤な有害事象は、貧血(4.2 % vs. 4.1%)
、腎不全(5.6% vs. 1.4%)
、好中球減
7
。用法・用量は、本剤 1,000 mg 又はプラセボを Day 1、15、168 及び 182 に投与するこ
ととされた。MMF は 1,500 mg/日から開始し、忍容性を確認しながら 4 週後までに 3,000 mg/
日に増量し、52 週まで投与を継続した。メチルプレドニゾロン 1,000 mg を Day 1 に静脈内投
与し、3 日以内に再投与した。また、infusion reaction の予防のため、Day 15、168 及び 182 の
治験薬投与の前には、メチルプレドニゾロン 100 mg を静脈内投与した。経口プレドニゾンは、
0.75 mg/kg/日(最大 60 mg)を Day 16 まで継続した後、16 週までに 10 mg/日以下に漸減した。
有効性の主要評価項目は、52 週後における腎奏効率とされた。結果は下表のとおりであり、
本剤群とプラセボ群との間に統計学的に有意な差は認められなかった(p=0.55、有意水準両
側 5%、Wilcoxon の順位和検定)。
表
本剤群(72 例)
プラセボ群(72 例)
52 週時点における腎奏効率
完全寛解(CR)
部分寛解(PR)
19 例(26.4%)
22 例(30.6%)
22 例(30.6%)
11 例(15.3%)
無効(NR)
31 例(43.1%)
39 例(54.2%)
完全寛解(CR)
:①血清クレアチニン値の正常化(ベースラインが正常値内であった場合には、ベースライン値の 115%以内
の変動)、②非活動性の尿沈渣(赤血球< 5 個/HPF、及び赤血球円柱を認めない)、及び③Upr/Ucr が< 0.5。
部分寛解(PR)
:①血清クレアチニン値がベースライン値の 115%以内の変動、②尿沈渣における赤血球数がベースラインか
らの上昇が≦50%、かつ赤血球円柱を認めず、③Upr/Ucr が≧50%の改善により <1.0 への低下(ただし、
ベースラインの Upr/Ucr が> 3.0 であった場合は、≦3.0 へ低下)
投与開始 78 週後までの有害事象の発現状況は下表のとおりであった。有害事象及び副作用
の発現頻度は、両群で同程度であったが、本剤群で好中球減少、白血球減少、低血圧の発現
頻度が高かった。本剤群で 2 例の死亡(敗血症、肺胞出血)が認められたが、いずれも治験
薬との因果関係は否定された。
表
投与開始 78 週後までの有害事象の発現状況
プラセボ群(71 例)
68 (95.8)
31 (43.7)
24 (33.8)
0
3 (4.2)
29 (40.8)
14 (19.7)
1 (1.4)
2 (2.8)
64 (90.1)
15 (21.1)
何らかの有害事象
グレード 3 以上の有害事象
副作用
死亡
試験中止に至った有害事象
重篤な有害事象
感染症
日和見感染
Infusion related
感染症(全グレード)
グレード 3 以上の感染症
頻発した感染症
上気道炎
尿路感染
帯状疱疹
Infusion related reaction
薬剤に関連した infusion related reaction
頻発した infusion related reaction の種類
血圧上昇
消化不良
悪心
頭痛
下痢
味覚障害
本剤群(73 例)
72 (98.6)
29 (39.7)
25 (34.2)
2 (2.7)
1 (1.4)
24 (32.9)
14 (19.2)
3 (4.1)
1 (1.4)
62 (84.9)
12 (16.4)
23 (32.4)
20 (28.2)
9 (12.7)
29 (40.8)
6 (8.5)
21 (28.8)
17 (23.3)
11 (15.1)
25 (34.2)
12 (16.4)
2(2.8)
3 (4.2)
3 (4.2)
2 (2.8)
3 (4.2)
3 (4.2)
4 (5.5)
2 (2.7)
2 (2.7)
2 (2.7)
1 (1.4)
1 (1.4)
重篤な有害事象の発現頻度は本剤群と比べてプラセボ群で高い傾向であった(プラセボ
群:74.3/100pt-year vs. 本剤群:42.9/100pt-year、以下同順)
。いずれの群においても比較的頻
度が高かった重篤な有害事象は、貧血(4.2 % vs. 4.1%)
、腎不全(5.6% vs. 1.4%)
、好中球減
7