よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1019KB] (27 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44308.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
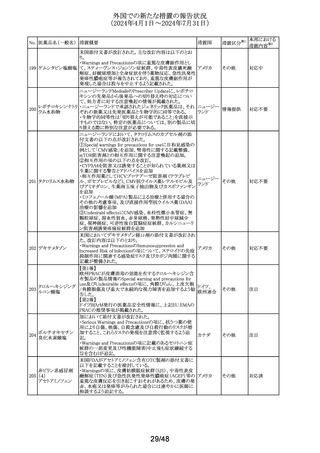
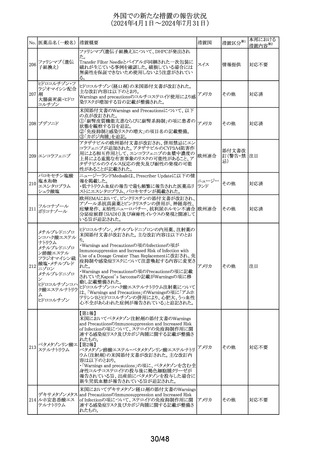
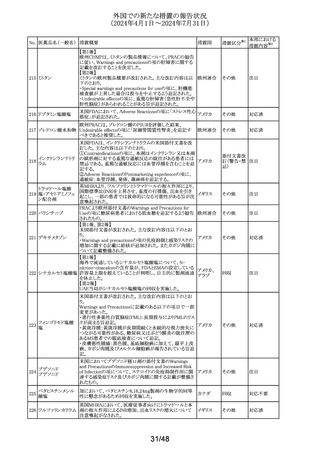
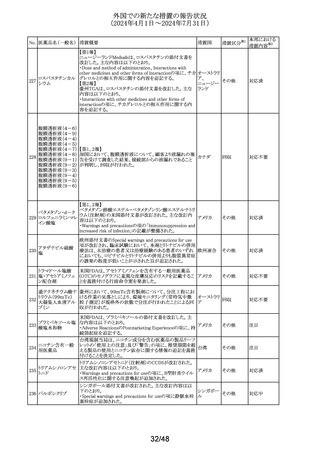
外国での新たな措置の報告状況
(2024年4月1日~2024年7月31日)
措置区分※1
本邦における
措置内容※2
その他
注目
その他
注目
その他
対応済
回収
注目
その他
対応中
情報提供
対応不要
その他
対応済
加において添付文書が改訂された。
ダントロレンナトリウ
・Warning and precautionsの項に、注射剤で肝不全を含む カナダ
ム水和物
肝機能障害が追記された。
その他
注目
【第1、2報】
トリアムシノロンアセトニド(注射剤)の米国添付文書が改訂
された。主な改訂内容は以下のとおり。
トリアムシノロンアセ ・Warnings and precautionsの項のアムホテリシンBとヒドロコ
188
アメリカ
トニド
ルチゾンの併用により心肥大とうっ血性心不全を起こした症
例が報告されている旨の記載が整備された。
・Warnings and precautionsの項の「Immunosuppression and
increased risk of infection」の項の記載が整備された。
その他
対応済
加HCにおいて、ベンジルペニシリンベンザチン水和物の製
ベンジルペニシリン 品モノグラフの改訂情報が掲載された。改訂内容は、
カナダ
ベンザチン水和物 Warnings and Precautionsにコーニス症候群が追記されたと
いうもの。
その他
対応中
No. 医薬品名(一般名) 措置概要
措置国
欧州EMA-PRACは、レボフロキサシン(静注及び経口製
剤)の定期的安全性報告について、使用に伴う骨髄機能不
全、ミオクローヌス、躁病、及び皮膚色素過剰のリスクにつ
レボフロキサシン水
180
いて検討し、事象の発現との因果関係がある可能性は否定 欧州連合
和物
できないと評価した。これによりPRACは、レボフロキサシン
の販売承認取得者に対して、本年9月12日までに変更届を
提出し、製品安全性情報を改訂するよう勧告した。
エチニルエストラジオール/etonogestrelの膣リングについ
て、米国添付文書が改訂された。
レボノルゲストレル・
主な改訂の内容は以下のとおり。
エチニルエストラジ
・Warnings and Precautions、Drug Interactionsの項におい
オール
て、ALT上昇のリスクにより併用を禁忌とするHCV治療薬と アメリカ
181
ノルエチステロン・
してオムビタスビル/パリタプレビル/リトナビルの併用が追
エチニルエストラジ
記された。
オール
・Adverse Reactionsの項に遺伝性及び後天性血管性浮腫
について追記された。
プレドニゾロン含有製剤の米国添付文書が改訂された。主
プレドニゾロン
な改訂内容は以下のとおり。
クロラムフェニコー ・Warnings and Precautionsの項の「Immunosuppression and
182 ル・フラジオマイシ Increased Risk of Infection」が改訂され、プレドニゾロン含 アメリカ
ン硫酸塩・プレドニ 有製剤を含むコルチコステロイドは免疫系を抑制し、感染
ゾロン配合剤
のリスクを高めることが追記され、具体的な感染症の記載が
整備された。
【第1報、第2報、第3報】
リザトリプタン安息香 米国FDAは、リザトリプタンに許容摂取量限度値を超えるニ
183
アメリカ
酸塩
トロソアミン不純物が含まれていることが判明したため一部
の製品で回収を行うことを公表した。
184 炭酸リチウム
欧州PRACは以下について製品情報を改訂する必要がある
と勧告し、CMDhが合意した。
・ブルガダ症候群、副甲状腺機能亢進症、高カルシウム血
欧州連合
症、副甲状腺腺腫、副甲状腺過形成、トピラマートとの薬物
相互作用、減量手術後の毒性、好酸球増加と全身症状を
伴う薬物反応(DRESS)
核酸同定・一般細
菌キット
核酸同定・ブドウ球 対象製品において、特定の血液培養ボトルの特定ロットと
組み合わせて使用した場合、特定の細菌の偽陽性の結果
菌キット
核酸同定・真菌キッ が出るリスクが高まることがわかった。偽陽性結果により、患
者への治療方針が不適切に変更される可能性がある。これ
ト
185 バンコマイシン耐性 により、対象製品の全ての納品先である医療機関等へ、カ アメリカ
スタマーレターを配布し、対象製品で当該血液培養ボトル
遺伝子キット
β-ラクタマーゼ遺 の対象ロットを用いて検査する場合、特定の細菌の陽性結
果は、検査結果を報告する前に他法で確認するよう注意喚
伝子キット
コリスチン耐性遺伝 起する。現在、本事象の原因を調査中である。
子キット
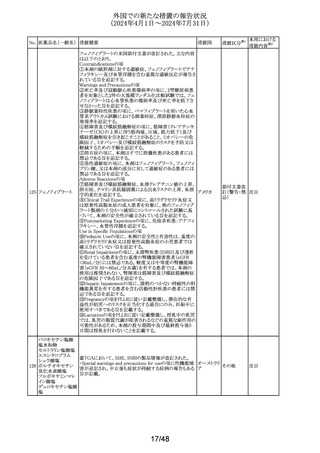
RM-1929/ASP-1929試験の治験薬概要書が変更された。
セツキシマブ サロ 主な変更内容は以下のとおり。
186 タロカンナトリウム
・Identified and Potential Risksの項において、舌腫脹、喉 アメリカ
(遺伝子組換え)
頭腫脹の発現率が高頻度又は10%超である旨が追記され
た。
187
189
27/48
(2024年4月1日~2024年7月31日)
措置区分※1
本邦における
措置内容※2
その他
注目
その他
注目
その他
対応済
回収
注目
その他
対応中
情報提供
対応不要
その他
対応済
加において添付文書が改訂された。
ダントロレンナトリウ
・Warning and precautionsの項に、注射剤で肝不全を含む カナダ
ム水和物
肝機能障害が追記された。
その他
注目
【第1、2報】
トリアムシノロンアセトニド(注射剤)の米国添付文書が改訂
された。主な改訂内容は以下のとおり。
トリアムシノロンアセ ・Warnings and precautionsの項のアムホテリシンBとヒドロコ
188
アメリカ
トニド
ルチゾンの併用により心肥大とうっ血性心不全を起こした症
例が報告されている旨の記載が整備された。
・Warnings and precautionsの項の「Immunosuppression and
increased risk of infection」の項の記載が整備された。
その他
対応済
加HCにおいて、ベンジルペニシリンベンザチン水和物の製
ベンジルペニシリン 品モノグラフの改訂情報が掲載された。改訂内容は、
カナダ
ベンザチン水和物 Warnings and Precautionsにコーニス症候群が追記されたと
いうもの。
その他
対応中
No. 医薬品名(一般名) 措置概要
措置国
欧州EMA-PRACは、レボフロキサシン(静注及び経口製
剤)の定期的安全性報告について、使用に伴う骨髄機能不
全、ミオクローヌス、躁病、及び皮膚色素過剰のリスクにつ
レボフロキサシン水
180
いて検討し、事象の発現との因果関係がある可能性は否定 欧州連合
和物
できないと評価した。これによりPRACは、レボフロキサシン
の販売承認取得者に対して、本年9月12日までに変更届を
提出し、製品安全性情報を改訂するよう勧告した。
エチニルエストラジオール/etonogestrelの膣リングについ
て、米国添付文書が改訂された。
レボノルゲストレル・
主な改訂の内容は以下のとおり。
エチニルエストラジ
・Warnings and Precautions、Drug Interactionsの項におい
オール
て、ALT上昇のリスクにより併用を禁忌とするHCV治療薬と アメリカ
181
ノルエチステロン・
してオムビタスビル/パリタプレビル/リトナビルの併用が追
エチニルエストラジ
記された。
オール
・Adverse Reactionsの項に遺伝性及び後天性血管性浮腫
について追記された。
プレドニゾロン含有製剤の米国添付文書が改訂された。主
プレドニゾロン
な改訂内容は以下のとおり。
クロラムフェニコー ・Warnings and Precautionsの項の「Immunosuppression and
182 ル・フラジオマイシ Increased Risk of Infection」が改訂され、プレドニゾロン含 アメリカ
ン硫酸塩・プレドニ 有製剤を含むコルチコステロイドは免疫系を抑制し、感染
ゾロン配合剤
のリスクを高めることが追記され、具体的な感染症の記載が
整備された。
【第1報、第2報、第3報】
リザトリプタン安息香 米国FDAは、リザトリプタンに許容摂取量限度値を超えるニ
183
アメリカ
酸塩
トロソアミン不純物が含まれていることが判明したため一部
の製品で回収を行うことを公表した。
184 炭酸リチウム
欧州PRACは以下について製品情報を改訂する必要がある
と勧告し、CMDhが合意した。
・ブルガダ症候群、副甲状腺機能亢進症、高カルシウム血
欧州連合
症、副甲状腺腺腫、副甲状腺過形成、トピラマートとの薬物
相互作用、減量手術後の毒性、好酸球増加と全身症状を
伴う薬物反応(DRESS)
核酸同定・一般細
菌キット
核酸同定・ブドウ球 対象製品において、特定の血液培養ボトルの特定ロットと
組み合わせて使用した場合、特定の細菌の偽陽性の結果
菌キット
核酸同定・真菌キッ が出るリスクが高まることがわかった。偽陽性結果により、患
者への治療方針が不適切に変更される可能性がある。これ
ト
185 バンコマイシン耐性 により、対象製品の全ての納品先である医療機関等へ、カ アメリカ
スタマーレターを配布し、対象製品で当該血液培養ボトル
遺伝子キット
β-ラクタマーゼ遺 の対象ロットを用いて検査する場合、特定の細菌の陽性結
果は、検査結果を報告する前に他法で確認するよう注意喚
伝子キット
コリスチン耐性遺伝 起する。現在、本事象の原因を調査中である。
子キット
RM-1929/ASP-1929試験の治験薬概要書が変更された。
セツキシマブ サロ 主な変更内容は以下のとおり。
186 タロカンナトリウム
・Identified and Potential Risksの項において、舌腫脹、喉 アメリカ
(遺伝子組換え)
頭腫脹の発現率が高頻度又は10%超である旨が追記され
た。
187
189
27/48