よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1019KB] (43 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44308.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
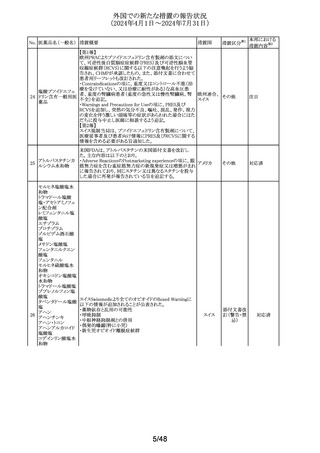
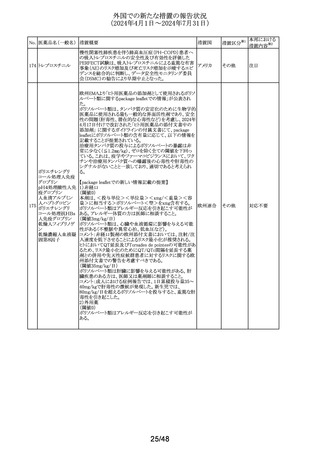
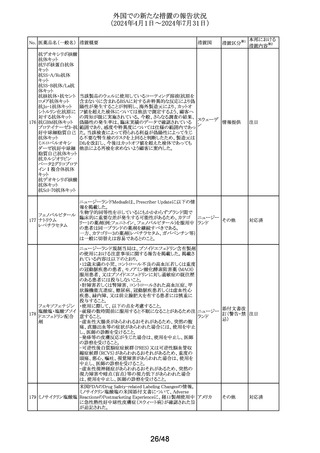
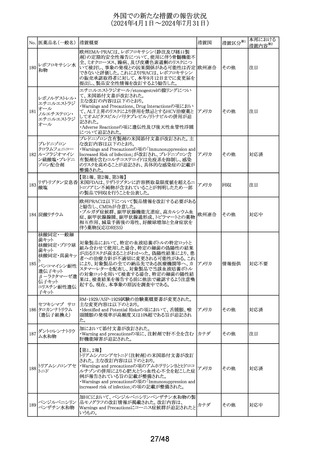
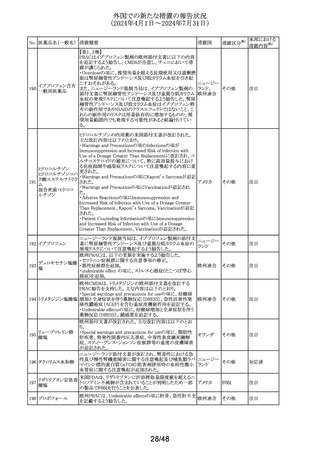
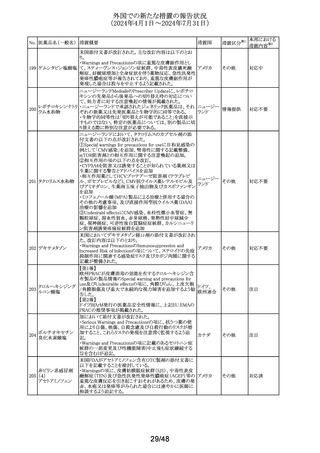
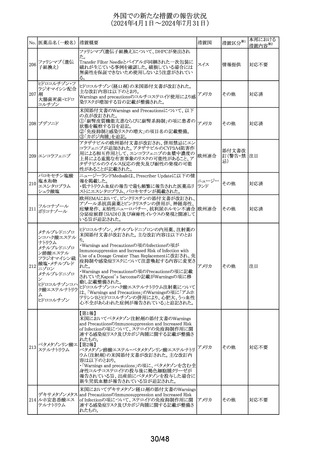
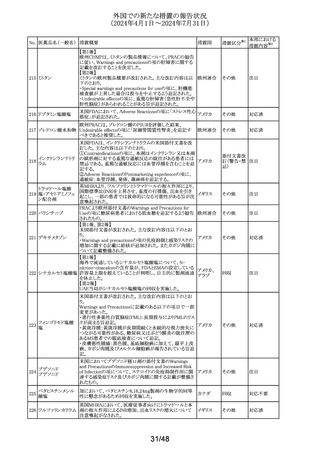
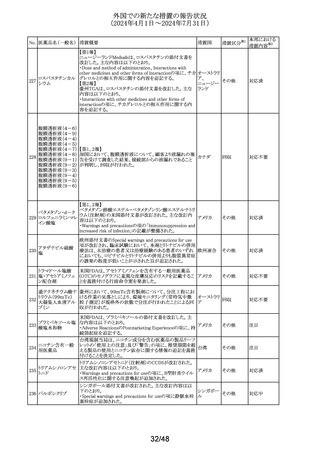
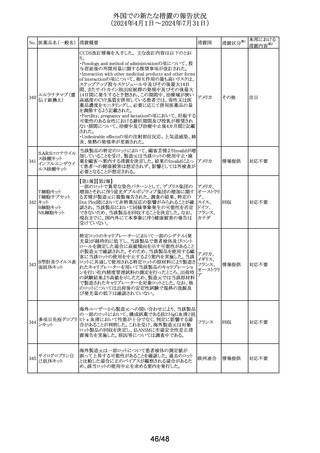
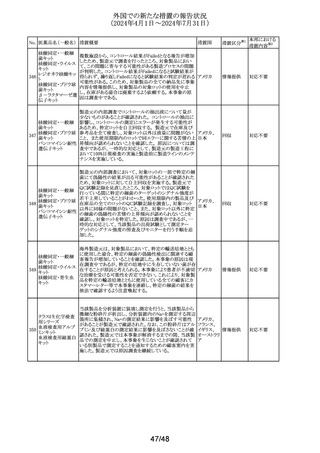
外国での新たな措置の報告状況
(2024年4月1日~2024年7月31日)
No. 医薬品名(一般名) 措置概要
318 ザルトプロフェン
319
アモキシシリン水和
物
320 ドンペリドン
措置区分※1
本邦における
措置内容※2
その他
対応済
オーストラリ
その他
ア
対応中
措置国
韓国において、ザルトプロフェンの添付文書が改訂された。
改訂内容は以下のとおり。
・Use in pregnant and Lactating womenの項において、羊水
過少症につながる胎児の腎機能障害が発現する可能性が 韓国
ある旨、本剤の投与が必要と判断された場合には必要最小
限の使用にとどめる旨、投与が48時間を超える場合は羊水
の超音波モニタリングを考慮する旨等を追記する。
アモキシシリン含有製剤の豪州添付文書が改訂された。改
訂内容は以下のとおり。
<アモキシシリン>
・Adverse effects (undesirable effects)に、対称性薬剤性間
擦性及び屈側部発疹(SDRIFE)(バブーン症候群) が追記
された。
<アモキシシリン・クラブラン酸カリウム>
・Special warnings and precautions for useに、コーニス症候
群、薬剤性腸炎症候群(DIES)が追記された。また、結晶尿
に関して急性腎障害が含められる内容に更新された。
・Adverse effects (undesirable effects)に、コーニス症候群、
DIES、膵炎、線状IgA病が追記された。
中国のPeriodic Safety Update Reportにおいて、2019~
2020年に実施された各国の安全対策措置について記載さ
れている。
①スイスにおいて、ドンペリドンのQT延長及び不整脈リスク
により、調剤カテゴリーC(調剤のみ;処方せんなし)からカテ
ゴリーBに再分類した(調剤は文書化しなければならない;薬
剤師又は医師に相談する必要がある;処方せんなし)。
中国
②スイス、サウジアラビアにおいて、小児の適応を削除し、
12歳以上で体重35kg以上の成人及び青年に限定。
③ヨルダン、エジプト、スペインにおいて、小児適応の削除
及び不整脈に関する再周知を実施した。
④香港において、成人及び12歳以上の青少年(体重35kg
以上)について、最低有効量を最短投与期間として使用す
るよう注意喚起した。
クラリスロマイシン
トラマドール塩酸
塩・アセトアミノフェ
ン配合剤
バルサルタン・アム
【第1報、第2報】
ロジピンベシル酸塩
欧州EMAは、ヒト用医薬品中のニトロソアミン不純物に係る
配合剤
321
意見書に関する販売承認取得者/申請者向けQ&Aを更新 欧州連合
バルサルタン
し、各物質固有の一日許容摂取量とCPCA categoryを更新
バルサルタン・ヒドロ
した。
クロロチアジド配合
剤
デキストロメトルファ
ン臭化水素酸塩水
和物
情報提供
注目
その他
注目
【第1報、第2報】
アモキシシリン・クラブラン酸カリウムの豪州添付文書が改
訂された。改訂内容は以下のとおり。
アモキシシリン水和 ・Special warnings and precautions for useに、コーニス症候 オーストラリ
322
その他
群、薬剤性腸炎症候群(DIES)が追記。また、結晶尿に関し ア
物
て急性腎障害が含められる内容に更新。
・Adverse effects (undesirable effects)に、コーニス症候群、
DIES、膵炎、線状IgA病が追記。
アガルシダーゼ ベータの米国添付文書が改訂された。主
アガルシダーゼ
な改訂内容は以下のとおり。
アメリカ
323 ベータ(遺伝子組換
・Boxed warningの項にアナフィラキシーについての記載が
え)[後続1]
追加された。
セベリパーゼ アルファの米国添付文書が改訂された。主
セベリパーゼ アル
な改訂内容は以下のとおり。
324 ファ(遺伝子組換
アメリカ
・Boxed warningの項にアナフィラキシーについての記載が
え)
追加された。
43/48
対応中
添付文書改
訂(警告・禁 対応済
忌)
添付文書改
訂(警告・禁 対応済
忌)
(2024年4月1日~2024年7月31日)
No. 医薬品名(一般名) 措置概要
318 ザルトプロフェン
319
アモキシシリン水和
物
320 ドンペリドン
措置区分※1
本邦における
措置内容※2
その他
対応済
オーストラリ
その他
ア
対応中
措置国
韓国において、ザルトプロフェンの添付文書が改訂された。
改訂内容は以下のとおり。
・Use in pregnant and Lactating womenの項において、羊水
過少症につながる胎児の腎機能障害が発現する可能性が 韓国
ある旨、本剤の投与が必要と判断された場合には必要最小
限の使用にとどめる旨、投与が48時間を超える場合は羊水
の超音波モニタリングを考慮する旨等を追記する。
アモキシシリン含有製剤の豪州添付文書が改訂された。改
訂内容は以下のとおり。
<アモキシシリン>
・Adverse effects (undesirable effects)に、対称性薬剤性間
擦性及び屈側部発疹(SDRIFE)(バブーン症候群) が追記
された。
<アモキシシリン・クラブラン酸カリウム>
・Special warnings and precautions for useに、コーニス症候
群、薬剤性腸炎症候群(DIES)が追記された。また、結晶尿
に関して急性腎障害が含められる内容に更新された。
・Adverse effects (undesirable effects)に、コーニス症候群、
DIES、膵炎、線状IgA病が追記された。
中国のPeriodic Safety Update Reportにおいて、2019~
2020年に実施された各国の安全対策措置について記載さ
れている。
①スイスにおいて、ドンペリドンのQT延長及び不整脈リスク
により、調剤カテゴリーC(調剤のみ;処方せんなし)からカテ
ゴリーBに再分類した(調剤は文書化しなければならない;薬
剤師又は医師に相談する必要がある;処方せんなし)。
中国
②スイス、サウジアラビアにおいて、小児の適応を削除し、
12歳以上で体重35kg以上の成人及び青年に限定。
③ヨルダン、エジプト、スペインにおいて、小児適応の削除
及び不整脈に関する再周知を実施した。
④香港において、成人及び12歳以上の青少年(体重35kg
以上)について、最低有効量を最短投与期間として使用す
るよう注意喚起した。
クラリスロマイシン
トラマドール塩酸
塩・アセトアミノフェ
ン配合剤
バルサルタン・アム
【第1報、第2報】
ロジピンベシル酸塩
欧州EMAは、ヒト用医薬品中のニトロソアミン不純物に係る
配合剤
321
意見書に関する販売承認取得者/申請者向けQ&Aを更新 欧州連合
バルサルタン
し、各物質固有の一日許容摂取量とCPCA categoryを更新
バルサルタン・ヒドロ
した。
クロロチアジド配合
剤
デキストロメトルファ
ン臭化水素酸塩水
和物
情報提供
注目
その他
注目
【第1報、第2報】
アモキシシリン・クラブラン酸カリウムの豪州添付文書が改
訂された。改訂内容は以下のとおり。
アモキシシリン水和 ・Special warnings and precautions for useに、コーニス症候 オーストラリ
322
その他
群、薬剤性腸炎症候群(DIES)が追記。また、結晶尿に関し ア
物
て急性腎障害が含められる内容に更新。
・Adverse effects (undesirable effects)に、コーニス症候群、
DIES、膵炎、線状IgA病が追記。
アガルシダーゼ ベータの米国添付文書が改訂された。主
アガルシダーゼ
な改訂内容は以下のとおり。
アメリカ
323 ベータ(遺伝子組換
・Boxed warningの項にアナフィラキシーについての記載が
え)[後続1]
追加された。
セベリパーゼ アルファの米国添付文書が改訂された。主
セベリパーゼ アル
な改訂内容は以下のとおり。
324 ファ(遺伝子組換
アメリカ
・Boxed warningの項にアナフィラキシーについての記載が
え)
追加された。
43/48
対応中
添付文書改
訂(警告・禁 対応済
忌)
添付文書改
訂(警告・禁 対応済
忌)