よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1019KB] (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44308.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
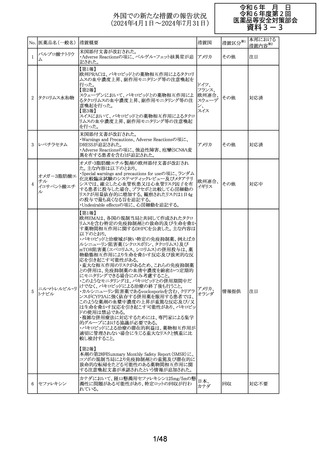
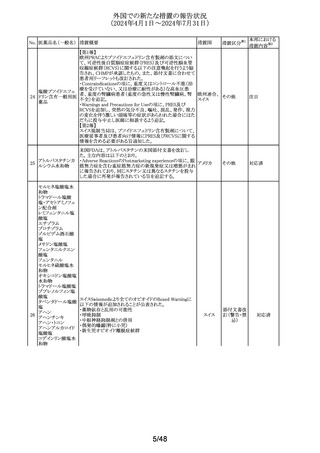
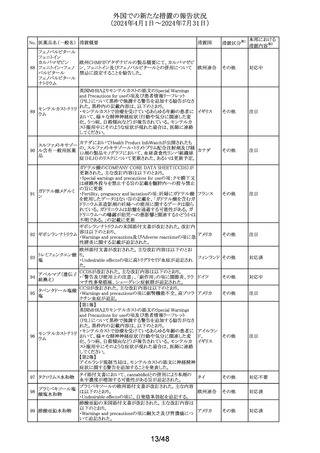
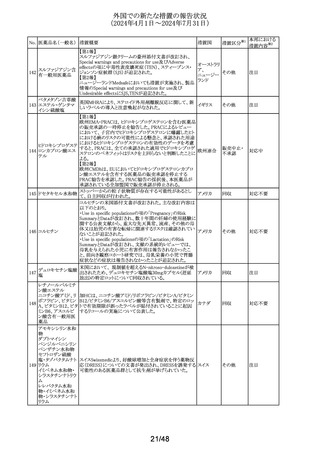
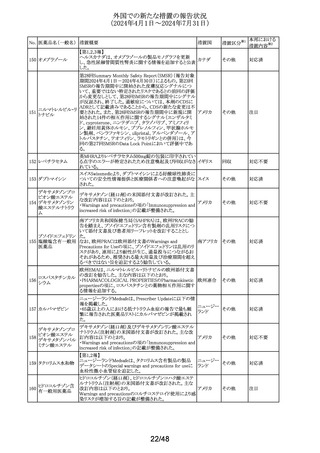
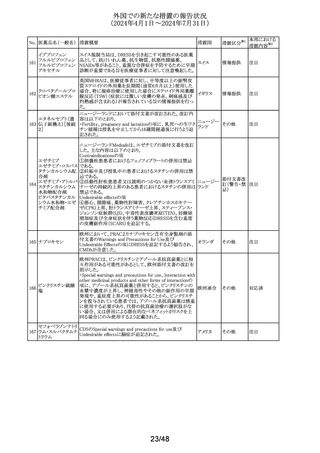
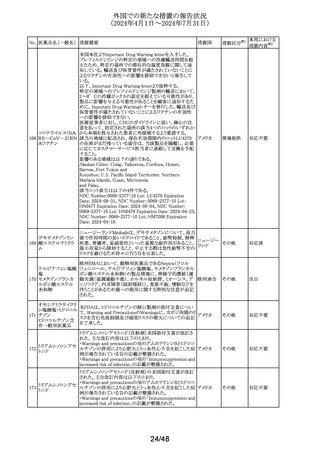
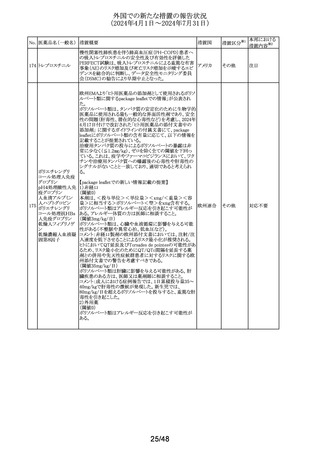
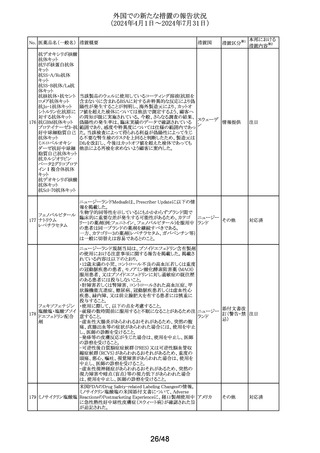
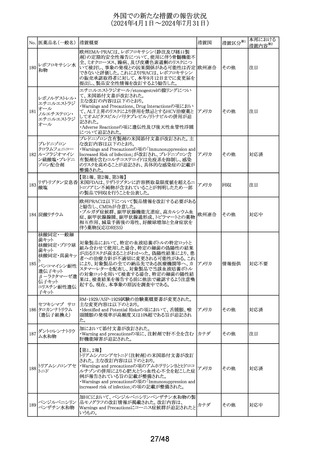
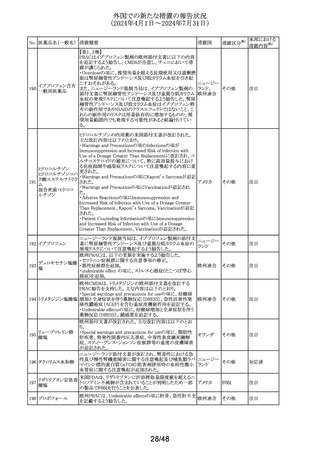
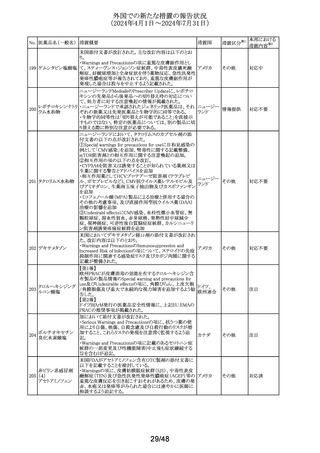
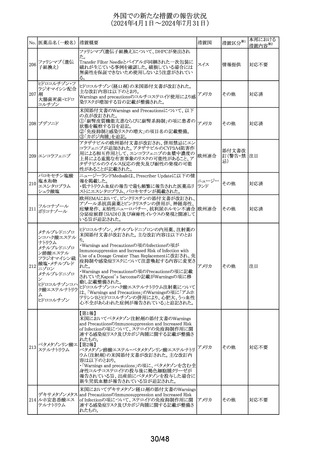
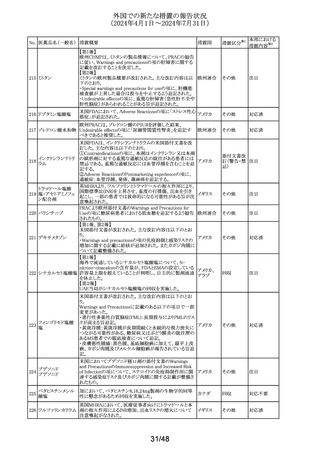
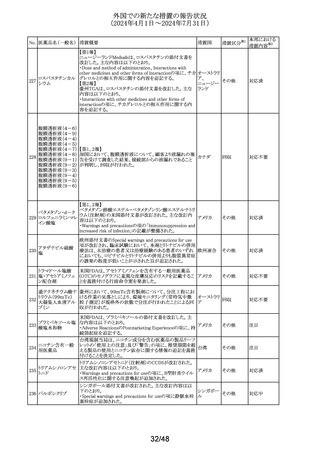
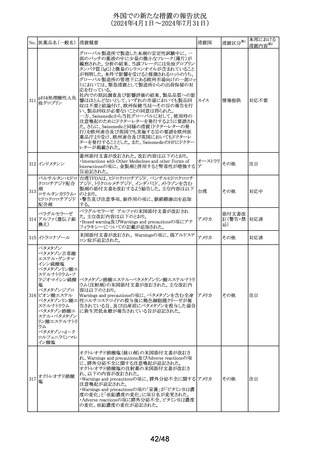
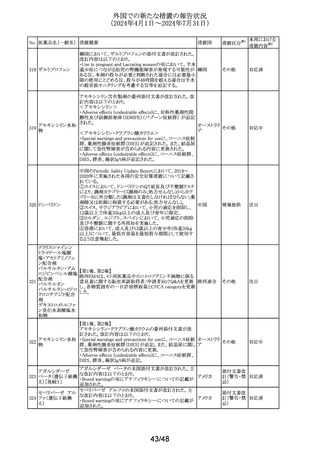
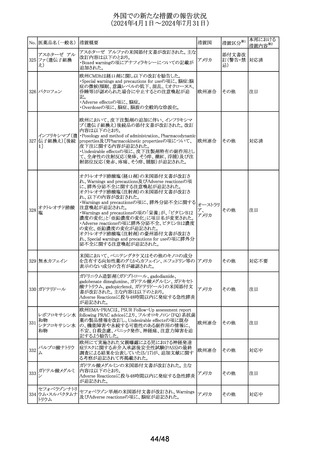
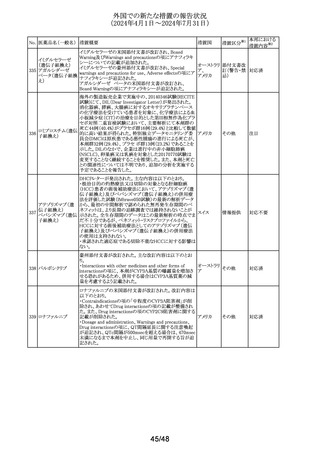
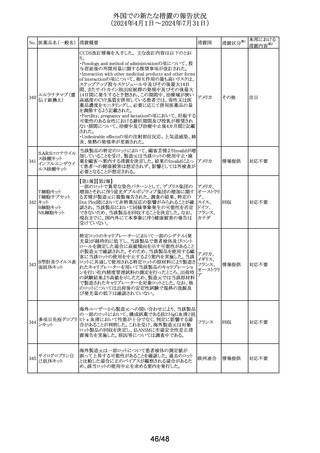
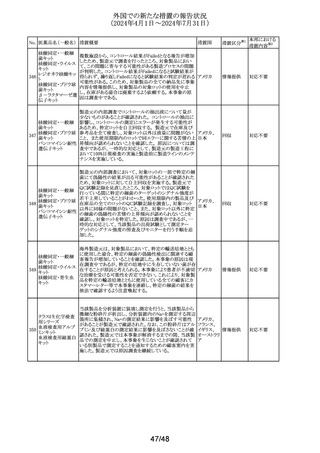
外国での新たな措置の報告状況
(2024年4月1日~2024年7月31日)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
本邦における
措置内容※2
情報提供
注目
その他
対応中
その他
対応済
その他
対応不要
その他
対応済
その他
注目
コデインリン酸塩水
和物(10%)
コデインリン酸塩水
和物(1%以下)
ジヒドロコデインリン
酸塩
ジヒドロコデインリン
酸塩(10%)
ペチジン塩酸塩
ペチジン塩酸塩・レ
バロルファン酒石酸
塩(1)
ペチジン塩酸塩・レ
バロルファン酒石酸
塩(2)
鎮咳配合剤(1)
ジヒドロコデインリン
酸塩含有一般用医
薬品
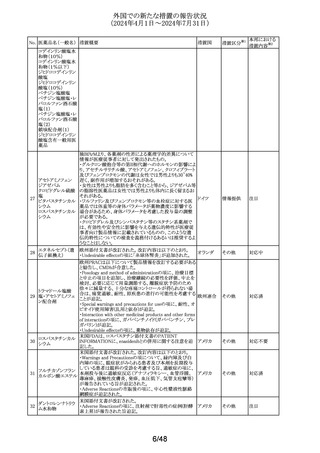
独BfArMより、各薬剤の性差による薬理学的差異について
情報が医療従事者に対して発出されたもの。
・グルクロン酸抱合等の第II相代謝へのホルモンの影響によ
り、アセチルサリチル酸、アセトアミノフェン、クロフィブラート
及びフェンプロクモンの代謝は女性では男性よりも30~40%
遅く、副作用が増加するおそれがある。
アセトアミノフェン
・女性は男性よりも脂肪を多く含むこと等から、ジアゼパム等
ジアゼパム
クロピドグレル硫酸 の脂溶性医薬品は女性では男性よりも体内に長く留まるお
それがある。
塩
27
ドイツ
ピタバスタチンカル ・ワルファリン及びフェンプロクモン等の血栓症に対する医
薬品では体重等の身体パラメータが薬物濃度に影響する
シウム
ロスバスタチンカル 場合があるため、身体パラメータを考慮した投与量の調整
が必要である。
シウム
・クロピドグレル及びシンバスタチン等のスタチン系薬剤で
は、有効性や安全性に影響を与える遺伝的特性が医療従
事者向け製品情報に記載されているものの、このような遺
伝的特性についての検査を義務付けるあるいは推奨するよ
うなことはしない。
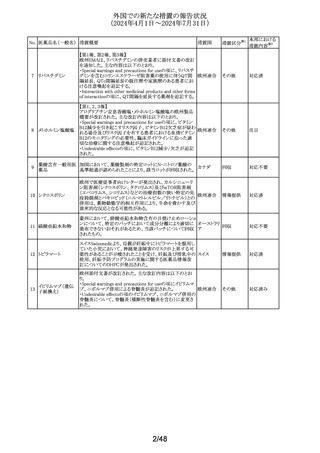
エタネルセプト(遺 欧州添付文書が改訂された。改訂内容は以下のとおり。
28
オランダ
伝子組換え)
・Undesirable effectsの項に「糸球体腎炎」が追加された。
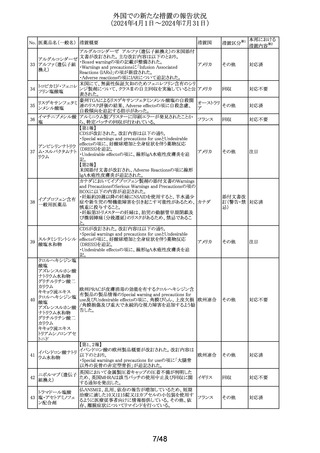
欧州PRACは以下について製品情報を改訂する必要がある
と勧告し、CMDhが合意した。
・Posology and method of administrationの項に、治療目標
と中止の項目を追加し、治療継続の必要性を評価、中止を
検討、必要に応じて用量調節する、離脱症状予防のため
徐々に減量する、十分な疼痛コントロールが得られない場
トラマドール塩酸
合は、痛覚過敏、耐性、原疾患の進行の可能性を考慮する
29 塩・アセトアミノフェ
欧州連合
ことが追記。
ン配合剤
・Special warnings and precautions for useの項に、耐性、オ
ピオイド使用障害(乱用と依存)が追記。
・Interaction with other medicinal products and other forms
of interactionの項に、ガバペンチノイド(ガバペンチン、プレ
ガバリン)が追記。
・Undesirable effectsの項に、薬物依存が追記。
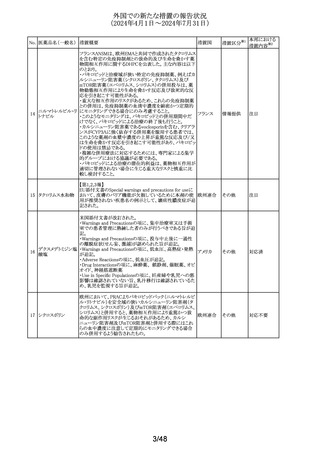
米国FDAは、ロスバスタチン添付文書のPATIENT
ロスバスタチンカル
30
INFORMATIONに、enasidenibとの併用に関する注意を追 アメリカ
シウム
記した。
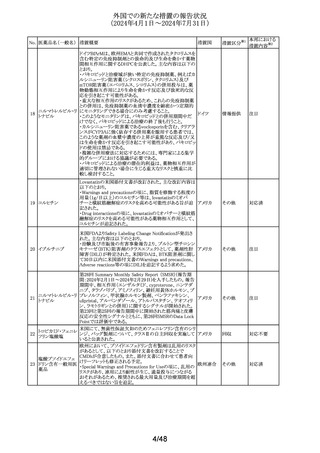
米国添付文書が改訂された。改訂内容は以下のとおり。
・Warnings and Precautionsの項について、緑内障及び白
内障の項に、眼症状がみられる患者及び本剤を長期投与
している患者は眼科の受診を考慮する旨、過敏症の項に、
フルチカゾンフラン
31
本剤投与後に過敏症反応(アナフィラキシー、血管浮腫、 アメリカ
カルボン酸エステル
蕁麻疹、接触性皮膚炎、発疹、血圧低下、気管支痙攣等)
が報告されている旨が追記された。
・Adverse Reactionsの市販後の項に、中心性漿液性脈絡
網膜症が追記された。
米国添付文書が改訂された。
ダントロレンナトリウ
32
・Adverse Reactionsの項に、注射剤で肝毒性の症例(肝酵 アメリカ
ム水和物
素上昇)が報告された旨追記。
6/48
(2024年4月1日~2024年7月31日)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
本邦における
措置内容※2
情報提供
注目
その他
対応中
その他
対応済
その他
対応不要
その他
対応済
その他
注目
コデインリン酸塩水
和物(10%)
コデインリン酸塩水
和物(1%以下)
ジヒドロコデインリン
酸塩
ジヒドロコデインリン
酸塩(10%)
ペチジン塩酸塩
ペチジン塩酸塩・レ
バロルファン酒石酸
塩(1)
ペチジン塩酸塩・レ
バロルファン酒石酸
塩(2)
鎮咳配合剤(1)
ジヒドロコデインリン
酸塩含有一般用医
薬品
独BfArMより、各薬剤の性差による薬理学的差異について
情報が医療従事者に対して発出されたもの。
・グルクロン酸抱合等の第II相代謝へのホルモンの影響によ
り、アセチルサリチル酸、アセトアミノフェン、クロフィブラート
及びフェンプロクモンの代謝は女性では男性よりも30~40%
遅く、副作用が増加するおそれがある。
アセトアミノフェン
・女性は男性よりも脂肪を多く含むこと等から、ジアゼパム等
ジアゼパム
クロピドグレル硫酸 の脂溶性医薬品は女性では男性よりも体内に長く留まるお
それがある。
塩
27
ドイツ
ピタバスタチンカル ・ワルファリン及びフェンプロクモン等の血栓症に対する医
薬品では体重等の身体パラメータが薬物濃度に影響する
シウム
ロスバスタチンカル 場合があるため、身体パラメータを考慮した投与量の調整
が必要である。
シウム
・クロピドグレル及びシンバスタチン等のスタチン系薬剤で
は、有効性や安全性に影響を与える遺伝的特性が医療従
事者向け製品情報に記載されているものの、このような遺
伝的特性についての検査を義務付けるあるいは推奨するよ
うなことはしない。
エタネルセプト(遺 欧州添付文書が改訂された。改訂内容は以下のとおり。
28
オランダ
伝子組換え)
・Undesirable effectsの項に「糸球体腎炎」が追加された。
欧州PRACは以下について製品情報を改訂する必要がある
と勧告し、CMDhが合意した。
・Posology and method of administrationの項に、治療目標
と中止の項目を追加し、治療継続の必要性を評価、中止を
検討、必要に応じて用量調節する、離脱症状予防のため
徐々に減量する、十分な疼痛コントロールが得られない場
トラマドール塩酸
合は、痛覚過敏、耐性、原疾患の進行の可能性を考慮する
29 塩・アセトアミノフェ
欧州連合
ことが追記。
ン配合剤
・Special warnings and precautions for useの項に、耐性、オ
ピオイド使用障害(乱用と依存)が追記。
・Interaction with other medicinal products and other forms
of interactionの項に、ガバペンチノイド(ガバペンチン、プレ
ガバリン)が追記。
・Undesirable effectsの項に、薬物依存が追記。
米国FDAは、ロスバスタチン添付文書のPATIENT
ロスバスタチンカル
30
INFORMATIONに、enasidenibとの併用に関する注意を追 アメリカ
シウム
記した。
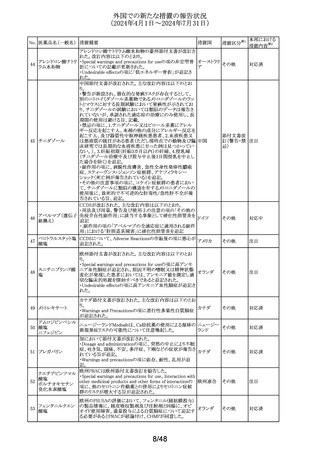
米国添付文書が改訂された。改訂内容は以下のとおり。
・Warnings and Precautionsの項について、緑内障及び白
内障の項に、眼症状がみられる患者及び本剤を長期投与
している患者は眼科の受診を考慮する旨、過敏症の項に、
フルチカゾンフラン
31
本剤投与後に過敏症反応(アナフィラキシー、血管浮腫、 アメリカ
カルボン酸エステル
蕁麻疹、接触性皮膚炎、発疹、血圧低下、気管支痙攣等)
が報告されている旨が追記された。
・Adverse Reactionsの市販後の項に、中心性漿液性脈絡
網膜症が追記された。
米国添付文書が改訂された。
ダントロレンナトリウ
32
・Adverse Reactionsの項に、注射剤で肝毒性の症例(肝酵 アメリカ
ム水和物
素上昇)が報告された旨追記。
6/48