よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1019KB] (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44308.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
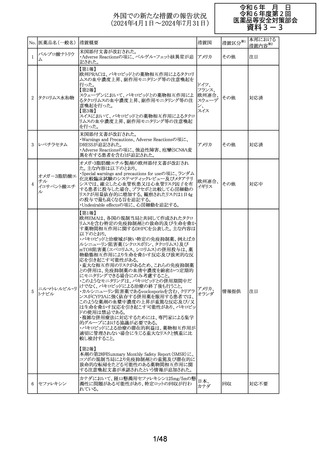
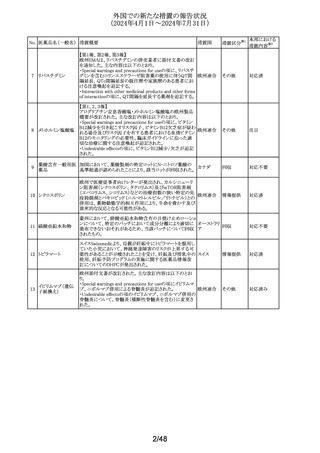
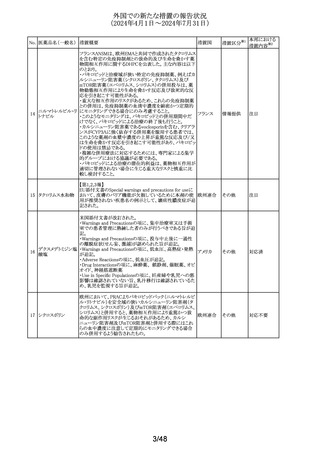
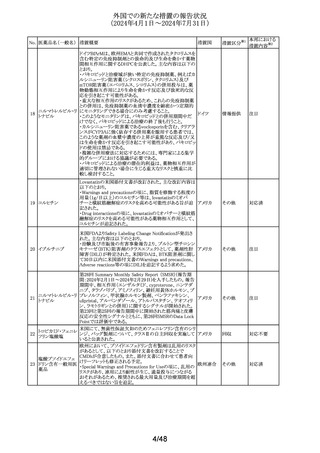
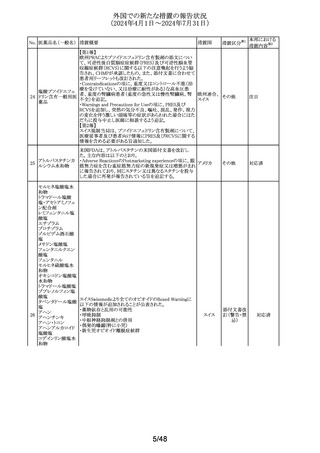
外国での新たな措置の報告状況
(2024年4月1日~2024年7月31日)
措置区分※1
本邦における
措置内容※2
情報提供
注目
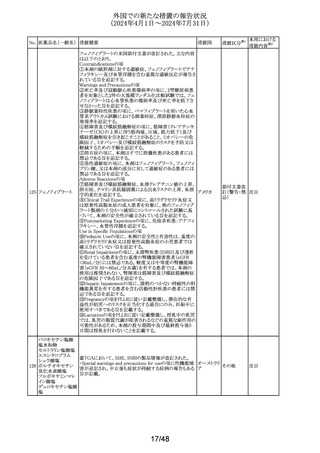
19 コルヒチン
Lovastatinの米国添付文書が改訂された。主な改訂内容は
以下のとおり。
・Warnings and precautionsの項に、脂質を修飾する程度の
用量(1g/日以上)のコルヒチン等は、lovastatinのミオパ
チーと横紋筋融解症のリスクを高める可能性がある旨が追 アメリカ
記された。
・Drug interactionsの項に、lovastatinのミオパチーと横紋筋
融解症のリスクを高める可能性がある薬物相互作用として、
コルヒチンが追記された。
その他
対応済
20 イブルチニブ
米国FDAよりSafety Labeling Change Notificationが発出さ
れた。主な内容は以下のとおり。
・治験及び市販後の有害事象報告より、ブルトン型チロシン
キナーゼ(BTK)阻害剤のクラスエフェクトとして、薬剤性肝 アメリカ
障害(DILI)が特定された。米国FDAは、BTK阻害剤に関し
て30日以内に米国添付文書のWarnings and precautions、
Adverse reactions等の項にDILIを追記するよう求めた。
その他
注目
その他
注目
回収
対応不要
その他
対応済
No. 医薬品名(一般名) 措置概要
措置国
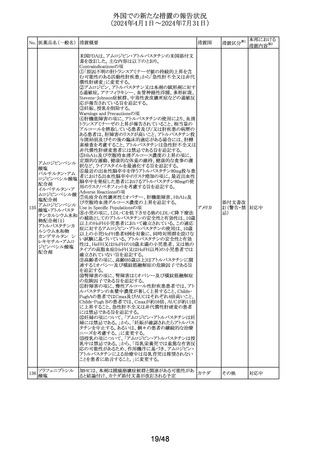
ドイツBfArMは、欧州EMAと共同で作成されたタクロリムスを
含む特定の免疫抑制剤との致命的及び生命を脅かす薬物
間相互作用に関するDHPCを公表した。主な内容は以下の
とおり。
・パキロビッドと治療域が狭い特定の免疫抑制薬、例えばカ
ルシニューリン阻害薬(シクロスポリン、タクロリムス)及び
mTOR阻害薬(エベロリムス、シロリムス)の併用投与は、薬
物動態相互作用により生命を脅かす反応及び致死的な反
応を引き起こす可能性がある。
・重大な相互作用のリスクがあるため、これらの免疫抑制薬
との併用は、免疫抑制薬の血清中濃度を綿密かつ定期的
ニルマトレルビル・リ にモニタリングできる場合にのみ考慮すること。
18
ドイツ
トナビル
・このようなモニタリングは、パキロビッドとの併用期間中だ
けでなく、パキロビッドによる治療の終了後も行うこと。
・カルシニューリン阻害薬であるvoclosporinを含む、クリアラ
ンスがCYP3Aに強く依存する併用薬を服用する患者では、
このような薬剤の血漿中濃度の上昇が重篤な反応及び/又
は生命を脅かす反応を引き起こす可能性があり、パキロビッ
ドの使用は禁忌である。
・複雑な併用療法に対応するためには、専門家による集学
的グループにおける協議が必要である。
・パキロビッドによる治療の潜在的利益は、薬物相互作用が
適切に管理されない場合に生じる重大なリスクと慎重に比
較し検討すること。
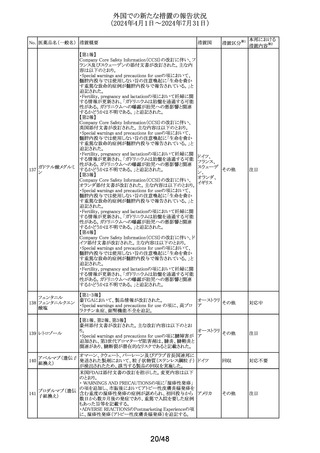
第26回 Summary Monthly Safety Report (SMSR)(報告期
間:2024年2月1日~2024年2月29日)を入手したもの。報告
期間中、相互作用(エンザルタミド、cyproterone、ニンテダ
ニブ、タラゾパリブ、アミノフィリン、避妊用黄体ホルモン、ブ
ニルマトレルビル・リ プレノルフィン、甲状腺ホルモン製剤、ベンラファキシン、
21
アメリカ
トナビル
ulipristal、アルベンダゾール、アトルバスタチン、テオフィリ
ン、ラモトリギンとの併用)に関するシグナルが開始された。
第23回と第25回の報告期間中に開始された筋肉痛と皮膚
反応の安全性シグナルとともに、第26回SMSRのData Lock
Pointでは評価中である。
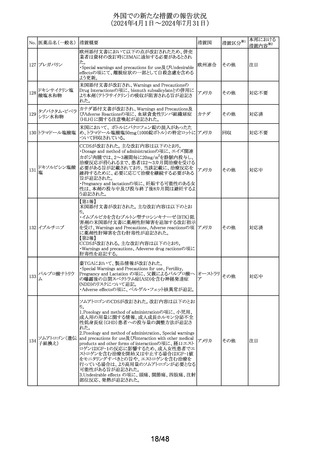
米国にて、無菌性保証欠如のためフェニレフリン含有のシリ
トロピカミド・フェニレ
22
ンジ、バッグ製剤について、クラスⅡの自主回収を実施して アメリカ
フリン塩酸塩
いると公表された。
欧州において、プソイドエフェドリン含有製剤は乱用のリスク
があるとして、以下のとおり添付文書を改訂することで
CMDhが合意したもの。また、添付文書に合わせて患者向
塩酸プソイドエフェ
けリーフレットも修正される予定。
23 ドリン含有一般用医
欧州連合
・Special Warnings and Precautions for Useの項に、乱用の
薬品
リスクがあり、連用により耐性が生じ、過量投与につながる
おそれがあるため、推奨される最大用量及び治療期間を超
えるべきではない旨を追記。
4/48
(2024年4月1日~2024年7月31日)
措置区分※1
本邦における
措置内容※2
情報提供
注目
19 コルヒチン
Lovastatinの米国添付文書が改訂された。主な改訂内容は
以下のとおり。
・Warnings and precautionsの項に、脂質を修飾する程度の
用量(1g/日以上)のコルヒチン等は、lovastatinのミオパ
チーと横紋筋融解症のリスクを高める可能性がある旨が追 アメリカ
記された。
・Drug interactionsの項に、lovastatinのミオパチーと横紋筋
融解症のリスクを高める可能性がある薬物相互作用として、
コルヒチンが追記された。
その他
対応済
20 イブルチニブ
米国FDAよりSafety Labeling Change Notificationが発出さ
れた。主な内容は以下のとおり。
・治験及び市販後の有害事象報告より、ブルトン型チロシン
キナーゼ(BTK)阻害剤のクラスエフェクトとして、薬剤性肝 アメリカ
障害(DILI)が特定された。米国FDAは、BTK阻害剤に関し
て30日以内に米国添付文書のWarnings and precautions、
Adverse reactions等の項にDILIを追記するよう求めた。
その他
注目
その他
注目
回収
対応不要
その他
対応済
No. 医薬品名(一般名) 措置概要
措置国
ドイツBfArMは、欧州EMAと共同で作成されたタクロリムスを
含む特定の免疫抑制剤との致命的及び生命を脅かす薬物
間相互作用に関するDHPCを公表した。主な内容は以下の
とおり。
・パキロビッドと治療域が狭い特定の免疫抑制薬、例えばカ
ルシニューリン阻害薬(シクロスポリン、タクロリムス)及び
mTOR阻害薬(エベロリムス、シロリムス)の併用投与は、薬
物動態相互作用により生命を脅かす反応及び致死的な反
応を引き起こす可能性がある。
・重大な相互作用のリスクがあるため、これらの免疫抑制薬
との併用は、免疫抑制薬の血清中濃度を綿密かつ定期的
ニルマトレルビル・リ にモニタリングできる場合にのみ考慮すること。
18
ドイツ
トナビル
・このようなモニタリングは、パキロビッドとの併用期間中だ
けでなく、パキロビッドによる治療の終了後も行うこと。
・カルシニューリン阻害薬であるvoclosporinを含む、クリアラ
ンスがCYP3Aに強く依存する併用薬を服用する患者では、
このような薬剤の血漿中濃度の上昇が重篤な反応及び/又
は生命を脅かす反応を引き起こす可能性があり、パキロビッ
ドの使用は禁忌である。
・複雑な併用療法に対応するためには、専門家による集学
的グループにおける協議が必要である。
・パキロビッドによる治療の潜在的利益は、薬物相互作用が
適切に管理されない場合に生じる重大なリスクと慎重に比
較し検討すること。
第26回 Summary Monthly Safety Report (SMSR)(報告期
間:2024年2月1日~2024年2月29日)を入手したもの。報告
期間中、相互作用(エンザルタミド、cyproterone、ニンテダ
ニブ、タラゾパリブ、アミノフィリン、避妊用黄体ホルモン、ブ
ニルマトレルビル・リ プレノルフィン、甲状腺ホルモン製剤、ベンラファキシン、
21
アメリカ
トナビル
ulipristal、アルベンダゾール、アトルバスタチン、テオフィリ
ン、ラモトリギンとの併用)に関するシグナルが開始された。
第23回と第25回の報告期間中に開始された筋肉痛と皮膚
反応の安全性シグナルとともに、第26回SMSRのData Lock
Pointでは評価中である。
米国にて、無菌性保証欠如のためフェニレフリン含有のシリ
トロピカミド・フェニレ
22
ンジ、バッグ製剤について、クラスⅡの自主回収を実施して アメリカ
フリン塩酸塩
いると公表された。
欧州において、プソイドエフェドリン含有製剤は乱用のリスク
があるとして、以下のとおり添付文書を改訂することで
CMDhが合意したもの。また、添付文書に合わせて患者向
塩酸プソイドエフェ
けリーフレットも修正される予定。
23 ドリン含有一般用医
欧州連合
・Special Warnings and Precautions for Useの項に、乱用の
薬品
リスクがあり、連用により耐性が生じ、過量投与につながる
おそれがあるため、推奨される最大用量及び治療期間を超
えるべきではない旨を追記。
4/48