よむ、つかう、まなぶ。
資料3-3 外国での新たな措置の報告状況[1019KB] (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_44308.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
外国での新たな措置の報告状況
(2024年4月1日~2024年7月31日)
措置区分※1
本邦における
措置内容※2
CCDS改訂情報を入手した。 主な改訂内容は以下のとお
り。
・Posology and method of administrationの項について、投
与遅延後の再開用量に関する推奨事項が改訂された。
・Interaction with other medicinal products and other forms
of interactionの項について、相互作用の最も高いリスクは、
ステップアップ投与スケジュール中及びその後最大14日
間、またサイトカイン放出症候群の発現中及びその後最大
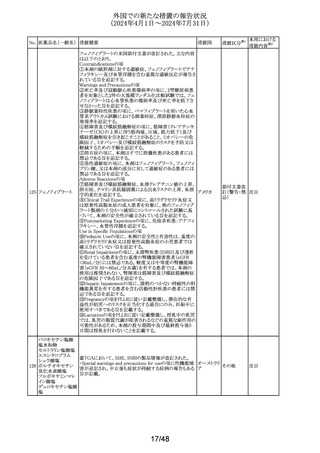
エルラナタマブ(遺 14日間に発生すると予想され、この期間中、治療域が狭い
340
アメリカ
伝子組換え)
高感度のCYP基質を併用している患者では、毒性又は医
薬品濃度をモニタリングし、必要に応じて併用医薬品の量
を調節するよう記載された。
・Fertility, pregnancy and lactationの項において、妊娠する
可能性のある女性における避妊期間及び授乳が推奨され
ない期間について、治療中及び治療中止後4カ月間と記載
された。
・Undesirable effectsの項の注射部位反応、上気道感染、肺
炎、発熱の発現率が更新された。
その他
注目
当該製品の特定のロットにおいて、顧客苦情よりInvalidが増
SARSコロナウイル
加していることを受け、製造元は当該ロットの使用中止・廃
ス核酸キット
341
棄を顧客へ案内する措置を決定した。結果のInvalidによっ アメリカ
インフルエンザウイ
て患者への健康被害は想定されず、影響としては再検査が
ルス核酸キット
必要となることが想定される。
情報提供
対応不要
No. 医薬品名(一般名) 措置概要
T細胞キット
T細胞サブセット
342 キット
B細胞キット
NK細胞キット
措置国
【第1報】【第2報】
一部のロットで異常な染色パターンとして、デブリス集団の アメリカ、
増加とそれに伴う蛍光ダブルポジティブ集団の増加に関す オーストラリ
る苦情が製造元に複数報告された。調査の結果、特定の ア、
Dot Plot図において非特異反応の影響がみられることが確 スイス、
回収
認され、当該製品において同様事象発生の可能性を否定 ドイツ、
できないため、当該製品を回収することを決定した。なお、 フランス、
現在までに、国内外にて本事象に伴う健康被害の報告は カナダ
受けていない。
対応不要
特定ロットのキャリブレーターにおいて一部のシグナル(発
光量)が経時的に低下し、当該製品で患者検体及びコント
ロールを測定した場合に高値傾向を示す可能性があること
が製造元で確認された。そのため、当該製品を使用する顧
アメリカ、
客に当該ロットの使用を中止するよう案内を実施した。当該
イギリス、
B型肝炎ウイルス表 ロットに共通して使用される特定ロットの原材料により製造さ
フランス、 情報提供
343
面抗体キット
れたキャリブレーターを用いて当該製品のキャリブレーショ
オーストラリ
ンを行い社内精度管理試料の測定を行ったところ、出荷時
ア
の試験結果より高値を示したため、製造元では当該原材料
で製造されたキャリブレーターを対象ロットとした。なお、他
のロットについては出荷後の安定性試験で規格の逸脱及
び発光量の低下は確認されていない。
対応不要
海外ユーザーから製造元への問い合わせにより、当該製品
の一部のロットにおいて、構成試薬である抗ヒトIgG血清と抗
多項目免疫グロブリ ヒトκ血清において性能が十分でなく、判定に影響する場
フランス
344
ンキット
合があることが判明した。これを受け、海外製造元は対象
ロット製品の回収を決定し、仏ANSMに市場安全性是正措
置報告を実施した。原因等については調査中である。
回収
対応不要
情報提供
対応不要
サイログロブリン自
345
己抗体キット
海外製造元は一部ロットについて患者検体の測定値が
誤って上昇する可能性があることを確認した。過去のロット
欧州連合
と比較した場合に正のバイアスが観察される場合があるた
め、該当ロットの使用中止を求める案内を発行した。
46/48
(2024年4月1日~2024年7月31日)
措置区分※1
本邦における
措置内容※2
CCDS改訂情報を入手した。 主な改訂内容は以下のとお
り。
・Posology and method of administrationの項について、投
与遅延後の再開用量に関する推奨事項が改訂された。
・Interaction with other medicinal products and other forms
of interactionの項について、相互作用の最も高いリスクは、
ステップアップ投与スケジュール中及びその後最大14日
間、またサイトカイン放出症候群の発現中及びその後最大
エルラナタマブ(遺 14日間に発生すると予想され、この期間中、治療域が狭い
340
アメリカ
伝子組換え)
高感度のCYP基質を併用している患者では、毒性又は医
薬品濃度をモニタリングし、必要に応じて併用医薬品の量
を調節するよう記載された。
・Fertility, pregnancy and lactationの項において、妊娠する
可能性のある女性における避妊期間及び授乳が推奨され
ない期間について、治療中及び治療中止後4カ月間と記載
された。
・Undesirable effectsの項の注射部位反応、上気道感染、肺
炎、発熱の発現率が更新された。
その他
注目
当該製品の特定のロットにおいて、顧客苦情よりInvalidが増
SARSコロナウイル
加していることを受け、製造元は当該ロットの使用中止・廃
ス核酸キット
341
棄を顧客へ案内する措置を決定した。結果のInvalidによっ アメリカ
インフルエンザウイ
て患者への健康被害は想定されず、影響としては再検査が
ルス核酸キット
必要となることが想定される。
情報提供
対応不要
No. 医薬品名(一般名) 措置概要
T細胞キット
T細胞サブセット
342 キット
B細胞キット
NK細胞キット
措置国
【第1報】【第2報】
一部のロットで異常な染色パターンとして、デブリス集団の アメリカ、
増加とそれに伴う蛍光ダブルポジティブ集団の増加に関す オーストラリ
る苦情が製造元に複数報告された。調査の結果、特定の ア、
Dot Plot図において非特異反応の影響がみられることが確 スイス、
回収
認され、当該製品において同様事象発生の可能性を否定 ドイツ、
できないため、当該製品を回収することを決定した。なお、 フランス、
現在までに、国内外にて本事象に伴う健康被害の報告は カナダ
受けていない。
対応不要
特定ロットのキャリブレーターにおいて一部のシグナル(発
光量)が経時的に低下し、当該製品で患者検体及びコント
ロールを測定した場合に高値傾向を示す可能性があること
が製造元で確認された。そのため、当該製品を使用する顧
アメリカ、
客に当該ロットの使用を中止するよう案内を実施した。当該
イギリス、
B型肝炎ウイルス表 ロットに共通して使用される特定ロットの原材料により製造さ
フランス、 情報提供
343
面抗体キット
れたキャリブレーターを用いて当該製品のキャリブレーショ
オーストラリ
ンを行い社内精度管理試料の測定を行ったところ、出荷時
ア
の試験結果より高値を示したため、製造元では当該原材料
で製造されたキャリブレーターを対象ロットとした。なお、他
のロットについては出荷後の安定性試験で規格の逸脱及
び発光量の低下は確認されていない。
対応不要
海外ユーザーから製造元への問い合わせにより、当該製品
の一部のロットにおいて、構成試薬である抗ヒトIgG血清と抗
多項目免疫グロブリ ヒトκ血清において性能が十分でなく、判定に影響する場
フランス
344
ンキット
合があることが判明した。これを受け、海外製造元は対象
ロット製品の回収を決定し、仏ANSMに市場安全性是正措
置報告を実施した。原因等については調査中である。
回収
対応不要
情報提供
対応不要
サイログロブリン自
345
己抗体キット
海外製造元は一部ロットについて患者検体の測定値が
誤って上昇する可能性があることを確認した。過去のロット
欧州連合
と比較した場合に正のバイアスが観察される場合があるた
め、該当ロットの使用中止を求める案内を発行した。
46/48