よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (23 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
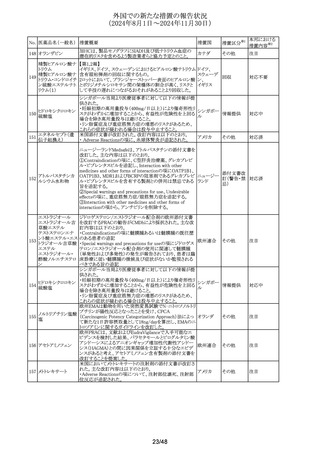
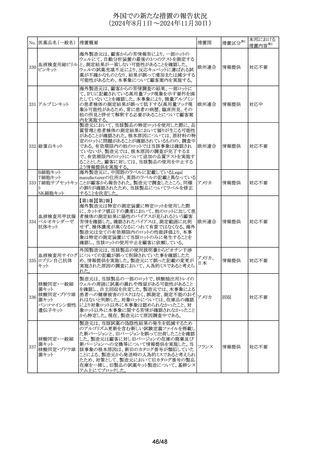
外国での新たな措置の報告状況
(2024年8月1日~2024年11月30日)
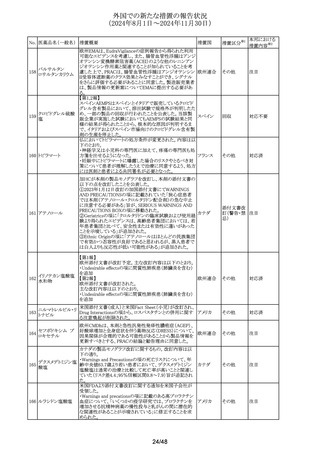
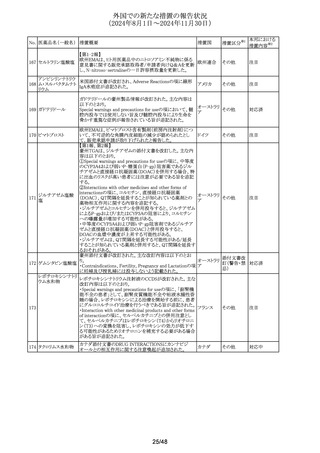
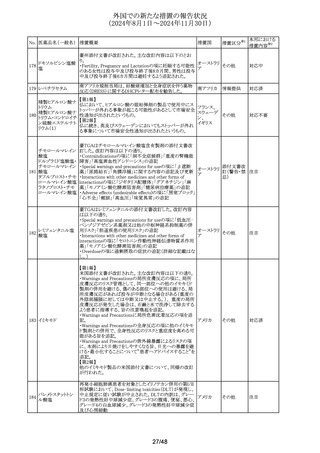
No. 医薬品名(一般名) 措置概要
148 オランザピン
加HCは、製品モノグラフにSIADH及び低ナトリウム血症の
潜在的リスクを含めるよう製造業者らと協力予定とのこと。
措置国
措置区分※1
本邦における
措置内容※2
カナダ
その他
注目
精製ヒアルロン酸ナ 【第1,2報】
トリウム
イギリス、ドイツ、スウェーデンにおけるヒアルロン酸ナトリウム ドイツ、
精製ヒアルロン酸ナ 含有眼粘弾剤の回収に関するもの。
スウェーデ
149
回収
トリウム・コンドロイチ 2ロットにおいて、プランジャーストッパー表面のヒアルロン酸 ン、
ン硫酸エステルナト とポリジメチルシロキサン間の架橋体の割合が高く、リスクと イギリス
リウム(1)
して手技の遅れにつながるおそれがあることより回収した。
シンガポール当局より医療従事者に対して以下の情報が提
供された。
・妊娠初期の高用量投与(400mg/日以上)により催奇形性リ
ヒドロキシクロロキン
シンガポー
150
スクがわずかに増加することから、有益性が危険性を上回る
情報提供
硫酸塩
ル
場合を除き高用量投与は避けること。
・リン脂質症及び重症筋無力症の増悪のリスクがあるため、
これらの症状が疑われる場合は投与中止すること。
エタネルセプト(遺 米国添付文書が改訂された。改訂内容は以下のとおり。
151
アメリカ
その他
伝子組換え)
・ Adverse Reactionsの項に、糸球体腎炎が追記された。
152
アトルバスタチンカ
ルシウム水和物
対応不要
対応中
対応済
ニュージーランドMedsafeは、アトルバスタチンの添付文書を
改訂した。主な内容は以下のとおり。
①Contraindicationの項に、C型肝炎治療薬、グレカプレビ
ル・ピブレンタスビルを追記し、Interaction with other
medicines and other forms of interactionの項にOATP1B1、
添付文書改
OATP1B3、MDR1およびBCRPの阻害剤であるグレカプレビ ニュージー
訂(警告・禁 対応済
ル・ピブレンタスビルを含有する製剤との併用は禁忌である ランド
忌)
旨を追記する。
②Special warnings and precautions for use、Undesirable
effectsの項に、重症筋無力症/眼筋無力症を追記する。
③Interaction with other medicines and other forms of
interactionの項から、アンチピリンを削除する。
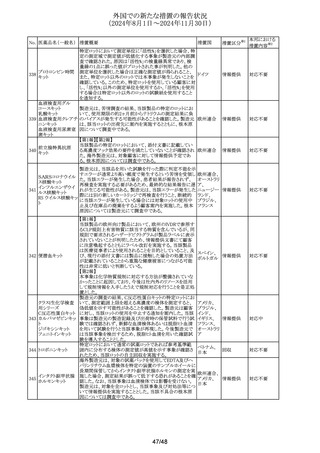
エストラジオール
ジドロゲステロン/エストラジオール配合剤の欧州添付文書
エストラジオール吉 を改訂するPRACの勧告がCMDhにより採択された。主な改
草酸エステル
訂内容は以下のとおり。
テストステロンエナ ・Contraindicationsの項に髄膜腫あるいは髄膜腫の既往歴
ント酸エステル・エス のある患者の追記
153
欧州連合 その他
トラジオール吉草酸 ・Special warnings and precautions for useの項にジドロゲス
エステル
テロン/エストラジオール配合剤の使用に関連して髄膜腫
エストラジオール・ (単発性および多発性)の発生が報告されており、患者は臨
酢酸ノルエチステロ 床診療に従い髄膜腫の徴候及び症状がないか監視される
ン
べきである旨の追記
シンガポール当局より医療従事者に対して以下の情報が提
供された。
・妊娠初期の高用量投与(400mg/日以上)により催奇形性リ
ヒドロキシクロロキン
シンガポー
154
スクがわずかに増加することから、有益性が危険性を上回る
情報提供
硫酸塩
ル
場合を除き高用量投与は避けること。
・リン脂質症及び重症筋無力症の増悪のリスクがあるため、
これらの症状が疑われる場合は投与中止すること。
欧州EMAは動物を用いた突然変異試験でN-ニトロソノルトリ
プチリンが陽性反応となったことを受け、CPCA
ノルトリプチリン塩酸
155
(Carcinogenic Potency Categorization Approach)法によっ オランダ
その他
塩
て新たな1日許容摂取量として18ng/dayを算出し、EMAのニ
トロソアミンに関するガイドラインを改訂した。
欧州PRACは、文献およびEudraVigilanceで入手可能なエ
ビデンスを検討した結果、パラセタモールとピログルタミン酸
アシドーシスによるアニオンギャップ増加性代謝性アシドー
156 アセトアミノフェン
欧州連合 その他
シス(HAGMA)との間に因果関係を立証する十分なエビデ
ンスがあると考え、アセトアミノフェン含有製剤の添付文書を
改訂することを提案した。
米国においてメトトレキサートの注射剤の添付文書が改訂さ
れた。主な改訂内容は以下のとおり。
157 メトトレキサート
アメリカ
その他
・Adverse Reactionsの項について、注射部位壊死、注射部
位反応が追記された。
23/48
注目
対応中
注目
注目
注目
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
148 オランザピン
加HCは、製品モノグラフにSIADH及び低ナトリウム血症の
潜在的リスクを含めるよう製造業者らと協力予定とのこと。
措置国
措置区分※1
本邦における
措置内容※2
カナダ
その他
注目
精製ヒアルロン酸ナ 【第1,2報】
トリウム
イギリス、ドイツ、スウェーデンにおけるヒアルロン酸ナトリウム ドイツ、
精製ヒアルロン酸ナ 含有眼粘弾剤の回収に関するもの。
スウェーデ
149
回収
トリウム・コンドロイチ 2ロットにおいて、プランジャーストッパー表面のヒアルロン酸 ン、
ン硫酸エステルナト とポリジメチルシロキサン間の架橋体の割合が高く、リスクと イギリス
リウム(1)
して手技の遅れにつながるおそれがあることより回収した。
シンガポール当局より医療従事者に対して以下の情報が提
供された。
・妊娠初期の高用量投与(400mg/日以上)により催奇形性リ
ヒドロキシクロロキン
シンガポー
150
スクがわずかに増加することから、有益性が危険性を上回る
情報提供
硫酸塩
ル
場合を除き高用量投与は避けること。
・リン脂質症及び重症筋無力症の増悪のリスクがあるため、
これらの症状が疑われる場合は投与中止すること。
エタネルセプト(遺 米国添付文書が改訂された。改訂内容は以下のとおり。
151
アメリカ
その他
伝子組換え)
・ Adverse Reactionsの項に、糸球体腎炎が追記された。
152
アトルバスタチンカ
ルシウム水和物
対応不要
対応中
対応済
ニュージーランドMedsafeは、アトルバスタチンの添付文書を
改訂した。主な内容は以下のとおり。
①Contraindicationの項に、C型肝炎治療薬、グレカプレビ
ル・ピブレンタスビルを追記し、Interaction with other
medicines and other forms of interactionの項にOATP1B1、
添付文書改
OATP1B3、MDR1およびBCRPの阻害剤であるグレカプレビ ニュージー
訂(警告・禁 対応済
ル・ピブレンタスビルを含有する製剤との併用は禁忌である ランド
忌)
旨を追記する。
②Special warnings and precautions for use、Undesirable
effectsの項に、重症筋無力症/眼筋無力症を追記する。
③Interaction with other medicines and other forms of
interactionの項から、アンチピリンを削除する。
エストラジオール
ジドロゲステロン/エストラジオール配合剤の欧州添付文書
エストラジオール吉 を改訂するPRACの勧告がCMDhにより採択された。主な改
草酸エステル
訂内容は以下のとおり。
テストステロンエナ ・Contraindicationsの項に髄膜腫あるいは髄膜腫の既往歴
ント酸エステル・エス のある患者の追記
153
欧州連合 その他
トラジオール吉草酸 ・Special warnings and precautions for useの項にジドロゲス
エステル
テロン/エストラジオール配合剤の使用に関連して髄膜腫
エストラジオール・ (単発性および多発性)の発生が報告されており、患者は臨
酢酸ノルエチステロ 床診療に従い髄膜腫の徴候及び症状がないか監視される
ン
べきである旨の追記
シンガポール当局より医療従事者に対して以下の情報が提
供された。
・妊娠初期の高用量投与(400mg/日以上)により催奇形性リ
ヒドロキシクロロキン
シンガポー
154
スクがわずかに増加することから、有益性が危険性を上回る
情報提供
硫酸塩
ル
場合を除き高用量投与は避けること。
・リン脂質症及び重症筋無力症の増悪のリスクがあるため、
これらの症状が疑われる場合は投与中止すること。
欧州EMAは動物を用いた突然変異試験でN-ニトロソノルトリ
プチリンが陽性反応となったことを受け、CPCA
ノルトリプチリン塩酸
155
(Carcinogenic Potency Categorization Approach)法によっ オランダ
その他
塩
て新たな1日許容摂取量として18ng/dayを算出し、EMAのニ
トロソアミンに関するガイドラインを改訂した。
欧州PRACは、文献およびEudraVigilanceで入手可能なエ
ビデンスを検討した結果、パラセタモールとピログルタミン酸
アシドーシスによるアニオンギャップ増加性代謝性アシドー
156 アセトアミノフェン
欧州連合 その他
シス(HAGMA)との間に因果関係を立証する十分なエビデ
ンスがあると考え、アセトアミノフェン含有製剤の添付文書を
改訂することを提案した。
米国においてメトトレキサートの注射剤の添付文書が改訂さ
れた。主な改訂内容は以下のとおり。
157 メトトレキサート
アメリカ
その他
・Adverse Reactionsの項について、注射部位壊死、注射部
位反応が追記された。
23/48
注目
対応中
注目
注目
注目