よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (38 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
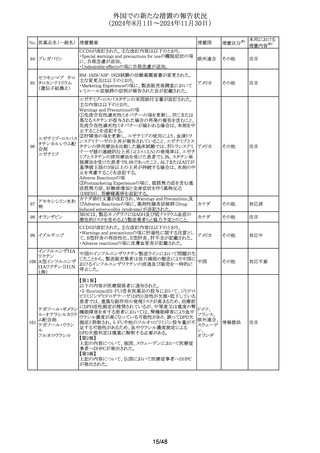
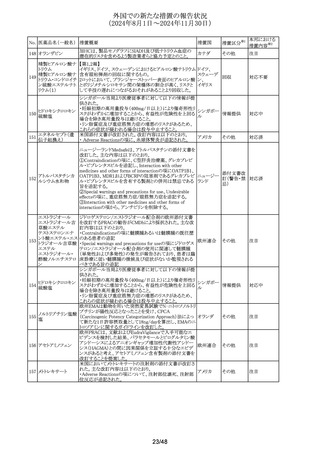
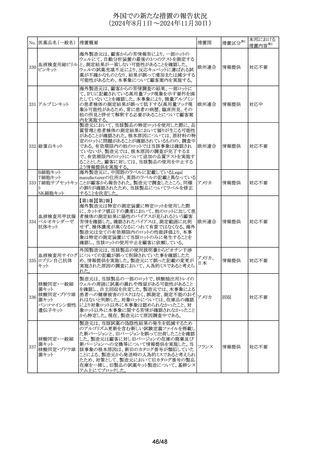
外国での新たな措置の報告状況
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
モルヒネ塩酸塩水
和物
270
フェンタニルクエン
酸塩
措置国
米国FDAは、opioid鎮痛剤の安全な破棄を強化するため、
REMSの変更を承認したというもの。2025年3月31日までに,
外来薬局やその他のopioid鎮痛剤の調剤者に対し,要請に アメリカ
応じて前払いの薬剤用返送用封筒の提供を開始することが
義務付けられるとのこと。
措置区分※1
本邦における
措置内容※2
その他
対応不要
精製ヒアルロン酸ナ
トリウム
オーストラリ
豪、仏、英における、ヒアルロン酸眼粘弾剤の無菌性に関す
精製ヒアルロン酸ナ
ア、
271
る問題(ブリスター製品の穴あき欠陥)を理由としたリコール
回収
トリウム・コンドロイチ
フランス、
に関するもの。
ン硫酸エステルナト
イギリス
リウム(1)
対応不要
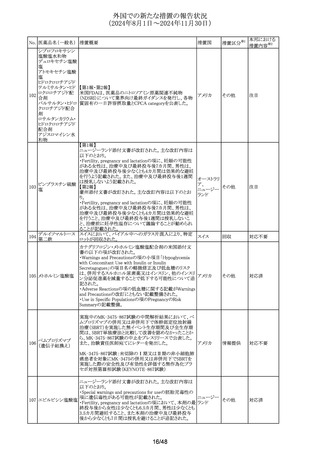
トリメトプリム単剤の豪州添付文書が改訂されたもの。主な改
訂内容は以下の通り。
・Special warnings and precautions for useの項に、「未熟児
スルファメトキサゾー 又は生後数週間の乳児には投与しないこと」を追記。
オーストラリ
272
その他
ル・トリメトプリム
・Interactions with other medicines and other forms of
ア
interactionsの項に、pyrimethamineを追記
・Adverse effects (undesirable effects)の項に、 造血への影
響、胃腸障害を追記。
対応済
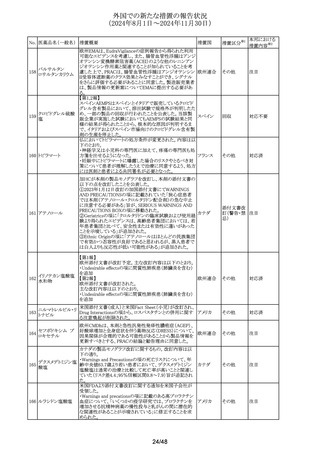
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
・Special warnings and precautions for useの項に、重度の
腎機能障害患者又は末期腎疾患患者では、ギルテリチニブ
の曝露量が増加する可能性があり、投与中はQT延長等の
発現を注意深く監視する必要がある旨が記載された。 なお
ギルテリチニブフマ
オーストラリ
273
腎機能障害患者において用量調節は不要とする記載に変
その他
ル酸塩
ア
更はない。
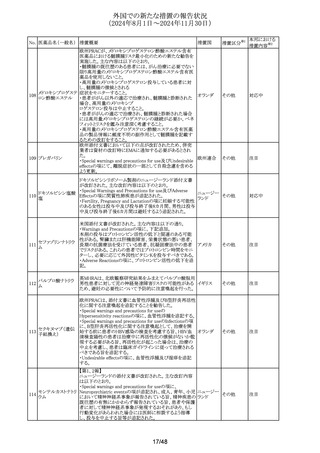
・PHARMACOKINETIC PROPERTIESの項の腎機能障害患
者に関する記載が変更され、重度の腎機能障害、末期腎疾
患の患者では、腎機能が正常な被験者と比較してギルテリ
チニブの平均Cmaxが1.4倍、平均AUCinfが1.5倍となること
が確認された旨が記載された。
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
タモキシフェンクエ ・Special Warnings and Precautions for useの項にQT延長、 オーストラリ
274
その他
ン酸塩
心臓の合併症の基礎的リスクを有する患者において、QT間 ア
隔延長の可能性があることから、ECG、電解質のモニタリン
グを推奨する旨が記載された。
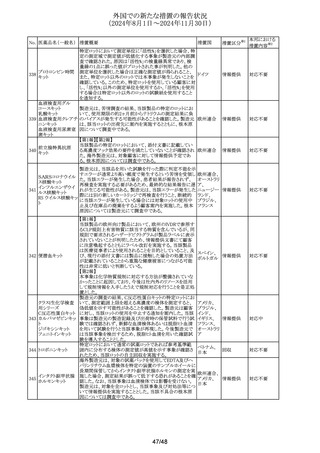
ドイツBfArMは、ジクロフェナクナトリウムの局所製剤の添付
文書について、以下の改訂をするよう勧告を行った。
<点眼用剤を除く局所製剤>
・Contraindicationsの項について、妊娠後期を禁忌とする。
・Fertility, pregnancy and lactationの項について、妊娠前
期及び妊娠中期では必要な場合のみ使用し、使用の際に
は可能な限り使用量及び使用期間を少なくすることを追記
する。
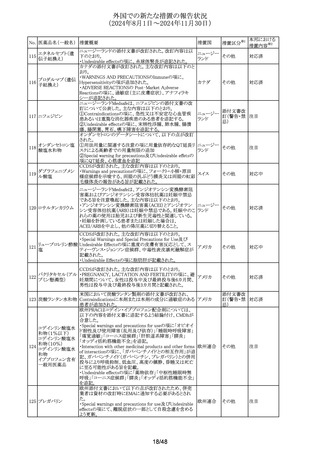
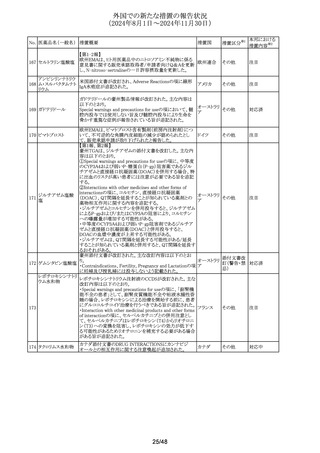
ジクロフェナクナトリ <点眼用剤>
275
ドイツ
ウム
Fertility, Pregnancy and Lactationの項について、妊娠中の
使用による臨床データはなく、全身曝露量が胚/胎児に有
害であるかどうかは不明である旨、妊娠前期及び妊娠中期
では必要な場合のみ使用し、使用の際には可能な限り使用
量及び使用期間を少なくすること、妊娠後期には、ジクロ
フェナクを含むプロスタグランジン合成酵素阻害薬の全身
使用は、胎児に心肺および腎毒性を誘発する可能性、母子
ともに出血が長引き陣痛が遅れることがあることから妊娠後
期には推奨されない旨を追記する。
38/48
その他
対応不要
注目
対応不要
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
モルヒネ塩酸塩水
和物
270
フェンタニルクエン
酸塩
措置国
米国FDAは、opioid鎮痛剤の安全な破棄を強化するため、
REMSの変更を承認したというもの。2025年3月31日までに,
外来薬局やその他のopioid鎮痛剤の調剤者に対し,要請に アメリカ
応じて前払いの薬剤用返送用封筒の提供を開始することが
義務付けられるとのこと。
措置区分※1
本邦における
措置内容※2
その他
対応不要
精製ヒアルロン酸ナ
トリウム
オーストラリ
豪、仏、英における、ヒアルロン酸眼粘弾剤の無菌性に関す
精製ヒアルロン酸ナ
ア、
271
る問題(ブリスター製品の穴あき欠陥)を理由としたリコール
回収
トリウム・コンドロイチ
フランス、
に関するもの。
ン硫酸エステルナト
イギリス
リウム(1)
対応不要
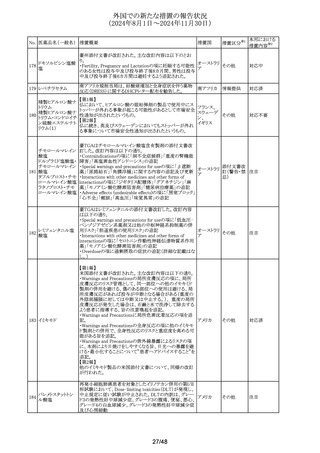
トリメトプリム単剤の豪州添付文書が改訂されたもの。主な改
訂内容は以下の通り。
・Special warnings and precautions for useの項に、「未熟児
スルファメトキサゾー 又は生後数週間の乳児には投与しないこと」を追記。
オーストラリ
272
その他
ル・トリメトプリム
・Interactions with other medicines and other forms of
ア
interactionsの項に、pyrimethamineを追記
・Adverse effects (undesirable effects)の項に、 造血への影
響、胃腸障害を追記。
対応済
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
・Special warnings and precautions for useの項に、重度の
腎機能障害患者又は末期腎疾患患者では、ギルテリチニブ
の曝露量が増加する可能性があり、投与中はQT延長等の
発現を注意深く監視する必要がある旨が記載された。 なお
ギルテリチニブフマ
オーストラリ
273
腎機能障害患者において用量調節は不要とする記載に変
その他
ル酸塩
ア
更はない。
・PHARMACOKINETIC PROPERTIESの項の腎機能障害患
者に関する記載が変更され、重度の腎機能障害、末期腎疾
患の患者では、腎機能が正常な被験者と比較してギルテリ
チニブの平均Cmaxが1.4倍、平均AUCinfが1.5倍となること
が確認された旨が記載された。
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
タモキシフェンクエ ・Special Warnings and Precautions for useの項にQT延長、 オーストラリ
274
その他
ン酸塩
心臓の合併症の基礎的リスクを有する患者において、QT間 ア
隔延長の可能性があることから、ECG、電解質のモニタリン
グを推奨する旨が記載された。
ドイツBfArMは、ジクロフェナクナトリウムの局所製剤の添付
文書について、以下の改訂をするよう勧告を行った。
<点眼用剤を除く局所製剤>
・Contraindicationsの項について、妊娠後期を禁忌とする。
・Fertility, pregnancy and lactationの項について、妊娠前
期及び妊娠中期では必要な場合のみ使用し、使用の際に
は可能な限り使用量及び使用期間を少なくすることを追記
する。
ジクロフェナクナトリ <点眼用剤>
275
ドイツ
ウム
Fertility, Pregnancy and Lactationの項について、妊娠中の
使用による臨床データはなく、全身曝露量が胚/胎児に有
害であるかどうかは不明である旨、妊娠前期及び妊娠中期
では必要な場合のみ使用し、使用の際には可能な限り使用
量及び使用期間を少なくすること、妊娠後期には、ジクロ
フェナクを含むプロスタグランジン合成酵素阻害薬の全身
使用は、胎児に心肺および腎毒性を誘発する可能性、母子
ともに出血が長引き陣痛が遅れることがあることから妊娠後
期には推奨されない旨を追記する。
38/48
その他
対応不要
注目
対応不要