よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (27 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
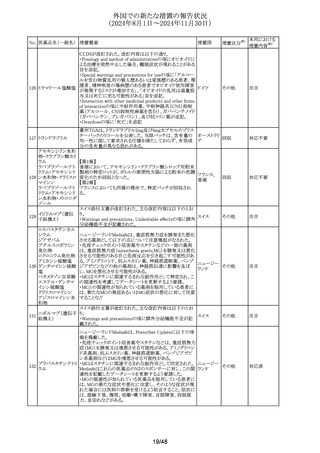
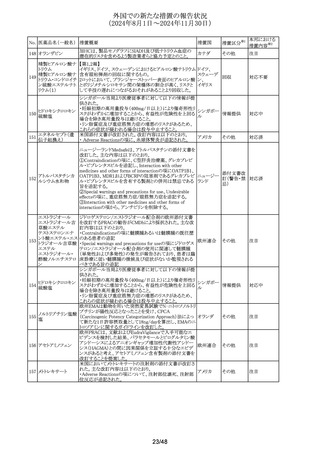
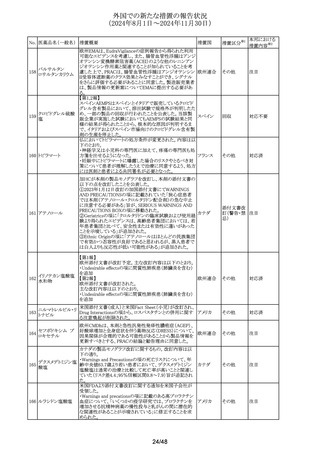
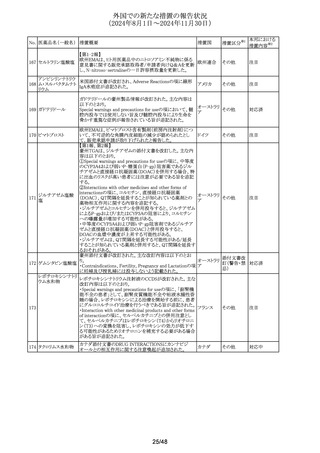
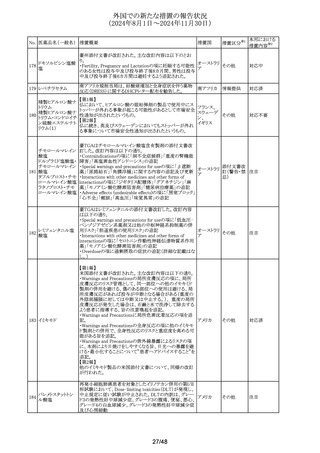
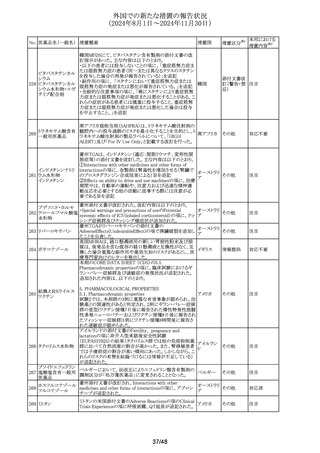
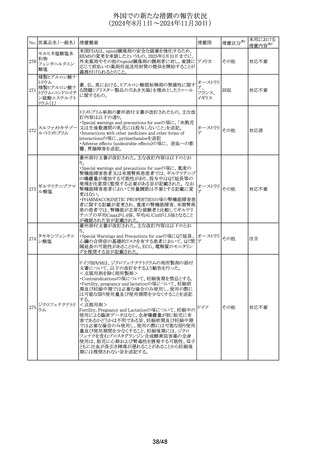
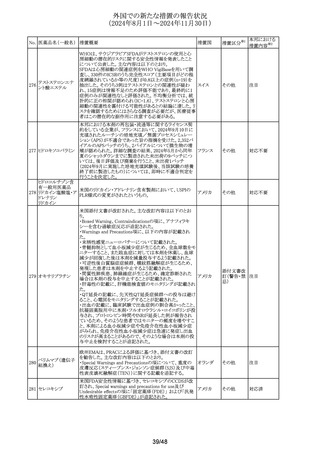
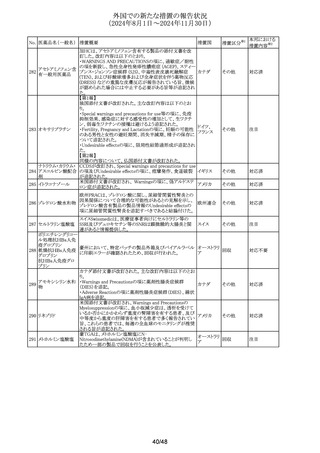
外国での新たな措置の報告状況
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
ドキソルビシン塩酸
オーストラリ
178
・Fertility, Pregnancy and Lactationの項に妊娠する可能性
その他
塩
ア
のある女性は投与中及び投与終了後8カ月間、男性は投与
中及び投与終了後6カ月間は避妊するよう追記された。
179 レベチラセタム
南アフリカ規制当局は、好酸球増加と全身症状を伴う薬物
反応(DRESS)に関するDHCPレター配布を勧告した。
南アフリカ 情報提供
【第1報】
精製ヒアルロン酸ナ
仏において、ヒアルロン酸の眼粘弾剤の製品で使用中にス
トリウム
フランス、
トッパーが外れる事象が起こる可能性があるとして市場安全
精製ヒアルロン酸ナ
スウェーデ
180
性通知が出されたというもの。
その他
トリウム・コンドロイチ
ン、
【第2報】
ン硫酸エステルナト
イギリス
仏に続き、英及びスウェーデンにおいてもストッパーが外れ
リウム(1)
る事象について市場安全性通知が出されたというもの。
本邦における
措置内容※2
対応中
対応済
対応不要
豪TGAはチモロールマレイン酸塩含有製剤の添付文書改
チモロールマレイン 訂した。改訂内容は以下の通り。
酸塩
・Contraindicationsの項に「洞不全症候群」「重度の腎機能
ドルゾラミド塩酸塩・ 障害」「高塩素血性アシドーシス」の追記
チモロールマレイン ・Special warnings and precautions for useの項に「β遮断
添付文書改
オーストラリ
181 酸塩
薬」「尿路結石」「角膜浮腫」に関する内容の追記及び更新
訂(警告・禁 注目
ア
タフルプロスト・チモ ・Interactions with other medicines and other forms of
忌)
ロールマレイン酸塩 interactionsの項に「ジギタリス配糖体」「グアネチジン」「麻
ラタノプロスト・チモ 薬」「モノアミン酸化酵素阻害剤」「糖尿病治療薬」の追記
ロールマレイン酸塩 ・Adverse effects (undesirable effects)の項に「房室ブロック」
「心不全」「頻脈」「高血圧」「味覚異常」の追記
182
レミフェンタニル塩
酸塩
183 イミキモド
184
バレメトスタットトシ
ル酸塩
豪TGAはレミフェンタニルの添付文書改訂した。改訂内容
は以下の通り。
・Special warnings and precautions for useの項に「低血圧ベンゾジアゼピン系薬剤又は他の中枢神経系抑制薬の併
用リスク」「胆道疾患の使用リスク」の追記
オーストラリ
その他
・Interactions with other medicines and other forms of
ア
interactionsの項に「セロトニン作動性神経伝達物質系作用
薬」「モノアミン酸化酵素阻害剤」の追記
・Overdoseの項に過剰摂取の症状の追記(詳細な記載はな
し。)
注目
【第1報】
米国添付文書が改訂された。主な改訂内容は以下の通り。
・Warnings and Precautionsの局所皮膚反応の項に、局所
皮膚反応のリスク管理として、同一部位への他のイモキミド
製剤の併用を避ける、傷のある部位への使用は避ける、局
所皮膚反応があれば投与が中断となる場合がある(重度の
外陰部腫脹に対しては中断又は中止する。)、 重度の局所
皮膚反応が発生した場合は、石鹸と水で洗浄して除去する
よう患者に指導する、旨の注意喚起を追記。
・Warnings and Precautionsに局所色素沈着反応の項を追
記。
アメリカ
・Warnings and Precautionsの全身反応の項に他のイミキモ
ド製剤との併用で、全身性反応のリスクと重症度を高める可
能がある旨を追記。
・Warnings and Precautionsの紫外線暴露によるリスクの項
に、本剤により日焼けをしやすくなる旨、日光への暴露を避
ける・最小化することについて”患者へアドバイスすること”を
追記。
【第2報】
他のイミキモド製品の米国添付文書について、同様の改訂
が行われた。
その他
対応済
再発小細胞肺癌患者を対象としたイリノテカン併用の第I/II
相試験において、Dose-limiting toxicities(DLT)が発現し、
中止規定に従い試験が中止された。DLTの内訳は、グレー
アメリカ
ド3の発熱性好中球減少症、グレード3の腹痛、便秘、悪心、
グレード4の白血球減少、グレード3の発熱性好中球減少症
及び心房細動
その他
注目
27/48
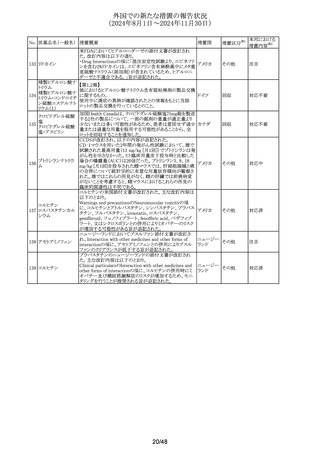
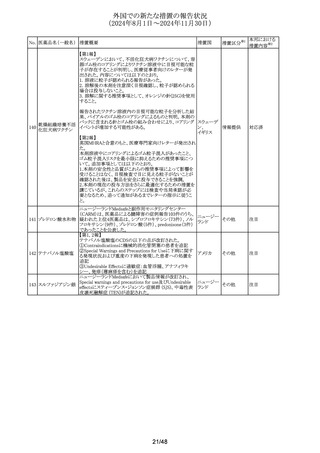
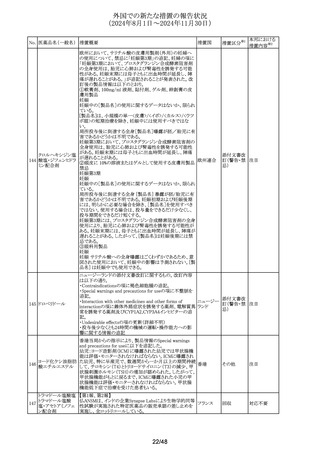
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
豪州添付文書が改訂された。主な改訂内容は以下のとお
り。
ドキソルビシン塩酸
オーストラリ
178
・Fertility, Pregnancy and Lactationの項に妊娠する可能性
その他
塩
ア
のある女性は投与中及び投与終了後8カ月間、男性は投与
中及び投与終了後6カ月間は避妊するよう追記された。
179 レベチラセタム
南アフリカ規制当局は、好酸球増加と全身症状を伴う薬物
反応(DRESS)に関するDHCPレター配布を勧告した。
南アフリカ 情報提供
【第1報】
精製ヒアルロン酸ナ
仏において、ヒアルロン酸の眼粘弾剤の製品で使用中にス
トリウム
フランス、
トッパーが外れる事象が起こる可能性があるとして市場安全
精製ヒアルロン酸ナ
スウェーデ
180
性通知が出されたというもの。
その他
トリウム・コンドロイチ
ン、
【第2報】
ン硫酸エステルナト
イギリス
仏に続き、英及びスウェーデンにおいてもストッパーが外れ
リウム(1)
る事象について市場安全性通知が出されたというもの。
本邦における
措置内容※2
対応中
対応済
対応不要
豪TGAはチモロールマレイン酸塩含有製剤の添付文書改
チモロールマレイン 訂した。改訂内容は以下の通り。
酸塩
・Contraindicationsの項に「洞不全症候群」「重度の腎機能
ドルゾラミド塩酸塩・ 障害」「高塩素血性アシドーシス」の追記
チモロールマレイン ・Special warnings and precautions for useの項に「β遮断
添付文書改
オーストラリ
181 酸塩
薬」「尿路結石」「角膜浮腫」に関する内容の追記及び更新
訂(警告・禁 注目
ア
タフルプロスト・チモ ・Interactions with other medicines and other forms of
忌)
ロールマレイン酸塩 interactionsの項に「ジギタリス配糖体」「グアネチジン」「麻
ラタノプロスト・チモ 薬」「モノアミン酸化酵素阻害剤」「糖尿病治療薬」の追記
ロールマレイン酸塩 ・Adverse effects (undesirable effects)の項に「房室ブロック」
「心不全」「頻脈」「高血圧」「味覚異常」の追記
182
レミフェンタニル塩
酸塩
183 イミキモド
184
バレメトスタットトシ
ル酸塩
豪TGAはレミフェンタニルの添付文書改訂した。改訂内容
は以下の通り。
・Special warnings and precautions for useの項に「低血圧ベンゾジアゼピン系薬剤又は他の中枢神経系抑制薬の併
用リスク」「胆道疾患の使用リスク」の追記
オーストラリ
その他
・Interactions with other medicines and other forms of
ア
interactionsの項に「セロトニン作動性神経伝達物質系作用
薬」「モノアミン酸化酵素阻害剤」の追記
・Overdoseの項に過剰摂取の症状の追記(詳細な記載はな
し。)
注目
【第1報】
米国添付文書が改訂された。主な改訂内容は以下の通り。
・Warnings and Precautionsの局所皮膚反応の項に、局所
皮膚反応のリスク管理として、同一部位への他のイモキミド
製剤の併用を避ける、傷のある部位への使用は避ける、局
所皮膚反応があれば投与が中断となる場合がある(重度の
外陰部腫脹に対しては中断又は中止する。)、 重度の局所
皮膚反応が発生した場合は、石鹸と水で洗浄して除去する
よう患者に指導する、旨の注意喚起を追記。
・Warnings and Precautionsに局所色素沈着反応の項を追
記。
アメリカ
・Warnings and Precautionsの全身反応の項に他のイミキモ
ド製剤との併用で、全身性反応のリスクと重症度を高める可
能がある旨を追記。
・Warnings and Precautionsの紫外線暴露によるリスクの項
に、本剤により日焼けをしやすくなる旨、日光への暴露を避
ける・最小化することについて”患者へアドバイスすること”を
追記。
【第2報】
他のイミキモド製品の米国添付文書について、同様の改訂
が行われた。
その他
対応済
再発小細胞肺癌患者を対象としたイリノテカン併用の第I/II
相試験において、Dose-limiting toxicities(DLT)が発現し、
中止規定に従い試験が中止された。DLTの内訳は、グレー
アメリカ
ド3の発熱性好中球減少症、グレード3の腹痛、便秘、悪心、
グレード4の白血球減少、グレード3の発熱性好中球減少症
及び心房細動
その他
注目
27/48