よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (29 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
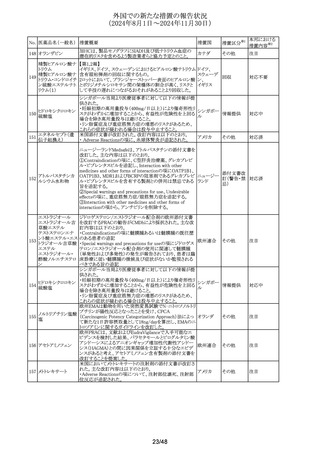
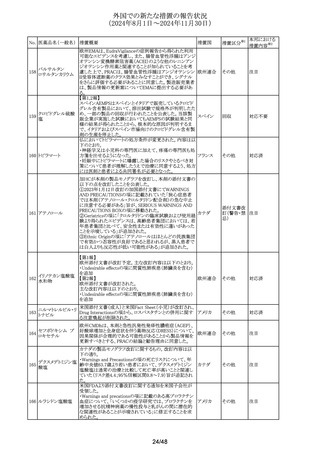
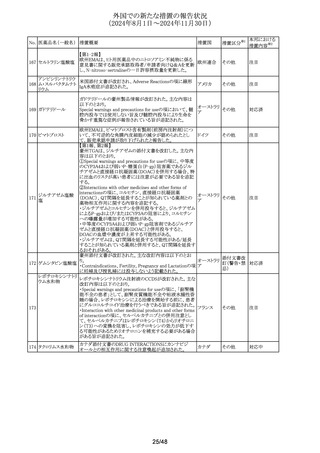
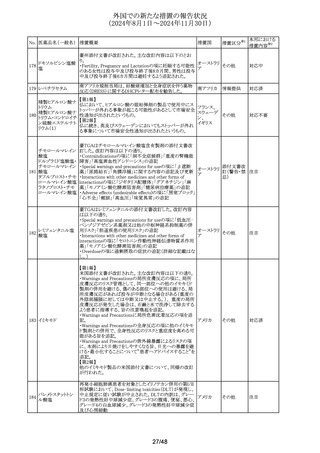
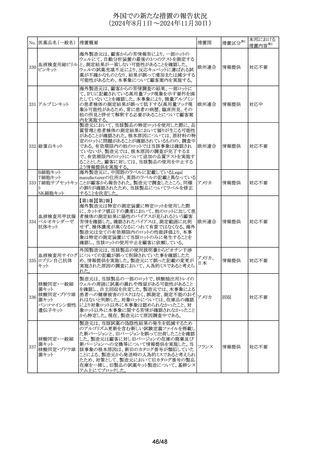
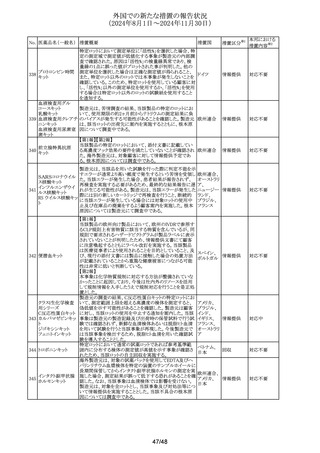
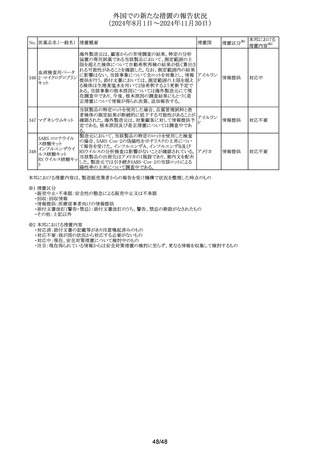
外国での新たな措置の報告状況
(2024年8月1日~2024年11月30日)
措置区分※1
本邦における
措置内容※2
ヒドロコルチゾン含
有一般用医薬品
192
大腸菌死菌・ヒドロ
コルチゾン
ヒドロコルチゾン酪酸エステル(皮膚疾患及びアトピー性皮
膚炎の適応をもつ外用剤)の米国添付文書が改訂された。
主な内容は以下のとおり。
・WARNINGS AND PRECAUTIONSの項に白内障及び緑内 アメリカ
障が報告されていることから、眼への接触は避ける旨の追記
・ADVERSE REACTIONSの項に霧視、白内障、緑内障、眼
圧上昇に関する追記
その他
注目
193 メトトレキサート
ドイツのmedac GmbH(本社)からの情報。以下のバッチを含
むメトジェクト皮下注の複数バッチをリコール予定である。
メトジェクト皮下注シリンジ15mg, 12.5mg, 10mg, 7.5mg
ドイツ
(2407053B/C/D/E)、メトジェクト皮下注ペン7.5mg
(F240341A), 12.5mg (F240346A), 10mg (F240347A), 15mg
(F240348A)
回収
対応不要
No. 医薬品名(一般名) 措置概要
措置国
ドイツ医師会医薬品委員会により、メトトレキサートの誤投与
(連日投与)を予防するための措置として医療専門家および
194 メトトレキサート
患者に対し注意喚起が行われたことが、独BfArMおよびPEI ドイツ
その他
(Paul-Ehrlich-Institut)の医薬品の安全性に関する報告書
の2024年第3号に掲載された。
ジルチアゼムの豪州添付文書が改訂された。改訂内容は以
下のとおり。
オーストラリ
195 コルヒチン
・Interactions with other medicines and other forms of
その他
ア
interactionsの項にコルヒチンが追記され、ジルチアゼムがコ
ルヒチンの代謝酵素を阻害する旨が追記された。
豪州TGAからの情報。Panadeine Forte(codeine phosphate
hemihydrate and paracetamol)、Mersyndol Forte(codeine
コデインリン酸塩水 phosphate hemihydrate, doxylamine succinate and
オーストラリ
196
その他
和物(1%以下)
paracetamol)について、Special warnings and precautions ア
for useにオピオイド誘発性痛覚過敏および異痛症が追記さ
れた。
197
デュロキセチン塩酸 豪州TGAにおいて、製品情報に以下の内容が追記された。 オーストラリ
その他
塩
・Adverse effectsの項に、たこつぼ型心筋症を追記。
ア
豪TGAからのアゼラスチン/フルチカゾン点鼻薬
(DYMISTA)の添付文書改訂情報。Special warnings and
フルチカゾンフラン precautions for useのLocal Effectsに、本剤には塩化ベンザ オーストラリ
198
その他
カルボン酸エステル コニウムが含まれており、ベンザルコニウム塩化物は、特に ア
長期間使用した場合、鼻の中に刺激や腫れを引き起こす可
能性がある旨が追記された。
南アフリカSAHPRAより遺伝毒性のある医薬品の避妊期間
199 パルボシクリブ
に関する通知が発出されたことを受け、本剤の避妊期間に 南アフリカ 情報提供
関するDHPCレターが発出された。
有効性の欠如を理由に小児ユーイング肉腫患者を対象とす
200 パルボシクリブ
るA5481092試験(第Ⅱ相試験)への登録を中止する旨の
アメリカ
情報提供
Dear Investigator Letterが配布された。
英国MHRAは、規格外のトランドラプリル2mg及び4mgカプセ
201 トランドラプリル
イギリス
回収
ルの特定バッチのリコールを公表した。
加国添付文書が改訂され、Warnings and Precautionsの項
202 メトトレキサート
カナダ
その他
に、進行性多巣性白質脳症が追記された。
CCDSについて、以下の点が改訂された。
①Dosage and Method of Administrationに「臨床的に意味
203 バダデュスタット
のあるHb値の上昇が得られない場合、24週間を超えて投薬 アメリカ
その他
を継続すべきではない。」を追記。
②Adverse Reactionsに消化不良、無力症を追記。
欧州において、コール酸に関する製品情報に、フェノバルビ
204 フェノバルビタール タール服用患者では本剤を使用してはならない旨の記載が 欧州連合 その他
あった。
最新のEU-RMPにおいて血栓症、溢出、注射部位壊死が
欧州連合、
205 ヘミン
重要な特定されたリスクとされ、追加のリスク最小化策(医療
その他
イギリス
従事者向け資材の提供)が策定された。
イオベルソールの香港添付文書が改訂された。主な内容は
以下のとおり。
PRECAUTIONSのGENERALに以下の追記。
206 イオベルソール
0~3歳の小児患者における甲状腺機能障害が報告されて 香港
その他
おり、ヨード造影剤に曝露された後は、特に正期産や早産
の新生児では、基礎となる危険因子に基づいて個別に甲状
腺機能モニタリングを行うこと。
29/48
対応済
対応済
注目
注目
注目
対応済
対応不要
対応不要
対応済
注目
対応済
注目
注目
(2024年8月1日~2024年11月30日)
措置区分※1
本邦における
措置内容※2
ヒドロコルチゾン含
有一般用医薬品
192
大腸菌死菌・ヒドロ
コルチゾン
ヒドロコルチゾン酪酸エステル(皮膚疾患及びアトピー性皮
膚炎の適応をもつ外用剤)の米国添付文書が改訂された。
主な内容は以下のとおり。
・WARNINGS AND PRECAUTIONSの項に白内障及び緑内 アメリカ
障が報告されていることから、眼への接触は避ける旨の追記
・ADVERSE REACTIONSの項に霧視、白内障、緑内障、眼
圧上昇に関する追記
その他
注目
193 メトトレキサート
ドイツのmedac GmbH(本社)からの情報。以下のバッチを含
むメトジェクト皮下注の複数バッチをリコール予定である。
メトジェクト皮下注シリンジ15mg, 12.5mg, 10mg, 7.5mg
ドイツ
(2407053B/C/D/E)、メトジェクト皮下注ペン7.5mg
(F240341A), 12.5mg (F240346A), 10mg (F240347A), 15mg
(F240348A)
回収
対応不要
No. 医薬品名(一般名) 措置概要
措置国
ドイツ医師会医薬品委員会により、メトトレキサートの誤投与
(連日投与)を予防するための措置として医療専門家および
194 メトトレキサート
患者に対し注意喚起が行われたことが、独BfArMおよびPEI ドイツ
その他
(Paul-Ehrlich-Institut)の医薬品の安全性に関する報告書
の2024年第3号に掲載された。
ジルチアゼムの豪州添付文書が改訂された。改訂内容は以
下のとおり。
オーストラリ
195 コルヒチン
・Interactions with other medicines and other forms of
その他
ア
interactionsの項にコルヒチンが追記され、ジルチアゼムがコ
ルヒチンの代謝酵素を阻害する旨が追記された。
豪州TGAからの情報。Panadeine Forte(codeine phosphate
hemihydrate and paracetamol)、Mersyndol Forte(codeine
コデインリン酸塩水 phosphate hemihydrate, doxylamine succinate and
オーストラリ
196
その他
和物(1%以下)
paracetamol)について、Special warnings and precautions ア
for useにオピオイド誘発性痛覚過敏および異痛症が追記さ
れた。
197
デュロキセチン塩酸 豪州TGAにおいて、製品情報に以下の内容が追記された。 オーストラリ
その他
塩
・Adverse effectsの項に、たこつぼ型心筋症を追記。
ア
豪TGAからのアゼラスチン/フルチカゾン点鼻薬
(DYMISTA)の添付文書改訂情報。Special warnings and
フルチカゾンフラン precautions for useのLocal Effectsに、本剤には塩化ベンザ オーストラリ
198
その他
カルボン酸エステル コニウムが含まれており、ベンザルコニウム塩化物は、特に ア
長期間使用した場合、鼻の中に刺激や腫れを引き起こす可
能性がある旨が追記された。
南アフリカSAHPRAより遺伝毒性のある医薬品の避妊期間
199 パルボシクリブ
に関する通知が発出されたことを受け、本剤の避妊期間に 南アフリカ 情報提供
関するDHPCレターが発出された。
有効性の欠如を理由に小児ユーイング肉腫患者を対象とす
200 パルボシクリブ
るA5481092試験(第Ⅱ相試験)への登録を中止する旨の
アメリカ
情報提供
Dear Investigator Letterが配布された。
英国MHRAは、規格外のトランドラプリル2mg及び4mgカプセ
201 トランドラプリル
イギリス
回収
ルの特定バッチのリコールを公表した。
加国添付文書が改訂され、Warnings and Precautionsの項
202 メトトレキサート
カナダ
その他
に、進行性多巣性白質脳症が追記された。
CCDSについて、以下の点が改訂された。
①Dosage and Method of Administrationに「臨床的に意味
203 バダデュスタット
のあるHb値の上昇が得られない場合、24週間を超えて投薬 アメリカ
その他
を継続すべきではない。」を追記。
②Adverse Reactionsに消化不良、無力症を追記。
欧州において、コール酸に関する製品情報に、フェノバルビ
204 フェノバルビタール タール服用患者では本剤を使用してはならない旨の記載が 欧州連合 その他
あった。
最新のEU-RMPにおいて血栓症、溢出、注射部位壊死が
欧州連合、
205 ヘミン
重要な特定されたリスクとされ、追加のリスク最小化策(医療
その他
イギリス
従事者向け資材の提供)が策定された。
イオベルソールの香港添付文書が改訂された。主な内容は
以下のとおり。
PRECAUTIONSのGENERALに以下の追記。
206 イオベルソール
0~3歳の小児患者における甲状腺機能障害が報告されて 香港
その他
おり、ヨード造影剤に曝露された後は、特に正期産や早産
の新生児では、基礎となる危険因子に基づいて個別に甲状
腺機能モニタリングを行うこと。
29/48
対応済
対応済
注目
注目
注目
対応済
対応不要
対応不要
対応済
注目
対応済
注目
注目