よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.4MB] (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_53729.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和6年度第3回 3/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
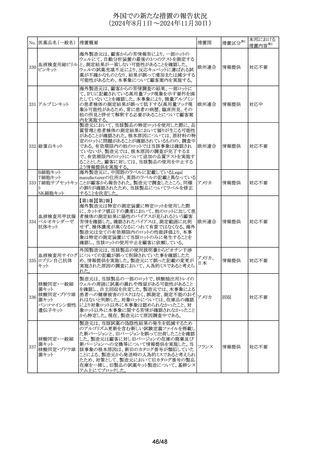
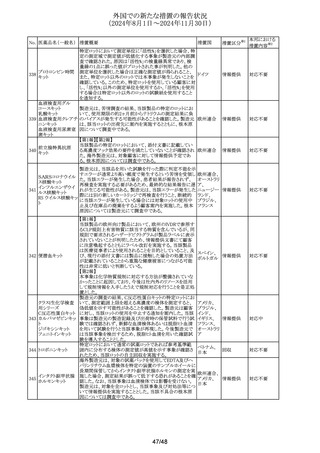
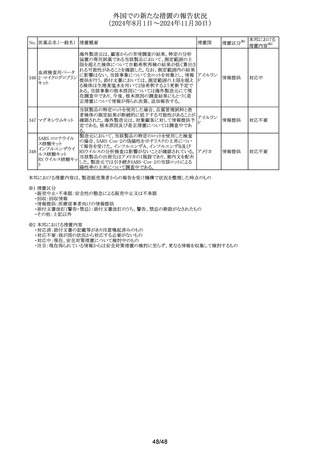
外国での新たな措置の報告状況
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
本邦における
措置内容※2
【第1報】
独BfArMは、メドロキシプロゲステロン酢酸エステル(MPA)
含有医薬品の髄膜腫の発症リスクに関する情報提供するた
め、Direct Healthcare Professional Communications
(DHPCs)を発行した。主な内容は以下のとおり。
・高用量のMPA(注射剤及び100mg以上の経口剤)では、長
期投与した後に髄膜腫を発症するリスクが増加する。
・高用量のMPAで治療を受けた患者は、臨床診療で髄膜腫
の兆候及び症状がないか観察すべきである。
<避妊又は腫瘍以外の適応症の場合(注射剤及び100mg
以上の経口剤)>
・高用量のMPAを含む薬剤は、髄膜腫又は髄膜腫の既往
歴のある患者には禁忌。
・高用量のMPAで治療中の患者において、髄膜腫と診断さ
れた場合は投与を中止する必要がある。
<腫瘍性疾患の適応症の場合>
・高用量のMPAで治療中の患者において、患者が髄膜腫と
診断された場合、本剤による治療継続の必要性は、患者の
ベネフィットとリスクを考慮し、慎重に検討する必要がある。
【第2報】
ドイツ、
メドロキシプロゲステ スウェーデン MPAは、メドロキシプロゲステロン酢酸エステ スウェーデ
217
情報提供
ロン酢酸エステル ル(MPA)含有医薬品の髄膜腫の発症リスクに関して情報提 ン、
供し、Direct Healthcare Professional Communications
イギリス
(DHPCs)を発行した。主な内容は以下のとおり。
・高用量のMPA(注射剤及び100mg以上の経口剤)では、長
期投与した後に髄膜腫を発症するリスクが増加する。
・高用量のMPAで治療を受けた患者は、臨床診療で髄膜腫
の兆候及び症状がないか観察すべきである。
<避妊又は腫瘍以外の適応症の場合(注射剤及び100mg
以上の経口剤)>
・高用量のMPAを含む薬剤は、髄膜腫又は髄膜腫の既往
歴のある患者には禁忌。
・高用量のMPAで治療中の患者において、髄膜腫と診断さ
れた場合は投与を中止する必要がある。
<腫瘍性疾患の応症の場合>
・高用量のMPAで治療中の患者において、患者が髄膜腫と
診断された場合、本剤による治療継続の必要性は、患者の
ベネフィットとリスクを考慮し、慎重に検討する必要がある。
【第3報】
英国MHRAはメドロキシプロゲステロン酢酸エステルを含有
する医薬品の髄膜腫リスクについてDirect Healthcare
Professional Communication (DHPC)を公表した。
対応中
218 シスプラチン
対応不要
不純物/品質劣化を理由とする回収が行われている。
アメリカ
回収
米国添付文書が改訂され、Warnings and Precautionsの過
敏反応の項、及びAdverse Reactionsの項に、「Acute
myocardial ischemia with or without myocardial infarction
219 シプロフロキサシン
アメリカ
その他
occurring as part of an allergic reaction(アレルギー反応の
一部として起こる、心筋梗塞を伴う又は伴わない急性心筋
虚血)」が追記された。
エルサルバドル保健当局は、欧州の措置を受けて製品情
報を改訂し、スティーブンス・ジョンソン症候群 (SJS)、好酸
球増多および全身症状を伴う薬物反応 (DRESS)、抗利尿ホ
レボフロキサシン水 ルモン分泌過剰症(SIADH)、ミオクローヌス、血液障害(白 エルサルバ
220
その他
和物
血球減少、好中球減少、汎血球減少、溶血性貧血、血小板 ドル
減少、再生不良性貧血、無顆粒球症を含む骨髄不全)、躁
病、皮膚色素過剰、大動脈瘤及び大動脈解離を追記するよ
う勧告した。
221 ガバペンチン
豪州TGAにおいて、製品情報に以下の内容が追記された。
オーストラリ
・Fertility, pregnancy and lactationの項に、妊娠カテゴリー
その他
ア
が更新されDとなった。
英国MHRAにおいて、本剤を服用していた患者に関する
Yellow Card報告を受けて、安全性レビューを実施した結
ブロモクリプチンメシ
222
果、分娩後の生理的乳汁分泌予防または抑制に対し本剤 イギリス
ル酸塩
を処方する場合は、特に治療開始後数日間の血圧モニタリ
ングが不可欠であることが示された。
31/48
その他
注目
注目
注目
対応済
(2024年8月1日~2024年11月30日)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
本邦における
措置内容※2
【第1報】
独BfArMは、メドロキシプロゲステロン酢酸エステル(MPA)
含有医薬品の髄膜腫の発症リスクに関する情報提供するた
め、Direct Healthcare Professional Communications
(DHPCs)を発行した。主な内容は以下のとおり。
・高用量のMPA(注射剤及び100mg以上の経口剤)では、長
期投与した後に髄膜腫を発症するリスクが増加する。
・高用量のMPAで治療を受けた患者は、臨床診療で髄膜腫
の兆候及び症状がないか観察すべきである。
<避妊又は腫瘍以外の適応症の場合(注射剤及び100mg
以上の経口剤)>
・高用量のMPAを含む薬剤は、髄膜腫又は髄膜腫の既往
歴のある患者には禁忌。
・高用量のMPAで治療中の患者において、髄膜腫と診断さ
れた場合は投与を中止する必要がある。
<腫瘍性疾患の適応症の場合>
・高用量のMPAで治療中の患者において、患者が髄膜腫と
診断された場合、本剤による治療継続の必要性は、患者の
ベネフィットとリスクを考慮し、慎重に検討する必要がある。
【第2報】
ドイツ、
メドロキシプロゲステ スウェーデン MPAは、メドロキシプロゲステロン酢酸エステ スウェーデ
217
情報提供
ロン酢酸エステル ル(MPA)含有医薬品の髄膜腫の発症リスクに関して情報提 ン、
供し、Direct Healthcare Professional Communications
イギリス
(DHPCs)を発行した。主な内容は以下のとおり。
・高用量のMPA(注射剤及び100mg以上の経口剤)では、長
期投与した後に髄膜腫を発症するリスクが増加する。
・高用量のMPAで治療を受けた患者は、臨床診療で髄膜腫
の兆候及び症状がないか観察すべきである。
<避妊又は腫瘍以外の適応症の場合(注射剤及び100mg
以上の経口剤)>
・高用量のMPAを含む薬剤は、髄膜腫又は髄膜腫の既往
歴のある患者には禁忌。
・高用量のMPAで治療中の患者において、髄膜腫と診断さ
れた場合は投与を中止する必要がある。
<腫瘍性疾患の応症の場合>
・高用量のMPAで治療中の患者において、患者が髄膜腫と
診断された場合、本剤による治療継続の必要性は、患者の
ベネフィットとリスクを考慮し、慎重に検討する必要がある。
【第3報】
英国MHRAはメドロキシプロゲステロン酢酸エステルを含有
する医薬品の髄膜腫リスクについてDirect Healthcare
Professional Communication (DHPC)を公表した。
対応中
218 シスプラチン
対応不要
不純物/品質劣化を理由とする回収が行われている。
アメリカ
回収
米国添付文書が改訂され、Warnings and Precautionsの過
敏反応の項、及びAdverse Reactionsの項に、「Acute
myocardial ischemia with or without myocardial infarction
219 シプロフロキサシン
アメリカ
その他
occurring as part of an allergic reaction(アレルギー反応の
一部として起こる、心筋梗塞を伴う又は伴わない急性心筋
虚血)」が追記された。
エルサルバドル保健当局は、欧州の措置を受けて製品情
報を改訂し、スティーブンス・ジョンソン症候群 (SJS)、好酸
球増多および全身症状を伴う薬物反応 (DRESS)、抗利尿ホ
レボフロキサシン水 ルモン分泌過剰症(SIADH)、ミオクローヌス、血液障害(白 エルサルバ
220
その他
和物
血球減少、好中球減少、汎血球減少、溶血性貧血、血小板 ドル
減少、再生不良性貧血、無顆粒球症を含む骨髄不全)、躁
病、皮膚色素過剰、大動脈瘤及び大動脈解離を追記するよ
う勧告した。
221 ガバペンチン
豪州TGAにおいて、製品情報に以下の内容が追記された。
オーストラリ
・Fertility, pregnancy and lactationの項に、妊娠カテゴリー
その他
ア
が更新されDとなった。
英国MHRAにおいて、本剤を服用していた患者に関する
Yellow Card報告を受けて、安全性レビューを実施した結
ブロモクリプチンメシ
222
果、分娩後の生理的乳汁分泌予防または抑制に対し本剤 イギリス
ル酸塩
を処方する場合は、特に治療開始後数日間の血圧モニタリ
ングが不可欠であることが示された。
31/48
その他
注目
注目
注目
対応済